Command Palette
Search for a command to run...
مهاجمة الأورام الصلبة الثلاثة الرئيسية بشكل مباشر! فريق جامعة شنغهاي جياو تونغ يصدر نظام التعلم العميق لتحسين دقة التنبؤ ببقاء مرضى السرطان

وأشار تقرير أصدرته منظمة الصحة العالمية في عام 2022 إلى أنلقد تجاوزت الأمراض غير المعدية مثل السرطان الأمراض المعدية لتصبح القاتل الأول في العالم.تشير أحدث البيانات الصادرة عن المركز الوطني للسرطان في الصين إلى أنه سيكون هناك ما يقرب من 4.8247 مليون حالة إصابة جديدة بالسرطان و2.5742 مليون حالة وفاة جديدة بالسرطان في الصين في عام 2022.
منذ وقت طويل، كان الناس خائفين من السرطان. ولكن في الواقع، باعتباره مرضًا مزمنًا، يمكن الوقاية من ثلث السرطان، ويمكن علاج الثلث الآخر من خلال الكشف المبكر والتشخيص المبكر والعلاج المبكر، وثلثه غير قابل للشفاء ولكن يمكن السيطرة عليه من خلال العلاج المناسب للحصول على نوعية حياة أفضل وإطالة البقاء على قيد الحياة. ومن بينها، تتضمن الوقاية بشكل أساسي الاهتمام بالصحة الشخصية من خلال تحسين المناعة الذاتية، وإجراء الفحوصات البدنية المنتظمة، وما إلى ذلك. وبعد تشخيص السرطان، يكون التحليل التوقعي مهمًا للغاية.
يشير تشخيص السرطان إلى التنبؤ بالمسار المحتمل ونتيجة مرضى السرطان. يساعد التحليل التشخيصي على تحسين فرص البقاء على قيد الحياة لمرضى السرطان.في الماضي، قام الباحثون بتوصيف البيئة المحيطة بالورم (TME) من منظور التعبير الجيني المكاني استنادًا إلى تكنولوجيا النسخ المكاني (ST) للتمييز بين مجموعات فرعية مختلفة من مرضى السرطان. ومع ذلك، فإن التكلفة العالية والفترة التجريبية الطويلة لـ ST تعوق تطبيقها في مجموعات كبيرة من مرضى السرطان للتنبؤ بالبقاء على قيد الحياة. وبالمقارنة، فإن الصور النسيجية فعالة من حيث التكلفة، ويمكن الوصول إليها بسهولة في الإعدادات السريرية، ويمكن أن توفر معلومات غنية حول مورفولوجيا الورم، مما يجعلها بديلاً أفضل لتحليل TME على المستوى الجزيئي وتمكين تشخيص السرطان بشكل أكثر دقة.
في الآونة الأخيرة، نشرت مجموعة البحث التابعة ليو تشانغ شنغ (كلية العلوم الحياتية والتكنولوجيا / مركز الأبحاث السريرية بكلية الطب)، ومجموعة البحث التابعة لوانغ يوجوانج (كلية العلوم الطبيعية / كلية العلوم الرياضية) من المركز الوطني للرياضيات التطبيقية في شنغهاي (فرع جامعة شنغهاي جياو تونغ) وزملائهما ورقة بحثية بعنوان "تسخير TME الموضح بالصور النسيجية لتحسين تشخيص السرطان من خلال نظام التعلم العميق" في Cell Reports Medicine.طورت هذه الدراسة نظام تعلم عميق يمكنه التنبؤ بمعلومات البيئة الدقيقة للورم لمرضى السرطان دون بيانات النسخ المكاني من خلال صور علم الأمراض النسيجية، وبالتالي تحقيق تشخيص دقيق للسرطان.
أبرز الأبحاث:
- التنبؤ بمعلومات TME من الصور النسيجية المرضية لمرضى السرطان دون بيانات ST
- TME الذي يتميز بـ IGI-DL يحسن دقة التنبؤ ببقاء السرطان
- يتوسع بشكل كبير استخدام معلومات التعبير المكاني للجينات في قواعد البيانات العامة الكبيرة لصور علم الأمراض الطبية الحيوية

عنوان الورقة:
https://www.cell.com/cell-reports-medicine/fulltext/S2666-3791(24)00205-2
اتبع الحساب الرسمي ورد "بيئة الورم" للحصول على ملف PDF كامل
مجموعة البيانات: تقييم عينات الأنسجة من 3 أنواع من الأورام الصلبة
استخدمت هذه الدراسة ثلاث مجموعات بيانات مختلفة لتقييم أداء النموذج على عينات الأنسجة من ثلاثة أنواع مختلفة من الأورام الصلبة: سرطان القولون والمستقيم (CRC)، وسرطان الثدي، وسرطان الخلايا الحرشفية الجلدية (cSCC).
بالنسبة لسرطان القولون والمستقيم،استخدم الباحثون 41492 نقطة من 10 مجموعات بيانات ST لـ 10 مرضى سرطان القولون والمستقيم من مستشفى Ruijin التابع لكلية الطب بجامعة شنغهاي جياو تونغ، والتي تم تسلسلها بواسطة 10 × Visium كمجموعة تحقق من استبعاد مريض واحد، كما هو موضح في الجدول أدناه.

بالنسبة لسرطان الثدي،استخدم الباحثون 34678 بقعة من 92 عينة أنسجة من 27 مريضًا، والتي تم تسلسلها باستخدام تقنية ST التقليدية، كمجموعة تحقق لترك مريض واحد، كما هو موضح في الجدول أدناه.

بالنسبة لسرطان الخلايا الحرشفية في الجلد،استخدم الباحثون 4353 بقعة من 12 عينة أنسجة من أربعة مرضى تم تسلسلها باستخدام تقنية ST التقليدية كمجموعة تحقق لترك مريض واحد، كما هو موضح في الجدول أدناه.

هندسة النموذج: نظام التعلم العميق الجديد يحسن تشخيص السرطان
في هذه الدراسة، قام الباحثون بتطوير نظام التعلم العميق الذي يمكنه تحسين تشخيص السرطان باستخدام TME الموضح في الصور النسيجية.
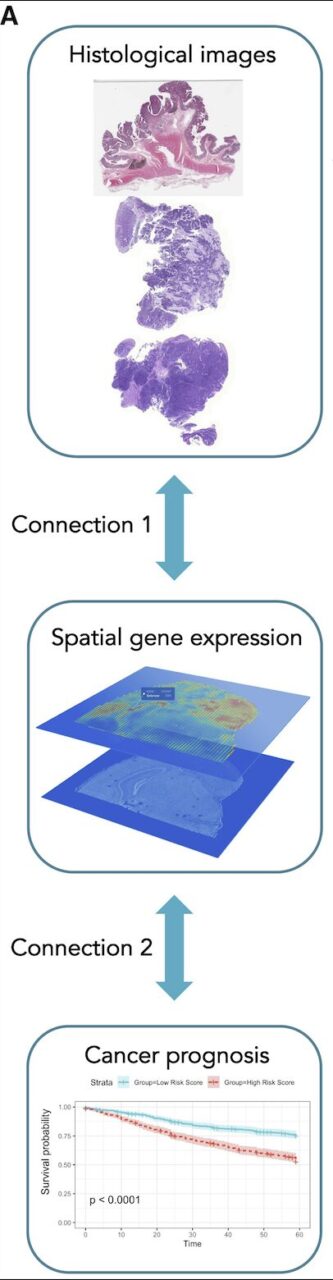
يتكون النظام من جزئين:
الجزء الأول (الاتصال 1 في الشكل أعلاه) هو نموذج يعتمد على التعلم العميق المتكامل للرسم البياني والصورة (IGI-DL)، والذي يستخدم الشبكات العصبية التلافيفية والشبكات العصبية البيانية لإسقاط صور نسيجية ملطخة بالهيماتوكسيلين والإيوزين في مساحة التعبير الجيني.
في الجزء الثاني (الاتصال 2 في الشكل أعلاه)، استخدم الباحثون الرسم البياني الفائق الرقعة والتعبير الجيني المكاني المتوقع من IGI-DL كميزات للعقدة في مجموعة سرطان القولون والمستقيم ومجموعة سرطان الثدي في مجموعة بيانات أطلس جينوم السرطان (TCGA) للتنبؤ بالتشخيص، ثم تم التحقق منه في مجموعة الاختبار الخارجية MCO-CRC (علم الأورام الجزيئي والخلوي لسرطان القولون والمستقيم).
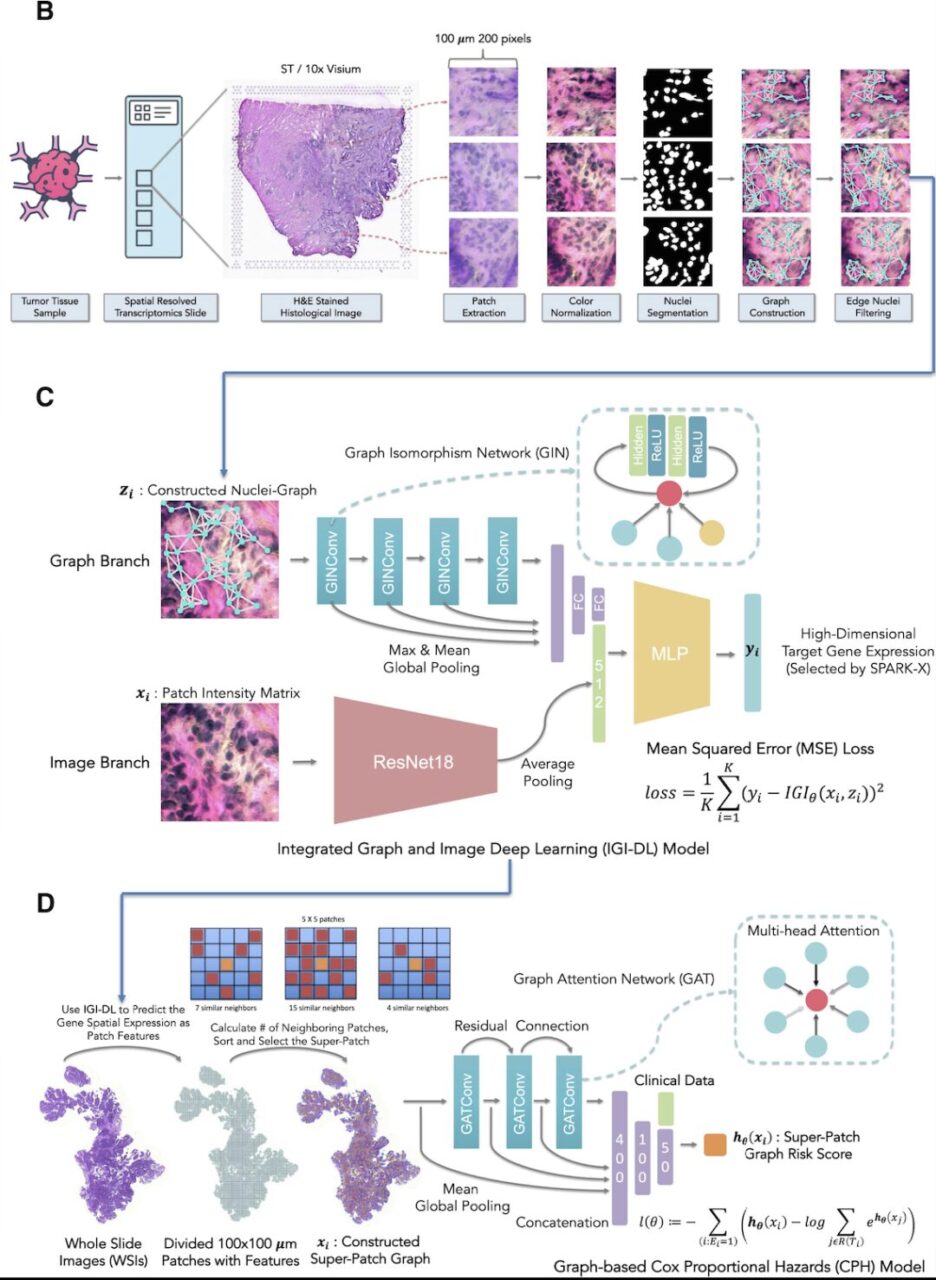
على وجه التحديد، يتضمن بناء النظام ثلاث خطوات: معالجة الصور النسيجية الملطخة بالهيماتوكسيلين والإيوزين مسبقًا، ونموذج التنبؤ بالتعبير الجيني المكاني، ونموذج بقاء الرسم البياني الفائق لرقعة التعبير الجيني المكاني استنادًا إلى التنبؤ.
- معالجة مسبقة للصورة النسيجية الملطخة بالـH&E:أولاً، تم تقسيم كل صورة نسيجية ملطخة بالهيماتوكسيلين والإيوزين إلى بقع متعددة غير متداخلة بحجم 200 × 200 بكسل بدقة 0.5 ميكرومتر/بكسل وفقًا لإحداثيات كل نقطة؛
- نموذج التنبؤ بالتعبير الجيني المكاني:بالنسبة لكل رقعة، قام الباحثون ببناء رسم بياني للنوى، حيث تم تمثيل كل نواة مقسمة بواسطة Hover-Net24 كعقدة، وتم تحديد المسافة بين كل زوج من النوى ما إذا كان هناك اتصال حافة. وبناءً على البنية الموضحة في الشكل C أعلاه، استخدم الباحثون نموذج IGI-DL للتنبؤ بتعبير الجينات المستهدفة في كل نقطة في صورة الأنسجة.
- نموذج بقاء الرسم البياني الفائق الرقعة يعتمد على التعبير الجيني المكاني المتوقع:وللتنبؤ بشكل أكبر بالتشخيص استنادًا إلى TME المحدد من خلال التعبير الجيني المكاني، قام الباحثون ببناء رسم بياني فائق الرقعة من التصوير الكامل للشريحة الملطخة بالهيماتويد والإيوزين (WSI) لكل مريض مصاب بالسرطان، ثم قاموا ببناء نموذج تنبؤ بالبقاء على قيد الحياة يعتمد على الرسم البياني باستخدام الرسم البياني الفائق الرقعة الذي تم إنشاؤه والخصائص السريرية كمدخلات.
نتائج البحث: نموذج IGI-DL يعمل بشكل جيد بشكل عام
بشكل عام، يدمج نموذج IGI-DL الذي تم إنشاؤه في هذه الدراسة مزايا الشبكات العصبية التلافيفية والشبكات العصبية الرسومية، مما يجعل الاستخدام الكامل لشدة البكسل والميزات البنيوية في الصور النسيجية المرضية لتحقيق تنبؤ أكثر دقة لمستويات التعبير المكاني للجين.أظهر النموذج أداءً جيدًا في ثلاثة أنواع من الأورام الصلبة: سرطان القولون والمستقيم، وسرطان الثدي، وسرطان الخلايا الحرشفية الجلدية، مع تحسن متوسط معامل الارتباط بمقدار 0.171 مقارنة بخمس طرق موجودة.

بالنسبة لسرطان القولون والمستقيم، قارن الباحثون ارتباط بيرسون لـ 179 جينًا تنبأت بها IGI-DL مع خمسة نماذج SOTA.حقق IGI-DL متوسط ارتباط بيرسون بلغ 0.343 في المرضى العشرة المحتفظ بهم، متفوقًا بشكل كبير على النماذج الأخرى بمتوسط زيادة بلغ 0.233،كما هو موضح في الصورة أعلاه.

بالنسبة لسرطان الثدي، قارن الباحثون ارتباطات بيرسون لـ 187 جينًا تنبأت بها IGI-DL مع النموذج السابق، وحققت IGI-DL ارتباطًا متوسطًا بلغ 0.231 في 27 مريضًا تم الاحتفاظ بهم. كما هو موضح في الشكل أعلاه،يتفوق نموذج IGI-DL على جميع نماذج SOTA بمتوسط تحسن يبلغ 0.142.

بالنسبة لسرطان الخلايا الحرشفية الجلدية، قارن الباحثون ارتباط بيرسون لـ 487 جينًا تنبأت بها IGI-DL مع النماذج السابقة. حقق IGI-DL ارتباطًا متوسطًا بلغ 0.198 في المرضى الأربعة المحتفظ بهم، وهو أفضل أداء بين جميع النماذج.تم تحسين الأداء المتوسط لنماذج SOTA الأخرى بمقدار 0.131.كما هو موضح في الصورة أعلاه.
من حيث الأداء عبر الأنظمة الأساسية وعبر أنواع السرطان المختلفة، كما هو الحال في التجارب المذكورة أعلاه، فإن أفضل نموذج SOTA ليس ثابتًا للتحقق الداخلي ومجموعات الاختبار الخارجية لأنواع السرطان المختلفة.ومع ذلك، فإن أداء نموذج IGI-DL أفضل دائمًا من النماذج الأخرى، مع تحسن متوسط يبلغ 0.171، مما يُظهر قدرة تعميم جيدة عبر الأنظمة الأساسية.
علاوة على ذلك، قام الباحثون بالتحقيق في أداء التنبؤ بالسرطان المتقاطع لـ IGI-DL، وقد أظهر نموذجه المدرب على سرطان القولون والمستقيم أداءً جيدًا في التحقق الداخلي ومجموعات الاختبار الخارجية لسرطان الخلايا الحرشفية الجلدية، مع متوسط ارتباطات بلغ 0.204 و0.143 على التوالي. ومع ذلك، كانت معظم أداءات التنبؤ بالسرطان المتقاطع أقل من تلك التي تم تحقيقها عند التدريب والاختبار على نوع واحد من السرطان.تشير هذه النتيجة إلى أن التعبير الجيني المكاني في مناطق الورم له خصوصية معينة فيما يتعلق بالسرطان، وهناك صعوبات متأصلة في التنبؤ بالسرطان المتقاطع.

فيما يتعلق بأداء التنبؤ التكهنى، في مجموعة سرطان الثدي في أطلس جينوم السرطان (TCGA-BRCA)، يمكن لنموذج بقاء الرسم البياني الفائق الرقعة الذي يعتمد على التعبير الجيني المكاني كميزات للعقدة أن يحقق مؤشر اتساق متوسط (مؤشر C) يبلغ 0.747 في التحقق المتبادل 5 أضعاف؛ في مجموعة سرطان القولون والمستقيم في أطلس جينوم السرطان (TCGA-CRC)، كان لنموذج البقاء على قيد الحياة مؤشر C يبلغ 0.725 في التحقق المتبادل بخمسة أضعاف، وهو أفضل من النماذج التنبؤية الأخرى، كما هو موضح في الشكل أعلاه.
ويحافظ هذا النموذج التنبؤي للبقاء على قيد الحياة أيضًا على ميزة الدقة في التنبؤ بتشخيص المرضى في المرحلة المبكرة (المرحلة الأولى والثانية)، ويمكن استخدام درجة المخاطر المتوقعة كمؤشر تنبؤي مستقل للمرضى في جميع المراحل والمرضى في المرحلة المبكرة. في مجموعة الاختبار الخارجية MCO-CRC التي تحتوي على بيانات أكثر من ألف مريض، حافظ نموذج التنبؤ بالبقاء على قيد الحياة على ميزة مستقرة وكان لديه القدرة على التعميم.
سرطان الثدي وسرطان البنكرياس أولاً: الاستفادة من الذكاء الاصطناعي لتحسين التشخيص
أثناء تشخيص وعلاج السرطان، يمكن لتحليل تشخيص السرطان أن يتجنب بشكل فعال الإفراط في العلاج وإهدار الموارد الطبية، ويوفر أساسًا علميًا للطاقم الطبي وأسرهم لاتخاذ القرارات الطبية. لقد أصبح موضوعًا ساخنًا في أبحاث السرطان في السنوات الأخيرة.
لتحسين نتائج سرطان الثدي، تعاون باحثو Salesforce في عام 2020 مع الأطباء في معهد لورانس جيه إليسون بجامعة جنوب كاليفورنياتم إطلاق نظام التعلم الآلي ReceptorNet،تستطيع خوارزميتها التنبؤ بحالة مستقبلات الهرمونات من صور الأنسجة منخفضة التكلفة وسهلة الوصول إليها - وهي علامة حيوية مهمة للأطباء عند تحديد مسار العلاج المناسب لمرضى سرطان الثدي. وصلت دقة النظام إلى 92%.

في فبراير 2024، استخدم باحثون من جامعة كنتاكي وجامعة ماكاو للعلوم والتكنولوجيا وجامعة ماكاو والمستشفى التابع الأول لجامعة قوانغتشو الطبية نموذج الشبكة العصبية لـتم إنشاء نظام تسجيل دقيق للتنبؤ، MIRS (درجة المخاطر النقائلية والمناعة الجينية).يوفر قياس نقائل الورم والمخاطر الجينومية المناعية أداة تنبؤية يمكن تطبيقها عالميًا تقريبًا على مرضى سرطان الثدي وتوفر اتجاهًا جديدًا لخيارات العلاج لسكان سرطان الثدي. (انقر هنا للحصول على تقرير مفصل: بهدف مكافحة أكثر أنواع السرطان شيوعًا في العالم، أنشأ علماء صينيون نظام تسجيل تشخيص سرطان الثدي MIRS)
علاوة على ذلك، يعد سرطان البنكرياس أحد الأورام الخبيثة الشائعة في الجهاز الهضمي، ومعدل البقاء على قيد الحياة لمدة خمس سنوات بعد التشخيص لا يزيد عن 10%. إن الخطوة الأساسية في تحسين معدلات بقاء المرضى هي التنبؤ بدقة بالمخاطر التي قد يتعرض لها المريض من أجل تصميم خطط علاجية مستهدفة. الفحص النسيجي هو فحص روتيني في علم الأورام يمكنه تحليل خصائص الورم على المستوى المجهري وهو طريقة مهمة لتقييم خطر تطور الورم. ومع ذلك، بسبب الحجم الكبير للشرائح والتركيبة المعقدة للأنسجة، فإن نتائج التقييم تتأثر بسهولة بالعوامل الذاتية.

في عام 2023، قام فريق بحثي من جامعة نانجينغ لعلوم المعلومات والتكنولوجيا ومعهد الرعاية الصحية الذكية، كلية الذكاء الاصطناعي،نُشر بحث بعنوان "نموذج تقسيم الأنسجة المتعددة لصور سرطان البنكرياس المقطعية الكاملة استنادًا إلى تعدد المهام والانتباه"تمت دراسة تقسيم الأنسجة لـ 8 فئات من المقاطع المرضية لسرطان البنكرياس. ومن خلال تقديم آلية الاهتمام وتصميم هيكل متعدد المهام هرمي ومشترك، تم تحسين أداء النموذج بشكل كبير باستخدام المهام المساعدة ذات الصلة.
تم تدريب النموذج المقترح في هذه الدراسة واختباره على مجموعة بيانات مستشفى شنغهاي تشانجهاي وتم التحقق من صحته خارجيًا على مجموعة بيانات TCGA العامة. وكانت درجات F1 في مجموعة الاختبار الداخلية أعلى من 0.97، وكانت درجات F1 في مجموعة التحقق الخارجية أعلى من 0.92. وكان أداء التعميم أفضل بشكل ملحوظ من طريقة الأساس.
ومن الجدير التأكيد على أن الذكاء الاصطناعي لا يمكن أن يحل محل خبراء علم الأمراض، بل يعمل كتكنولوجيا تشخيصية مساعدة لتوفير المزيد من الراحة لتشخيص علم الأمراض وتحسين كفاءة عمل علماء الأمراض بشكل أكبر. ومن منظور طويل الأمد، لا يزال أمام الذكاء الاصطناعي مجال كبير للتطور في مجال الكشف عن المؤشرات الحيوية الرقمية، وتحليل الصور الطبية، والتنبؤ بمسار المرض، وغيرها من المجالات.
مراجع:
1.https://news.un.org/zh/story/2018/09/1017602
2.https://mp.weixin.qq.com/s/VE68FKL6kwpO1IFsbR-LVA
3.https://ins.sjtu.edu.cn/articles/286
4.https://www.cdstm.cn/theme/khsj/khzx/khcb/202012/t20201214_1039028.html