Command Palette
Search for a command to run...
Die Genauigkeit Der Frühdiagnose Der Parkinson-Krankheit Hat Sich Auf 90,2% erhöht. Das Shenzhen Institute of Advanced Technology Und Das Zhongshan First Hospital Haben Gemeinsam Das GSP-GCNs-Modell Vorgeschlagen

Ein Forschungsteam des First Affiliated Hospital der Sun Yat-sen University und des Institute of Advanced Technology des USTC hat ein Deep-Learning-Modell vorgeschlagen – Graph Signal Processing-Graph Convolutional Networks (GSP-GCNs), das ereignisbezogene EEG-Daten aus spezifischen Aufgaben der Tonregulierung zur Diagnose der Parkinson-Krankheit verwendet.
Zittern, langsame Bewegungen, steifer Gesichtsausdruck ... Wenn von der Parkinson-Krankheit die Rede ist, denken die meisten Menschen zuerst an „Handzittern“. Sie wissen jedoch nicht, dass die Patienten im mittleren und späten Stadium der Krankheit sogar Probleme wie Gleichgewichtsstörungen und Schwierigkeiten beim Umdrehen haben können. Ihre unteren Gliedmaßen und ihr Kopf zittern unwillkürlich, was ihre Lebensqualität ernsthaft beeinträchtigt.
Im April 2023 veröffentlichte Daten der Chinesischen Vereinigung für Rehabilitationsmedizin zeigen, dass es in meinem Land mehr als drei Millionen Parkinson-Patienten gibt, also mehr als ein Viertel der weltweiten Gesamtzahl, und dass jedes Jahr etwa 100.000 neue Fälle hinzukommen.Schätzungen zufolge wird die Gesamtzahl der Parkinson-Patienten in meinem Land bis 2030 fünf Millionen erreichen, also fast die Hälfte der weltweiten Patientenzahl.
Allerdings ist die Pathogenese der Parkinson-Krankheit noch immer unbekannt und nur 201 TP3T-Fälle können auf spezifische genetische Faktoren zurückgeführt werden, sodass eine frühzeitige Diagnose vor großen Herausforderungen steht.
Das Ruhe-Elektroenzephalogramm (EEG) hat sich zu einer wichtigen Methode zur Diagnose der Parkinson-Krankheit entwickelt, da es nichtinvasiv ist und die Gehirnaktivität mit hoher zeitlicher Auflösung erfassen kann. In den letzten Jahren wurde in einschlägigen Studien damit begonnen, Deep Learning mit EEG zur Frühdiagnose der Parkinson-Krankheit zu kombinieren. Allerdings erfordern die meisten dieser Methoden stabile EEG-Signale, um zu funktionieren, und können die dynamischen Merkmale der mit der Parkinson-Krankheit verbundenen Veränderungen der Gehirnaktivität nicht erfassen.
In Anbetracht dessenForscher der Shenzhen Institutes of Advanced Technology der Chinesischen Akademie der Wissenschaften und des First Affiliated Hospital der Sun Yat-sen-Universität haben ein interpretierbares Graph-Signal-Processing-Graph-Convolutional-Network-Modell (GSP-GCNs) vorgeschlagen, das abnormale EEG-Merkmale von Sprachmotoraufgaben bei der Parkinson-Krankheit verwendet.Mithilfe der EEG-Daten der Sprachgrundfrequenzmodulationsaufgabe und der Gewinnung neuronaler Marker des großflächigen funktionellen Gehirnnetzwerks von Parkinson-Patienten ist es uns gelungen, eine hochpräzise intelligente Diagnose der Parkinson-Krankheit zu erstellen.

Holen Sie sich das Papier:
https://www.nature.com/articles/s41746-023-00983-9
Antworten Sie im öffentlichen WeChat-Konto mit „Parkinson“, um das vollständige PDF zu erhalten
Datensatz: Vokalisationsexperiment mit 100 Teilnehmern
Das Forschungsteam lud 100 Teilnehmer ein, darunter 52 Personen mit der DiagnoseIdiopathische Parkinson-KrankheitPatienten (24 Frauen und 28 Männer) und 48 gesunde Kontrollpersonen gleichen Geschlechts und Alters.Alle Teilnehmer führten das Vokalisationsexperiment durch.
Während des Experiments mussten die Teilnehmer 5–6 Sekunden lang Vokale mit einer Dauer von 200 ms produzieren. Jede Äußerung besteht aus 4–5 Störungen.PseudozufälligAuf diese Weise präsentiert. Die Teilnehmer gaben in insgesamt 100 Versuchen 20–25-mal hintereinander Laute von sich.
Während die Teilnehmer das Vokalisationsexperiment durchführten, zeichneten die Forscher mithilfe der NetStation-Software EEG-Signale mit einer Abtastfrequenz von 1 kHz auf. Dabei verwendeten sie eine 64-adrige Elektrodenkappe, die an einen Net Amps 300-Verstärker (EGI) angeschlossen war.
GSP-GCNs-Modell: besteht aus 4 aufeinanderfolgenden Komponenten
Das GSP-GCNs-Modellframework besteht aus vier Modulen: Graphsignalverarbeitungsmodul (GSP), Graphnetzwerkmodul, Klassifikator und interpretierbares Modell.

* Zunächst analysiert und verarbeitet das GSP-Modul große EEG-Netzwerke, um dynamische Verbindungsmuster zu identifizieren.
* Zweitens erfasst das Graphnetzwerkmodul diese Konnektivitätsmuster als Schlüsselmerkmale für die Klassifizierung; * Anschließend nutzt die Klassifikatorkomponente diese extrahierten Merkmale, um Parkinson-Patienten von gesunden Personen zu unterscheiden; * Schließlich verbessert das Interpretierbarkeitsmodell die Interpretierbarkeit des Frameworks, indem es eine globale Visualisierung der erlernten wesentlichen Merkmale bereitstellt und diese mit sprachbezogenen mikromorphen EEG-Merkmalen abgleicht.
Durch die Übernahme dieses innovativen Ansatzes zielt das GSP-GCNs-Framework darauf ab, erklärende Informationen bereitzustellen, um die Verwendung von Deep-Learning-Modellen bei der Diagnose der Parkinson-Krankheit mit aufgabenbezogenen EEG-Daten zu erleichtern.
Modelleffekt: gute Interpretierbarkeit
Die Studie schlug vier auf Graphennetzwerken basierende Modelle vor: PCC + GCN, PLV + GCN, PCC + GSP-GCN und PLV + GSP-GCN.
Darunter stellen PCC (Pearson-Korrelationskoeffizient) und PLV (Phase Locking Value) verschiedene Merkmale dar, die zum Aufbau von Gehirnnetzwerken verwendet werden. Unabhängig vom FeaturetypDie GSP-GCNs-Modelle zeigen alle eine deutlich bessere Leistung als die GCNs-Modelle.
Wie in der folgenden Abbildung gezeigt, bleiben die ROC-Werte des vom Institut vorgeschlagenen GSP-GCN-Modells unter 0,08. Dies unterstreicht das Potenzial von GSP, die Klassifizierungsleistung zu verbessern, indem lokale und globale Informationen in Single-Hop- und Multi-Hop-Netzwerken durch Graphaggregation ausgeglichen werden.

Durch die Kombination lokaler und globaler InformationenDas in dieser Studie vorgeschlagene GSP-GCNs-Modell weist eine durchschnittliche Klassifizierungsgenauigkeit von 90,2% zur Unterscheidung von Parkinson-Patienten von normalen Kontrollpersonen auf, die mit 9,5% deutlich höher ist als bei anderen Deep-Learning-Modellen.Darüber hinaus weist das GCNs-Modell eine geringere Rechenkomplexität auf als alle Basismodelle.

Vergleich von Klassifizierungsleistung und Rechenkomplexität
Darüber hinaus analysierte das Forschungsteam die Interpretierbarkeit des GSP-GCNs-Modells und enthüllte seine Lernergebnisse hinsichtlich der Differenzverteilung zwischen großflächigen EEG-Netzwerken und MS5-Mikrozustands-EEG-Topographiekarten. Bei der Aufgabe zur Regulierung der Grundfrequenz der Sprache liegen die Gehirnbereiche mit signifikanten Unterschieden zwischen Parkinson-Patienten und normalen Kontrollpersonen hauptsächlich im linken ventralen prämotorischen Kortex, im oberen Temporallappen und im Broca-Areal. Dies steht in hohem Maße im Einklang mit dem Gehirnnetzwerk der zuvor entdeckten Sprachbewegungsstörungen bei der Parkinson-Krankheit.
Dies zeigt, dassDas in dieser Studie vorgeschlagene GSP-GCN-Modell kann einzigartige EEG-Biomarker aus großen Netzwerken identifizieren und bietet eine gute Interpretierbarkeit.
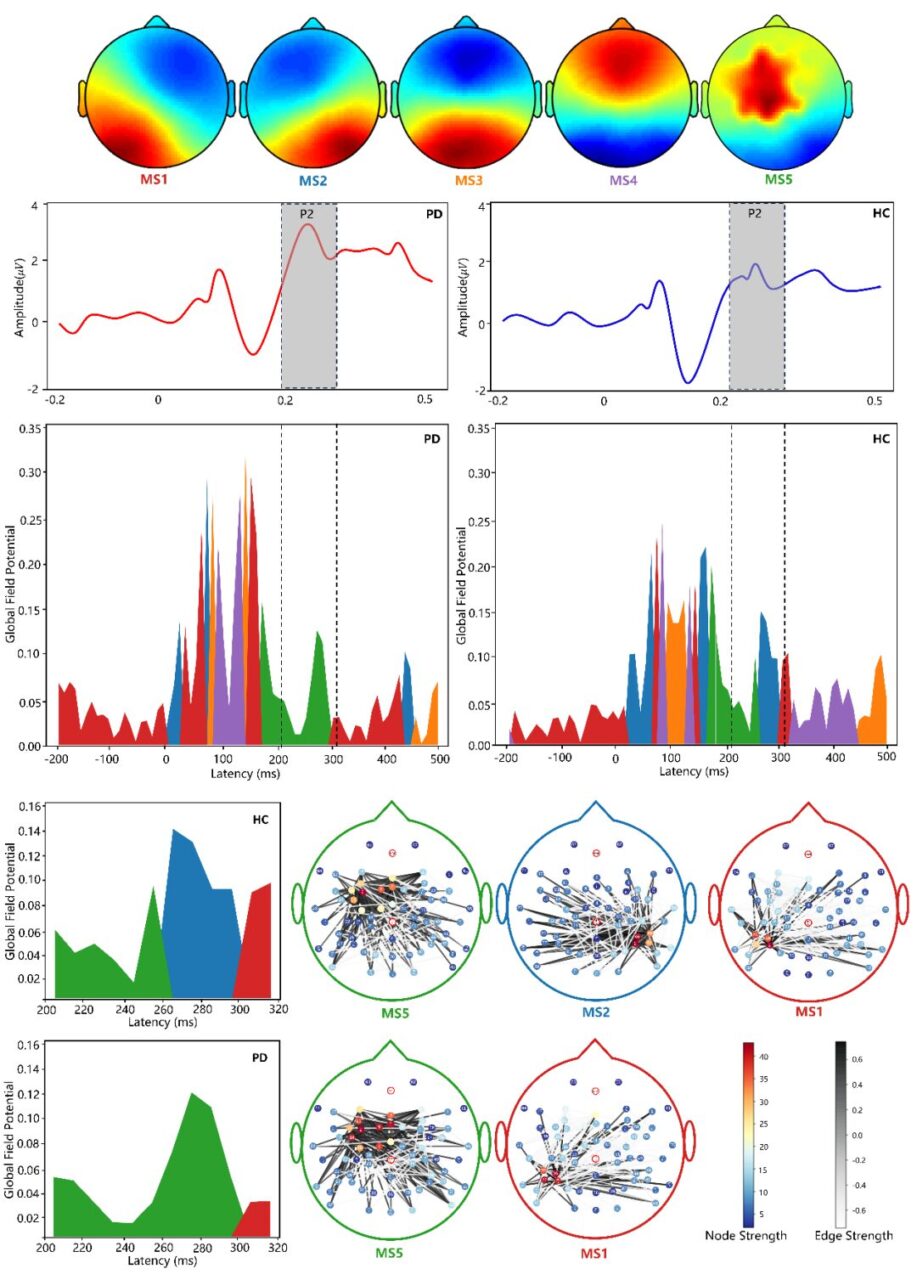
Vergleich der ERP-Mikrozustandsverteilung
(PD in der oberen rechten Ecke ist die Parkinson-Krankheitsgruppe und HC ist die normale Kontrollgruppe)
Noch wichtiger ist, dass das Modell die Unterschiede zwischen den funktionellen Netzwerken des Gehirns von Parkinson-Patienten und normalen Kontrollpersonen bei Aufgaben mit auditiver Rückmeldung effektiv erlernen kann und so eine neue Methode zur Analyse der Interpretierbarkeit von Deep-Learning-Modellen bietet, die zur Diagnose und Klassifizierung von Krankheiten eingesetzt werden.
KI identifiziert Biomarker zur Diagnose der Parkinson-Krankheit
Ausbruch der Parkinson-KrankheitDie Krankheit verläuft versteckt und schreitet langsam voran. Daher sind eine frühzeitige Diagnose und ein rechtzeitiges Eingreifen äußerst wichtig, um die Wirksamkeit zu verbessern. Ein wichtiger Ansatz zur Frühdiagnose der Parkinson-Krankheit ist die Identifizierung von Biomarkern in verschiedenen Verhaltensbereichen, darunter Handschriftmuster, motorische Funktionen, Gangmuster und Sprachmerkmale.
Maschinelles Lernen hat sich in den letzten Jahren als leistungsstarkes Werkzeug im Bereich der medizinischen Bildgebung herausgestellt und hilft dabei, hochrangige Merkmale und Muster aus komplexen neurologischen Bildgebungsdaten zu extrahieren. Darüber hinaus kann maschinelles Lernen aufgrund seiner hervorragenden multidimensionalen Analysefähigkeiten auch zur individuellen Klassifizierung im Bereich der medizinischen Bildgebung eingesetzt werden. Das vom gemeinsamen Forschungsteam des der Zhongshan-Universität angeschlossenen Zhongshan-Krankenhauses vorgeschlagene GSP-GCNs-Modell ermöglicht die Diagnose durch die Ermittlung sprachbezogener neuronaler Marker von Parkinson-Patienten. Bei der Anwendung von KI-Deep-Learning-Modellen zur Identifizierung verschiedener Verhaltensbereiche der Parkinson-Krankheit besteht noch erheblicher Entwicklungsbedarf.
Ähnlich,Ein Forschungsteam des Union Hospital der Fujian Medical University hat kürzlich ein maschinelles Lernmodell entwickelt, um das Risiko des Einfrierens des Gangs bei Parkinson-Patienten auf individueller Ebene vorherzusagen.Mithilfe des Geräts können Parkinson-Patienten frühzeitig identifiziert werden, bei denen die Wahrscheinlichkeit einer verzögerten Gangstarre besteht. Dadurch erhalten Klinikärzte wertvolle Hinweise, wie sie Symptome einer Gangstarre bei Parkinson-Patienten verhindern und behandeln können.
Auch,Das Forschungsteam des University College London (UCL) trainierte einen KI-Algorithmus mithilfe von Videodaten von 300 Parkinson-Patienten und 300 gesunden Freiwilligen.Es ermöglicht die Identifizierung der Bewegungsmuster von Parkinson-Patienten mit einer Genauigkeitsrate von bis zu 90% bei der Diagnose der Parkinson-Krankheit.
Wir gehen davon aus, dass maschinelles Lernen und KI auf der Grundlage der Neurobildgebung künftig noch stärker eingesetzt werden können, um Menschen dabei zu helfen, Biomarker in verschiedenen Verhaltensbereichen, die mit den Symptomen der Parkinson-Krankheit in Zusammenhang stehen, effektiv zu identifizieren und so die Weiterentwicklung der Frühdiagnose der Parkinson-Krankheit zu fördern.