Command Palette
Search for a command to run...
نجح فريق فرنسي في التنبؤ بـ 2.39 مليون بروتين مضاد للفيروسات واستخدم نموذج التعلم العميق لرسم خريطة المناعة المضادة للفيروسات البكتيرية.

في عالم الميكروسكوب، لم تتوقف "سباق التسلح" بين البكتيريا والفيروسات العاثية. عادةً ما يفوق عدد الفيروسات العاثية عدد البكتيريا بنحو عشرة أضعاف، مستخدمةً البكتيريا كحاضنات لتكاثرها. في الوقت نفسه، طورت البكتيريا أنظمة دفاعية مضادة للفيروسات شديدة التنوع عبر تطور طويل الأمد. حاليًا، تم التحقق تجريبيًا من أكثر من 250 نظامًا مضادًا للفيروسات العاثية، تشمل آليات متنوعة مثل أنظمة التقييد والتعديل وأنظمة كريسبر-كاس، ويجري اكتشاف أنظمة جديدة باستمرار. تشير هذه الظاهرة إلى أن تعقيد وتنوع أنظمة الدفاع البكتيرية قد يتجاوز بكثير الفهم الحالي. ومع ذلك،بسبب محدودية الأساليب التجريبية التقليدية والتقنيات الحسابية، لا يزال عدد كبير من الآليات المحتملة المضادة للفيروسات مخفيًا في الجينوم البكتيري ولم يتم استكشافها بشكل منهجي حتى الآن.
أشارت الأبحاث الحالية إلى وجود خصائص مشتركة معينة بين أنظمة مضادات العاثيات المعروفة على مستوى تسلسل البروتين وتنظيم الجينوم، مثل تكرار المجالات المميزة وتوزيعها الغني في "جزر الدفاع" أو مناطق ما قبل العاثية. تشير هذه الأنماط إلى ما يلي:إذا أمكن تحديد هذه الأنماط الشائعة واستخدامها، فقد يكون من الممكن الكشف بشكل منهجي عن أنظمة مضادة للفيروسات غير معروفة على نطاق الجينوم بأكمله.
استنادًا إلى هذا النهج، طوّر باحثون في معهد باستور بفرنسا ثلاثة نماذج تعلّم عميق متكاملة، وقاموا بضبطها بدقة، للتنبؤ واسع النطاق بمقاومة العاثيات. يعتمد نموذج ALBERT_DF كليًا على السياق الجينومي المحلي للاستدلال؛ بينما يستخدم نموذج ESM_DF نموذج لغة البروتين لتحليل تسلسلات الأحماض الأمينية؛ أما نموذج GeneCLR_DF فيدمج معلومات التسلسل مع السياق الجينومي. في اختبار معياري موحد،حقق GeneCLR_DF أفضل أداء، حيث بلغ دقة 991 TP3T واستدعاء 921 TP3T.
استنادًا إلى هذا النموذج عالي الدقة، أجرت الدراسة تنبؤات شاملة على مستوى الجينوم لأنظمة مقاومة الفيروسات. وأظهرت النتائج أن ما يقرب من 1.51 جينًا من جينات TP3T في أكثر من 32000 جينوم بكتيري نموذجي تشارك في الدفاع المضاد للفيروسات؛ والأهم من ذلك، أن أكثر من 851 جينًا من جينات TP3T، التي تمثل عائلة بروتينية متوقعة مرتبطة بالدفاع، لم يسبق ربطها بوظيفة المناعة. في نهاية المطاف،وتوقع النموذج ما يقرب من 2.39 مليون بروتين مضاد للفيروسات، ينتمي عدد كبير منها إلى أنظمة دفاعية أحادية الجين، وحدد ما يقرب من 23000 عائلة من الأوبيرون بناءً على علاقات التواجد المشترك للجينات.لم تكن الغالبية العظمى من هذه البكتيريا مرتبطة سابقًا بالدفاع المضاد للفيروسات. وتُقدّم هذه النتائج مجتمعةً صورةً منهجيةً للمناعة البكتيرية المضادة للفيروسات، كاشفةً عن نطاقها وتنوعها الذي يتجاوز بكثير المعرفة الحالية.
وقد نُشرت نتائج البحث ذات الصلة، بعنوان "نماذج اللغة البروتينية والجينومية تكشف عن التنوع غير المستكشف للمناعة البكتيرية"، في مجلة ساينس.
أبرز الأبحاث:
* تم التنبؤ بما مجموعه 2.39 مليون بروتين مضاد للفيروسات، منها 85% لم يتم ربطها بوظيفة المناعة من قبل؛
* في الجينوم البكتيري النموذجي، يكون ما يقرب من 1.51 جين TP3T مسؤولاً بشكل خاص عن الدفاع المضاد للفيروسات.
* تم التنبؤ بوجود ما يقرب من 23000 عائلة فرعية من عائلات المعالجات، وقد تم اكتشاف الغالبية العظمى منها لأول مرة؛
* يوجد عدد كبير من البروتينات الدفاعية المتوقعة في شكل أنظمة جينية مفردة، مما يتحدى النظرة التقليدية القائلة بأن الوظائف الدفاعية عادة ما يتم إنجازها من خلال تعاون جينات متعددة.

عنوان الورقة:
https://www.science.org/doi/10.1126/science.adv8275
تابع حسابنا الرسمي على WeChat وأجب بكلمة "GeneCLR" في الخلفية للحصول على ملف PDF كامل.
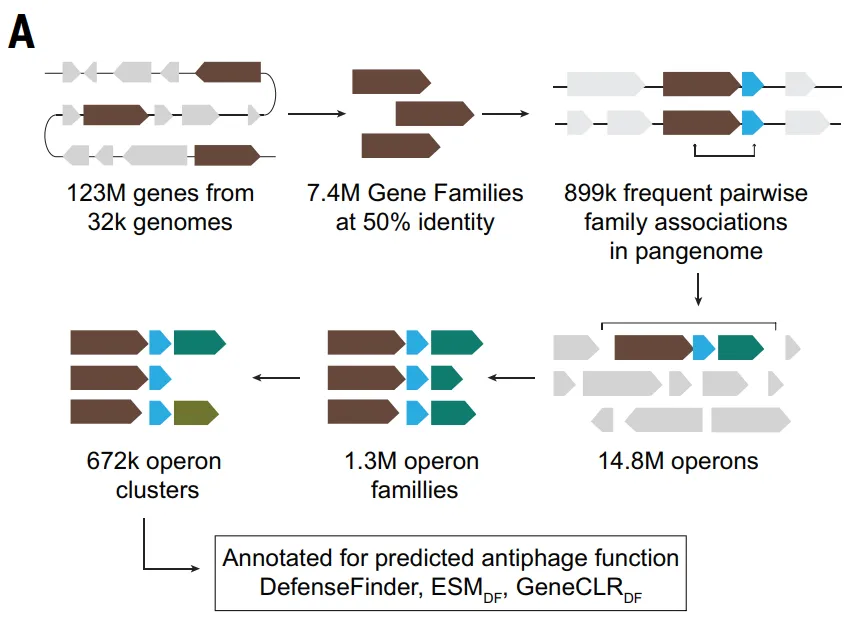
مجموعة البيانات: تستند إلى 123 مليون بروتين و32000 جينوم
استخدمت هذه الدراسة في البداية أدوات DefenseFinder و PadLoc،تم إجراء مسح منهجي لـ 32798 جينوم بكتيري كامل في قاعدة بيانات RefSeq لتوصيف أنظمة مضادات العاثيات المعروفة كمياً.من بين ما يقرب من 123 مليون بروتين، حدد DefenseFinder v1.3 521360، وهو ما يمثل 0.41 TP3T، والتي تنتمي إلى مكونات نظام مضاد العاثيات، بينما حدد PadLoc 805357، وهو ما يمثل 0.651 TP3T.
تجدر الإشارة إلى أن العديد من أنظمة الدفاع اكتُشفت في البداية من خلال ارتباطات جينومية مع أنظمة معروفة. ويمكن قياس هذه الارتباطات على مستوى عائلة البروتينات باستخدام "مؤشر الدفاع"، الذي يقيس مدى تكرار وجود عائلة بروتينية معينة مع بروتينات دفاعية معروفة في الجينوم.
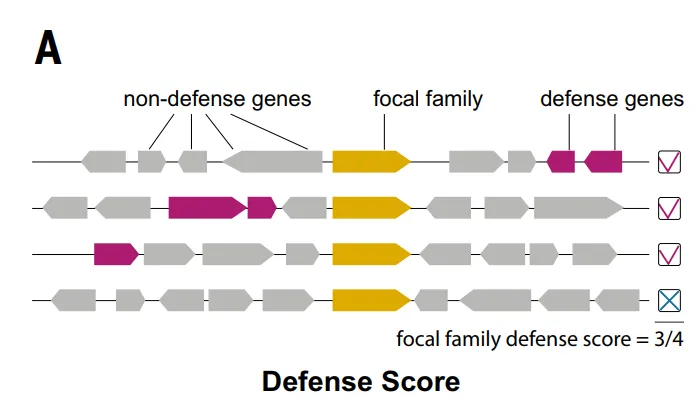
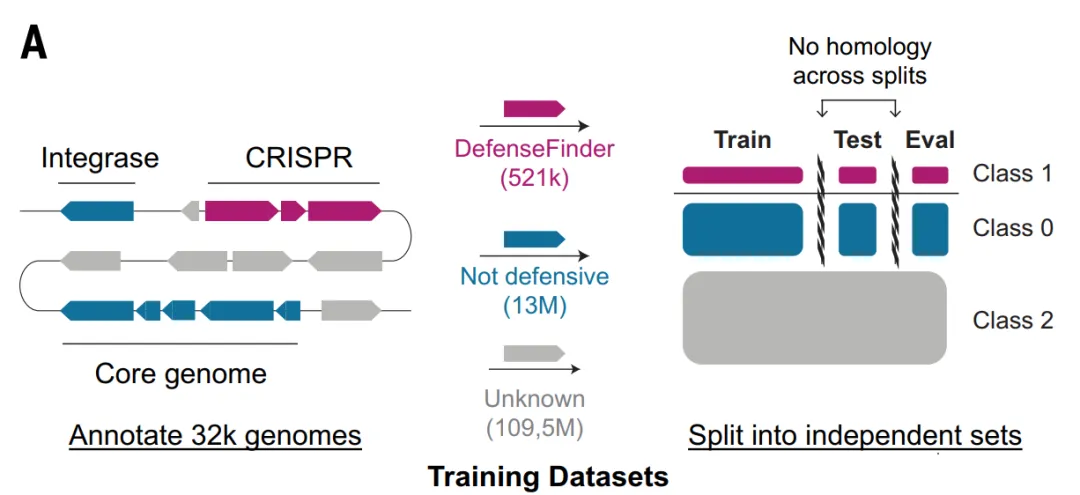
استنادًا إلى طريقة تسجيل نقاط الدفاع، كما هو موضح في الشكل أدناه.حدد الباحثون ما مجموعه 37959 عائلة بروتينية (4.61٪ من TP3T) كعائلات مرشحة مضادة للفيروسات.وفي وقت لاحق، استبعدت الدراسة 7799 عائلة، مثل الإنزيمات المدمجة، التي كانت مرتبطة بالوظائف البيولوجية الأساسية أو العناصر الجينية المتنقلة، مما أدى في النهاية إلى اختيار 30160 عائلة مرشحة (تمثل 3.71 TP3T).
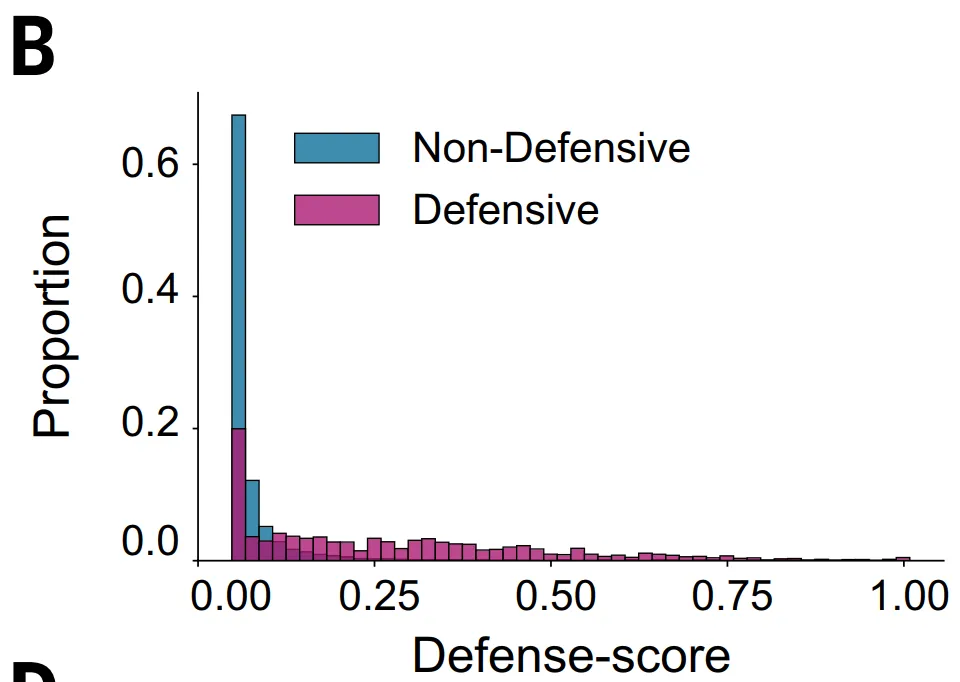
لكن هذه الطريقة لها قيود واضحة:أولاً،ينطبق هذا فقط على عائلات البروتينات التي تحتوي على أكثر من خمسة تسلسلات متماثلة، وبالتالي يستثني البروتينات التي يبلغ عددها حوالي 23%؛ثانيًا،بعض أنظمة مكافحة العاثيات لا تقع في جزر الدفاع النموذجية، وحتى لو كانت لها وظائف دفاعية، فقد تكون درجات دفاعها منخفضة، مما يؤدي إلى تجاهلها.
للتغلب على القيود المذكورة أعلاه والتقاط الإشارات الجينومية المتعلقة بالدفاع بشكل أكثر شمولاً،وقد قامت الدراسة أيضاً بإنشاء مجموعة بيانات مناسبة للتعلم العميق.في إطار نموذج ALBERT_DF، قامت الدراسة بنمذجة الجينوم البكتيري بطريقة "لغوية": حيث تعاملت مع كل عائلة بروتينية على أنها "كلمة" ومع أجزاء الجينات المجاورة على أنها "جملة".
لأن مجموعة البيانات الكاملة تحتوي على أكثر من 8 ملايين عائلة بروتينية مختلفة، وهو ما يتجاوز بكثير حجم مفردات نماذج اللغة التقليدية،وقد اقتصرت الدراسة على نطاق التدريب لشعبة الأكتينوبكتيريا، حيث تم إنشاء مجموعة بيانات تحتوي على 10796 جينومًا.تم تجميع الجينات في 4.2 مليون عائلة بروتينية، بينما اقتصرت المفردات على 524288 عائلة الأكثر شيوعًا، وبالتالي تغطي ما يقرب من 891 بروتين TP3T.
بالنسبة لنموذجي ESM_DF و GeneCLR_DF، قامت الدراسة بإنشاء مجموعة بيانات Gembase_DF: كما هو موضح في الشكل أدناه، تم استخدام 521360 بروتين مضاد للفيروسات تم وضع علامة عليه باستخدام DefenseFinder كعينات إيجابية، وتم استخدام 116 مليون جين أساسي محفوظ للغاية موجود في أكثر من 99% و 14 مليون جين عنصر وراثي متنقل غير دفاعي كعينات سلبية، وتم الاحتفاظ بالبروتينات المتبقية كمرشحين غير موسومين.
ولتجنب تسرب المعلومات بين التدريب والتحقق والاختبار، قامت الدراسة بتجميع جميع البروتينات الخاصة بنظام الدفاع نفسه في نفس طية البيانات واستخدمت MMseqs2 لإزالة التشابه المتبقي عبر طيات البيانات، مما يضمن دقة تقييم النموذج.
بنية النموذج: نموذج تعلم عميق ثلاثي الطبقات يتقدم خطوة بخطوة.
للتغلب على قيود أساليب "درجة الدفاع" التقليدية، قام فريق البحث ببناء إطار عمل للتعلم العميق تكميلي وتدريجي، يستهدف ثلاثة أهداف: اكتشاف الأنظمة غير المعروفة، والتنقيب على نطاق الجينوم الشامل، والتنبؤ المتكامل عالي الدقة.على وجه التحديد، يشمل ذلك ALBERT_DF المستند إلى السياق الجينومي، وESM_DF المستند إلى تسلسل البروتين، وGeneCLR_DF الذي يدمج معلومات التسلسل والسياق.
ومن بينها، يركز ALBERT_DF على تعلم الإشارات الوظيفية من "علاقات الجوار" الجينية ولديه القدرة على اكتشاف أنظمة دفاعية جديدة؛ يستخدم ESM_DF نمذجة تسلسل الأحماض الأمينية بشكل مباشر ولديه قدرة جيدة على التعميم عبر التسلسل؛ بينما يدمج GeneCLR_DF النوعين من المعلومات في إطار موحد ويحقق توازنًا أفضل بين دقة التعرف وتغطية التنبؤ.
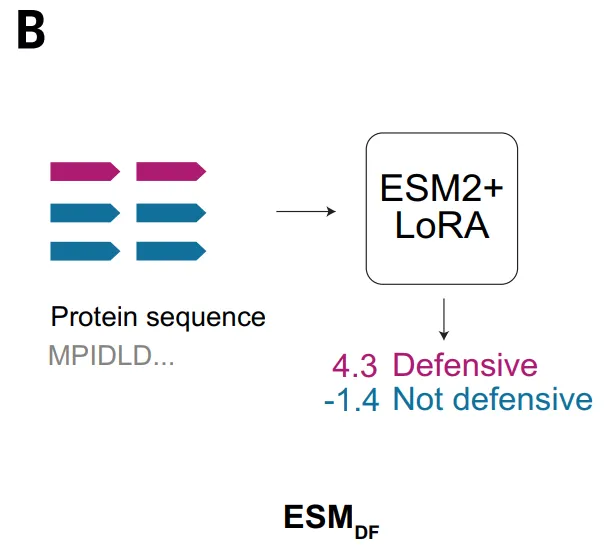
يعتمد نموذج ALBERT_DF على ملاحظة أساسية: تميل أنظمة الفيروسات المضادة إلى التجمع في الجينوم، مع وجود أنماط تنظيمية مستقرة داخل الجينات المتجاورة وفيما بينها. بناءً على هذه الخاصية،تُقدّم هذه الدراسة بنية ALBERT من معالجة اللغة الطبيعية إلى نمذجة الجينوم.من خلال التعامل مع عائلات البروتينات على أنها "كلمات" وتسلسلات الجينات على أنها "هياكل نحوية"، نتعلم السياق المحلي من خلال التنبؤ بالجينات المقنعة.
بخلاف الطرق التقليدية القائمة على تشابه التسلسل، تستخدم هذه الطريقة في النمذجة معلومات التنظيم الجينومي مباشرةً، مما يمنحها إمكانات أكبر لتحديد آليات دفاعية جديدة تفتقر إلى التشابه مع الأنظمة المعروفة. مع ذلك، ونظرًا لاعتمادها على تمثيلات "معجمية" منفصلة، فإن هذا النوع من الطرق له قيود متأصلة عند تطبيقه على أنواع مختلفة.
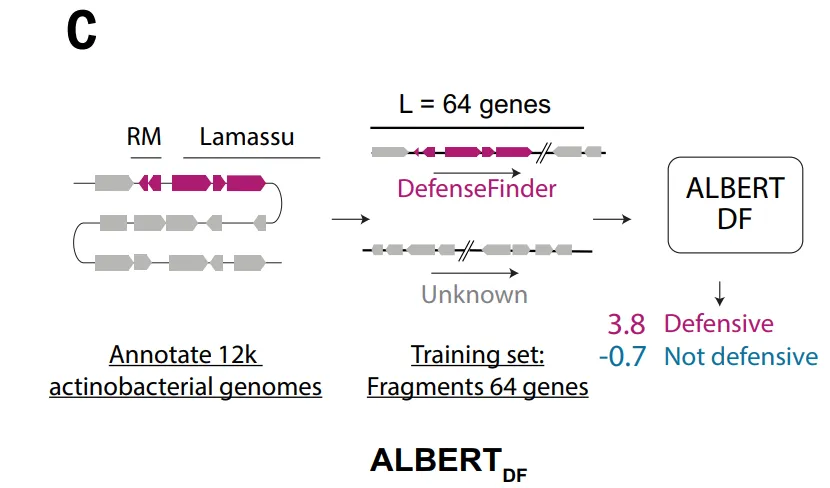
أما نموذج ESM_DF، من ناحية أخرى، فيتبع نهجاً مختلفاً، حيث يعمل مباشرة على تسلسل الأحماض الأمينية للبروتين.يتعلم هذا النموذج التغيرات المشتركة بين البقايا وعلاقات التسلسل بعيدة المدى من خلال التدريب المسبق واسع النطاق.يُتيح هذا استخلاص الإشارات الوظيفية دون الاعتماد على خصائص اصطناعية. بعد الضبط الدقيق، يُمكن لـ ESM_DF تقييم أي بروتين لتحديد ما إذا كان يُشارك في الدفاع ضد العاثيات. يُحسّن هذا النهج بشكلٍ كبير من قابلية تطبيق الطريقة، مما يُتيح لها العمل على نطاق الجينوم الكامل. مع ذلك، في الوقت نفسه، لا تزال قدرة ESM_DF على التمييز تعتمد إلى حدٍ ما على تشابه التسلسل، وبالتالي فهي أفضل في تحديد المتغيرات البعيدة لأنظمة الدفاع المعروفة، وقدرتها على تحديد المجالات الجديدة التي تفتقر إلى التشابه محدودة نسبيًا.
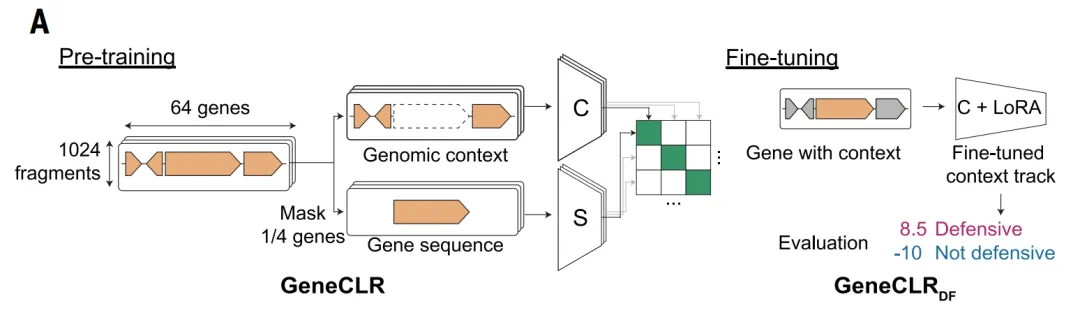
وبناءً على ذلك، تم اقتراح نموذج GeneCLR_DF لدمج معلومات التسلسل والسياق الجينومي.يستخدم هذا النموذج إطار عمل للتعلم التبايني، حيث يتعلم في الوقت نفسه تمثيلين لكل جين:يُستمد أحد نوعي التمثيل من تسلسل البروتين، والآخر من محيطه الجينومي. ومن خلال تدريب النموذج، يتم تحديد ما إذا كان هذان التمثيلان يتطابقان مع الجين نفسه، وبالتالي يتم مواءمة نوعي المعلومات في فضاء التمثيل.
يُقدّم هذا التصميم ميزةً رئيسية: فعندما تفتقر بعض الجينات إلى التماثل على مستوى التسلسل، يُمكن أن يُوفّر سياقها الجينومي النموذجي أدلةً على تحديدها؛ وعلى العكس من ذلك، عندما تكون المعلومات السياقية غير نمطية، يُمكن أن تُساعد خصائص التسلسل في التمييز بينها. ومن خلال هذه الآلية التكميلية،يوازن برنامج GeneCLR بين القدرة على اكتشاف أنظمة جديدة وقابلية التوسع للتطبيقات واسعة النطاق في التنبؤات اللاحقة.
بشكل عام، تُشكّل هذه الأنواع الثلاثة من النماذج مسارًا تقنيًا واضحًا: من تعلّم الأنماط المحلية القائم على السياق إلى التعميم العالمي القائم على التسلسل، ثم إلى النمذجة الموحدة للمعلومات متعددة المصادر. لا يقتصر هذا التصميم الهرمي على تجنّب قيود الطريقة الواحدة فحسب، بل يُوفّر أيضًا إطارًا تقنيًا أكثر شمولية لاستكشاف آليات الفيروسات المضادة غير المعروفة بشكل منهجي.
حقق دقة 991 TP3T واستدعاء 921 TP3T.
في التحقق التجريبي، قامت الدراسة أولاً بتقييم القدرة التنبؤية لـ ALBERT_DF.توقع النموذج ما مجموعه 1930 عائلة بروتينية مضادة للفيروسات المرشحة، والتي تداخلت منها حوالي 331 عائلة من TP3T مع نتائج طريقة درجة الدفاع.قام الباحثون باختيار عشرة أنظمة مرشحة تفتقر إلى كلٍ من دعم نقاط الدفاع والتماثل المعروف، وعبروا عنها في بكتيريا *Streptomyces whiteus*، ثم عرضوها لاثني عشر عاثية. أظهرت ستة من هذه الأنظمة حماية قوية، حيث خفضت وحدات تكوين اللويحات بأكثر من مئة ضعف. تحتوي هذه الأنظمة (مثل Ceres وGeb) على إنزيمات أيضية وبروتينات صغيرة ذات وظائف غير معروفة، متجاوزةً نطاق مجالات الدفاع التقليدية، مما يدل على أن الأساليب القائمة على السياق الجينومي قادرة على اكتشاف آليات دفاعية جديدة يصعب تحديدها باستخدام الأساليب التقليدية.
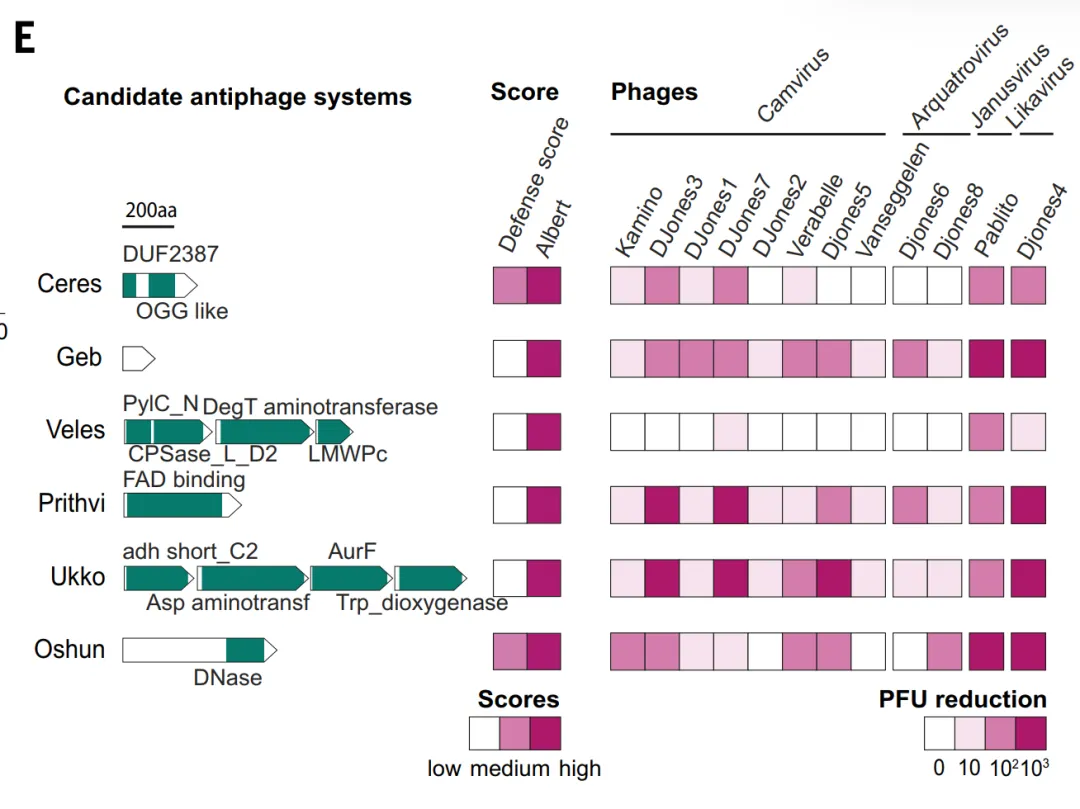
في إطار التحقق من صحة نظام ESM_DF، اختبرت الدراسة مجموعة من الأنظمة المرشحة ذات الأداء العالي في بكتيريا الإشريكية القولونية، حيث أظهرت ستة منها قدرات مضادة للفيروسات، بما في ذلك نظام ESM_DF المقاوم لأنواع متعددة من العاثيات. وشملت هذه الأنظمة متغيرات من نطاقات دفاعية معروفة، بالإضافة إلى نطاقات لم يسبق ربطها بوظيفة مضادة للفيروسات، مثل DUF7946.يشير هذا إلى أن ESM لا يعتمد فقط على تشابه التسلسل، بل يمكنه أيضًا تحديد نطاق أوسع من السمات الوظيفية، ولكنه بشكل عام لا يزال يميل إلى أن يكون امتدادًا للأنظمة المعروفة.
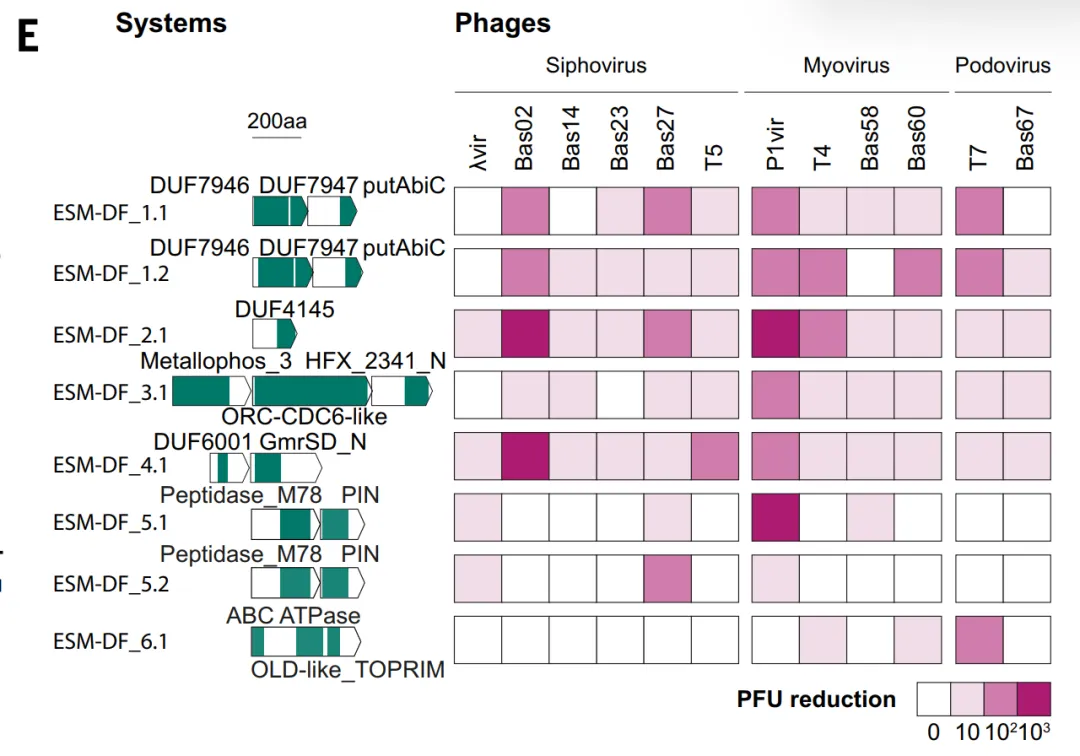
أظهر برنامج GeneCLR_DF أفضل أداء في تقييم النظام. على مجموعة الاختبار،تستطيع نتائج التنبؤ الخاصة به التمييز بوضوح بين البروتينات الدفاعية وغير الدفاعية.في التحليل التطوري، قام البرنامج باستمرار بتعيين درجات عالية لفروع الدفاع الرئيسية مثل النسخ العكسي، وCBASS، وThoeris، في حين أن ESM-650M_DF لم يتمكن إلا من تحديدها جزئيًا.
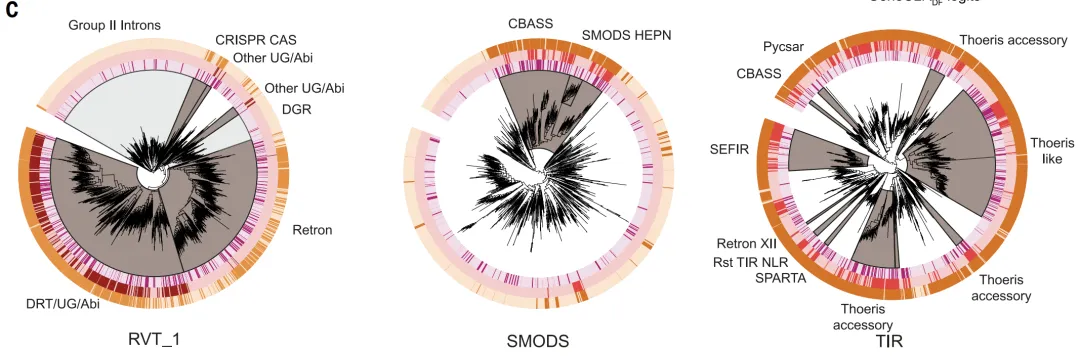
في سياقات جينومية مختلفة (جزر الدفاع، والإنترونات، ومناطق ما قبل العاثيات)،يستطيع برنامج GeneCLR_DF تحديد موقع وحدة الدفاع بدقة.أظهرت النتائج الكمية أنه عند عتبة -0.74، حقق برنامج GeneCLR_DF دقة بلغت 991 TP3T واستدعاءً بلغ 92.41 TP3T؛ بينما عند نفس الدقة، استدعى برنامج ESM_DF 581 TP3T فقط. وبمعدل اكتشاف خاطئ بلغ 11 TP3T، استرجع برنامج GeneCLR_DF 941 TP3T في عائلات دفاعية معروفة، وهو أعلى بكثير من برنامج ESM-650MDF (351 TP3T) وطريقة جزء الدفاع (51 TP3T)، وحدد 561 عائلة TP3T فقط؛ كما استعاد 751 TP3T من 110 أنظمة مضافة حديثًا. ومن بين 615,672 عائلة بروتينية مرشحة، تم الكشف عن 931 TP3T بواسطة برنامج GeneCLR_DF فقط.
على مستوى الأوبيرون، كشف تحليل إضافي قائم على التجميع الخطي أن عددًا كبيرًا من هياكل الدفاع لا يزال مجهولًا: فقد تم تحديد عائلة البروتين المتوقعة 85% فقط بواسطة ESM_DF وGeneCLR_DF، بينما كانت عائلة الأوبيرون 45% ومجموعة الأوبيرون 52.7% تفتقران سابقًا إلى الشروح الوظيفية. كما كشف التحليل التطوري أن...ارتفع متوسط نسبة جينات الدفاع في الجينوم البكتيري من 0.46% إلى 1.53%.علاوة على ذلك، فإن عددًا كبيرًا من الأنظمة غني بالعناصر الجينية المتنقلة، حيث يقع 23.5% داخل حدود MGE، ومن المتوقع أن تقوم العناصر الفرعية لـ 47.1% بتشفير القدرات الدفاعية.
على مستوى التنوع الجزيئي، وسّع برنامج GeneCLR_DF عدد عائلات Pfam المرتبطة بالدفاع من 934 إلى 3154 (ما يقارب 15% من إجمالي عائلات Pfam). في الوقت نفسه، افتقرت أكثر من 400,000 عائلة بروتينية متوقعة إلى أي بيانات تعريفية من Pfam، مع ظهور أقل من 5% في DefenseFinder؛ وتألفت أكثر من 3500 عائلة أوبيرون بالكامل من بروتينات بدون نطاقات معروفة. تشير هذه النتائج إلى أن...لم يتم بعد توصيف جزء كبير من الفضاء الجزيئي للدفاع ضد الفيروسات بشكل منهجي.
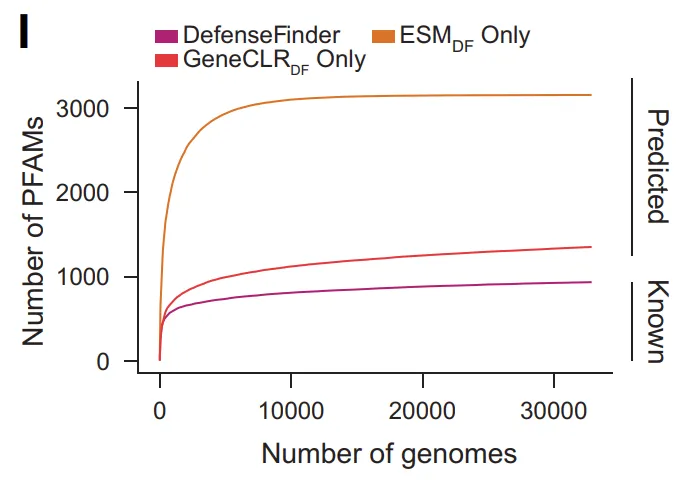
التعلم العميق يقود إلى قفزة نوعية في كفاءة اكتشاف الدفاعات المضادة للفيروسات.
تُتيح أُطر التنبؤ بأنظمة مضادات العاثيات القائمة على التعلم العميق، وأطالس المناعة المضادة للفيروسات البكتيرية المُستمدة منها، مسارًا بحثيًا أكثر قابلية للتوسع في هذا المجال، إذ ينتقل من "الاكتشافات الفردية" القائمة على حالات مُحددة إلى "التنقيب المنهجي" القائم على التعرف على الأنماط. ولا يُحسّن هذا التغيير كفاءة اكتشاف آليات دفاعية جديدة فحسب، بل يُقرّب أيضًا بين البحث الأكاديمي والتطبيقات الصناعية.
في الأوساط الأكاديمية، توسع هذا النهج بسرعة. فقد بدأت العديد من المؤسسات البحثية في دمج التعلم الآلي مع التحليل الجينومي في محاولة لتحديد الأنظمة المقاومة للفيروسات على نطاق أوسع. على سبيل المثال،نموذج التنبؤ بالدفاع، الذي طوره فريق في معهد ماساتشوستس للتكنولوجيا،بالاعتماد على منطق نمذجة نماذج لغة البروتين ودمج معلومات تسلسل الجينات والسياق الجينومي، تم التوصل إلى تحديد دقيق للغاية لبروتينات مضادات العاثيات. تم تدريب النموذج على ما يقارب 17000 جينوم مرجعي بدائيات النوى، وحدد ما يقارب 821 نظام دفاعي جديد من نوع TP3T في اختبارات مستقلة، مما يؤكد جدوى "الاكتشاف القائم على الأنماط للوظائف غير المعروفة".
عنوان الورقة البحثية: DefensePredictor: نموذج تعلم آلي لاكتشاف أنظمة المناعة في بدائيات النوى
رابط الورقة:
https://www.science.org/doi/10.1126/science.adv7924
في هذا القطاع، تُطبَّق التقنيات ذات الصلة بوتيرة متسارعة. ومع تفاقم مقاومة المضادات الحيوية، تستعيد العاثيات البكتيرية وتقنياتها المشتقة أهميتها، لتصبح اتجاهًا حاسمًا لاستبدال المضادات الحيوية التقليدية أو دعمها. وقد طورت شركة لوكاس للعلوم الحيوية، وهي شركة في مرحلة التجارب السريرية، منصةً تعتمد على العاثيات البكتيرية المُهندسة، تجمع بين التعلم الآلي وعلم الأحياء التركيبي، لتطوير LBP-EC01، وهو علاج مرشح لبكتيريا الإشريكية القولونية المقاومة للأدوية المتعددة، مما يُحسِّن دقة العلاج بالعاثيات وقابليته للتحكم.
في الوقت نفسه، تتبنى شركة ميكريوس نهجًا أكثر تركيزًا على التطبيقات، حيث تركز على تصنيع العاثيات البكتيرية والإندوسومالينات على نطاق صناعي. وقد استُخدم منتجها "ليستكس" في معالجة الأغذية لمنع تلوث الليستيريا، وحصل على الموافقات التنظيمية في العديد من البلدان. أما منتج "ستاف إيفكت" فيستفيد من القدرات المبيدة للبكتيريا للإندوسومالينات في مجال العناية بالبشرة. ويؤكد هذا النهج على "التطبيق العملي"، أي تحويل آليات العاثيات المضادة إلى منتجات ملموسة وقابلة للاستخدام، بدلًا من الاكتفاء بالبقاء على المستوى المختبري.
بشكل عام، من النماذج الخوارزمية إلى التحقق التجريبي ثم إلى التطبيقات الصناعية، تتشكل تدريجياً سلسلة متكاملة لأبحاث مضادات العاثيات. ومن المتوقع أنه مع تراكم المزيد من البيانات وتطوير النماذج، سيستمر هذا المسار، الذي يبدأ بالحسابات، ويتحقق من خلال التجارب، ويسترشد بالتطبيقات، في تعزيز فهم أعمق لأنظمة المناعة البكتيرية، وترجمة هذه النتائج بشكل أكثر فعالية إلى حلول عملية.
روابط مرجعية:
https://mp.weixin.qq.com/s/usrVEOeBD5gphhslZahLCA
https://mp.weixin.qq.com/s/Pxlh69TXSr8ffAp_ul3URw