Command Palette
Search for a command to run...
تجاوز قيود التكامل متعدد الوسائط التقليدي! يقترح معهد ماساتشوستس للتكنولوجيا إطار عمل أبولو، الذي يحقق فصلاً واضحاً بين المعلومات المشتركة بين الخلايا والمعلومات الخاصة بكل خلية.
في أبحاث بيولوجيا الخلية الواحدة، يُسهم التطور السريع لتقنيات القياس في توسيع آفاق الاستكشاف العلمي باستمرار. وقد مكّنت الإنجازات في مجالات مثل التصوير المتعدد، وتسلسل النسخ الجيني للخلية الواحدة (scRNA-seq)، وتسلسل الكروماتين المفتوح (scATAC-seq)، والكشف عن وفرة البروتينات، الباحثين من إجراء ملاحظات شاملة للخلايا المفردة من أبعاد متعددة، تشمل تنظيم النسخ، وحالة الكروماتين، والتعبير البروتيني، والبنية المورفولوجية. تُفسّر هذه البيانات متعددة الوسائط شفرة الحياة من مستويات مختلفة، ويُتيح تكاملها التكميلي فرصة غير مسبوقة للكشف عن التباين الخلوي واستكشاف آليات الأمراض.
ومع ذلك، لا تزال الأساليب التحليلية الحالية تعاني من قيود كبيرة عند التعامل مع مثل هذه البيانات عالية الإنتاجية.غالباً ما تتضمن الاستراتيجيات السائدة تحليل كل نمط على حدة ثم مقارنتها، وهو أمر ليس غير فعال فحسب، بل يجعل من الصعب أيضاً التقاط الارتباطات العميقة بين الأنماط.هناك نوع آخر من الأساليب يدمج البيانات متعددة الوسائط في نفس الفضاء الكامن من خلال تعلم التمثيل، ولكنه غالباً ما يخلط بين المعلومات المشتركة والمعلومات الخاصة بكل وسيط، مما يحجب المساهمة الفريدة لكل بُعد في وظيفة الخلية.
تبرز هذه المشكلة بشكل خاص في التحليل المتكامل لبيانات scATAC-seq و scRNA-seq المزدوجة.غالبًا ما تُبسّط الطرق التقليدية إمكانية الوصول إلى الكروماتين إلى مستوى الجين للمقارنة مع التعبير الجيني. ورغم أن هذا يُبسّط المشكلة، إلا أنه قد يُهمل معلومات هيكلية دقيقة على مستوى الكروماتين، ولا يُمكن تطبيقه إلا على أنواع البيانات ذات الخصائص المتجانسة نسبيًا. أما طرق التكامل الأكثر تعقيدًا، مثل النماذج الخطية والشبكات التوليدية التنافسية، فتواجه صعوبة في التكيف مع البيانات غير المهيكلة كالتصوير، أو تُعاني من ضعف الأداء في فصل المعلومات المشتركة عن المعلومات الخاصة، ما يُعيق تلبية الطلب المتزايد على تحليل البيانات متعددة الوسائط في بنوك البيانات الحيوية الكبيرة.
لذلك، ومع التطور المستمر لتكنولوجيا الخلية الواحدة والنمو السريع لحجم البيانات، أصبحت كيفية دمج البيانات متعددة الوسائط بكفاءة وتلقائية مع فصل المعلومات المشتركة بوضوح عن المعلومات الخاصة بكل نمط تحديًا أساسيًا يواجه بيولوجيا الخلية الواحدة.
ولمعالجة هذا التحدي، اقترح فريق بحث مشترك من معهد ماساتشوستس للتكنولوجيا ومعهد زيورخ للتكنولوجيا إطار عمل عام للحوسبة العميقة يسمى أبولو (المشفر التلقائي مع مساحة كامنة متداخلة جزئيًا يتم تعلمها من خلال التحسين الكامن).يوفر هذا الإطار مسارًا تقنيًا عمليًا لتحليل أكثر شمولية ودقة لحالات الخلايا ومنطقها التنظيمي من خلال نمذجة المعلومات المشتركة والمعلومات الخاصة بكل نمط بشكل صريح.
وقد نُشرت نتائج البحث ذات الصلة، بعنوان "التضمين متعدد الوسائط المشترك جزئيًا يتعلم التمثيل الشامل لحالة الخلية"، في مجلة Nature Computational Science.
أبرز الأبحاث:
* يقترح هذا البحث APOLLO، وهو إطار عمل عام للتعلم العميق يمكنه فصل "المعلومات المشتركة" عن "المعلومات الخاصة بالوسائط" في البيانات متعددة الوسائط بشكل تلقائي وصريح.
* يتعلم نظام APOLLO فضاءً كامنًا متداخلًا جزئيًا من خلال تزويد كل نمط بمشفر تلقائي واستخدام استراتيجية تدريب من خطوتين، وبالتالي تحديد وتمييز الإشارات البيولوجية التي يتم التقاطها بشكل مشترك عبر أنماط متعددة بشكل فعال.
* يمكن لـ APOLLO أن يكشف عن العلاقة بين الاختلافات في التموضع الخلوي الفرعي للبروتين وشكل حجرات الخلية المختلفة، وبالتالي توسيع نطاق التحليل من بيانات علم الجينوم البحتة إلى مجال التشكل المكاني.

عنوان الورقة:
https://www.nature.com/articles/s43588-025-00948-w
تابع حسابنا الرسمي على WeChat وأجب بكلمة "APOLLO" في الخلفية للحصول على ملف PDF كامل.
مجموعة البيانات: تحقق شامل يغطي التسلسل والتصوير
لتقييم أداء إطار عمل APOLLO بشكل شامل، استخدمت الدراسة مجموعات بيانات متعددة متاحة للجمهور للخلايا المفردة متعددة الوسائط، والتي تغطي تقنيات التسلسل والتصوير.
فيما يتعلق ببيانات التسلسل،استخدم الباحثون في البداية بيانات النسخ الجيني للخلايا المفردة المزدوجة (scRNA-seq) وبيانات إمكانية الوصول إلى الكروماتين (scATAC-seq) التي تم قياسها بواسطة تقنية SHARE-seq للتحقق مما إذا كان بإمكان APOLLO تحديد وتمييز نشاط الجينات الذي تم التقاطه بواسطة كل من النسخ الجيني وإمكانية الوصول إلى الكروماتين، بالإضافة إلى نشاط الجينات الذي تم التقاطه بواسطة نمط واحد فقط من أي منهما.
ثانيًا، استخدم الباحثون بيانات وفرة بروتينات سطح الخلية المقترنة بـ scRNA-seq والتي تم الحصول عليها بواسطة CITE-seq لاختبار مدى قابلية تطبيق النموذج على بيانات التسلسل.تم اشتقاق مجموعة بيانات CITE-seq من طحال الفئران والعقد اللمفاوية، وتتضمن مجموعتين من عينات الفئران البرية التي خضعت لعلاج تجريبي مستقل.لا يمكن استخدامه فقط لتقييم قدرة التمييز بين أنواع الخلايا، ولكنه يكشف أيضًا عن تأثير الدفعة التجريبية الناجم عن مصادر الفئران المختلفة.
فيما يتعلق ببيانات التصوير،قدّم الباحثون مجموعة بيانات تصوير متعددة لخلايا الدم المحيطية أحادية النواة (PBMCs) البشرية، تضم 32345 خلية من 40 مريضًا، مصنفة إلى أربع فئات تشخيصية: سليمة، ورم سحائي، ورم دبقي، وأورام الرأس والرقبة. جُمعت مجموعتان من بيانات التصوير من كل مريض بناءً على تركيبات مختلفة من الأجسام المضادة: استخدمت إحدى المجموعتين صبغة DAPI لتحديد الكروماتين، بالإضافة إلى تلوين الأجسام المضادة CD4 وCD8 وCD16؛ بينما استخدمت المجموعة الأخرى صبغة DAPI أيضًا، ولكن مع تلوين الأجسام المضادة لامين وCD3 وγH2AX.
أظهرت الاختبارات التي أجريت باستخدام هذه المجموعة من البيانات ما يلي:يستطيع نظام APOLLO تحديد معلومات الحالة الخلوية المشتركة بين الطريقتين في بنية الكروماتين وتحديد موقع البروتين، بالإضافة إلى السمات المورفولوجية التي تلتقطها طريقة واحدة فقط.بالإضافة إلى ذلك، ومن خلال الجمع بين علامات تلوين الخلايا الإضافية مثل الأنابيب الدقيقة والشبكة الإندوبلازمية، استخدمت الدراسة أيضًا بيانات تصوير متعددة من أطلس البروتين البشري (HPA) لإثبات أنه يمكن استخدام APOLLO للكشف عن العلاقة بين الاختلافات في التموضع الخلوي الفرعي للبروتين وشكل حجرات الخلية المختلفة.
نموذج أبولو: مُشفِّر تلقائي يستخدم استراتيجية التحسين الكامن
لمعالجة المشكلة الشائعة في أساليب التكامل متعدد الوسائط الحالية التي تخلط بين المعلومات المشتركة والمعلومات الخاصة بكل وسيط، تقترح هذه الدراسة إطار عمل APOLLO. يستخدم هذا الإطار التحسين الكامن لتعلم مُشفِّر تلقائي في فضاء كامن متداخل جزئيًا، بهدف التعلم التلقائي وفصل المعلومات المشتركة عن المعلومات الخاصة بكل وسيط بشكل فعال عبر وسائط متعددة. على عكس المُشفِّرات التلقائية التقليدية التي تُحاذي جميع الأبعاد الكامنة بشكل موحد،يقوم برنامج APOLLO بإجراء محاذاة متعددة الوسائط فقط على بعض الأبعاد المحتملة، مع الاحتفاظ بالأبعاد المتبقية للمعلومات الخاصة بكل وسيط، وبالتالي تحقيق فصل واضح بين المعلومات المشتركة والمعلومات الخاصة في تصميم النموذج.
فيما يتعلق ببنية النموذج،تم تجهيز أبولو بجهاز تشفير تلقائي لكل نمط من أنماط البيانات ويمكنه إدخال أجهزة فك تشفير إضافية حسب الحاجة للمهمة.يستخدم كل من المُشفِّر والمُفكِّك هياكل شبكات عصبية مُكيَّفة مع طرائق مُحدَّدة؛ فعلى سبيل المثال، تُستخدم الشبكات الالتفافية لبيانات التصوير، بينما تُستخدم الشبكات كاملة الاتصال لبيانات التعبير الجيني، وذلك لاستيعاب خصائص البيانات لكل طريقة بشكل كامل. يُقسَّم الفضاء الكامن صراحةً إلى جزأين: سمات كامنة مشتركة وسمات كامنة خاصة بكل طريقة. عادةً ما يكون بُعد الفضاء الكامن المشترك أكبر بكثير من بُعد الفضاء الخاص بكل طريقة لضمان تمثيل كافٍ للمعلومات المشتركة بين الطرائق.
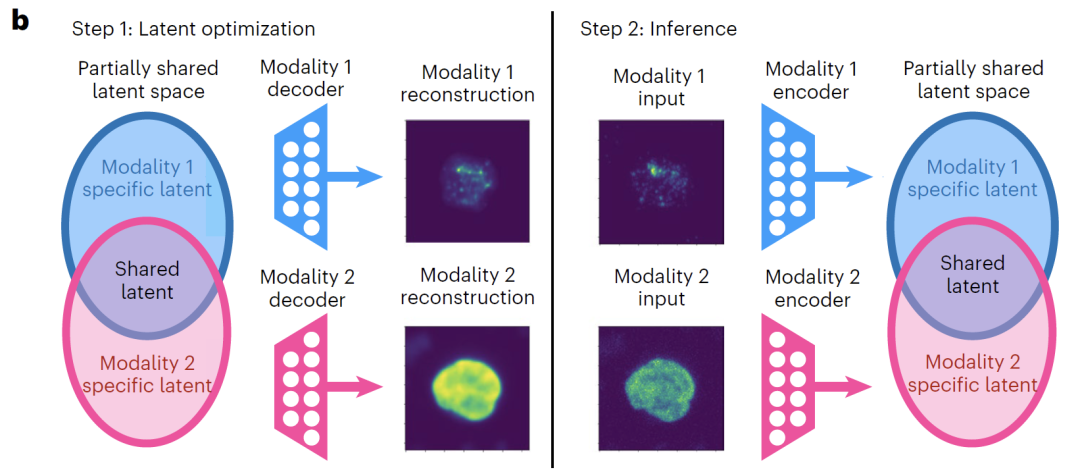
كما هو موضح في الشكل أدناه، تتكون عملية تدريب أبولو من خطوتين:تركز الخطوة الأولى على تدريب أجهزة فك التشفير لكل نمط، مع تحديث الفضاء الكامن في نفس الوقت.يتمثل الهدف الأساسي في تمكين وحدة فك التشفير من إعادة بناء بيانات الإدخال بدقة من الفضاء الكامن. إذا تطلبت المهمة تعزيز تمثيل المعلومات المشتركة وتحقيق التنبؤ عبر الوسائط، يتم إدخال وحدتي فك تشفير إضافيتين لربط الفضاء الكامن المشترك بكل وسيط على حدة، ويتم إكمال التدريب عن طريق تقليل خسارة إعادة البناء.
الخطوة الثانية هي تدريب المشفر الخاص بالنمط.يتم ربط كل نمط بيانات بفضائه الكامن المقابل. ومن خلال تقليل متوسط مربع الخطأ، يتم استنتاج تمثيل العينات غير المشاركة في التدريب في الفضاء الكامن، مما يضمن قدرة النموذج على التعميم بشكل جيد.
وللتحقق من صحة النموذج، اختبرت الدراسة أولاً أداء فصل APOLLO على خمس مجموعات بيانات محاكاة ذات هياكل أساسية حقيقية معروفة.تظهر النتائج أن النموذج يمكنه الحفاظ على أداء مستقر بغض النظر عن التبعية بين السمات الكامنة المشتركة والخاصة.أظهرت المزيد من عمليات التحقق على البيانات الحقيقية أن التعلم الصريح لـ APOLLO لمشاركة المعلومات الجزئية لا يمكنه فقط فصل المعلومات متعددة الوسائط، بل يمكنه أيضًا تحقيق تنبؤات دقيقة عبر الوسائط، مثل التنبؤ بالبروتينات غير المكتشفة من تصوير الكروماتين.
بشكل عام، يقوم برنامج APOLLO بفصل وتفسير المعلومات المشتركة والخاصة بالنمط في مجموعات البيانات متعددة الوسائط بشكل فعال من خلال تعلم المساحات الكامنة المشتركة جزئيًا، مما يوفر إطارًا عامًا للكشف عن الآليات البيولوجية.
بالإضافة إلى أطر التكامل متعددة الوسائط التقليدية، هناك حاجة إلى فهم أكثر شمولاً لحالات الخلايا.
لتقييم شمولية ومزايا نموذج APOLLO الأساسية بشكل شامل، تم تصميم سلسلة من التجارب حول خمسة اتجاهات: تكامل بيانات التسلسل الزوجي، وتكامل تصوير الكروماتين والبروتين، والتنبؤ متعدد الوسائط، والتعرف على السمات المورفولوجية، واستكشاف التوطين الخلوي الفرعي للبروتين.
في تكامل بيانات التسلسل المزدوجأظهرت تجارب SHARE-seq أن إضافة مساحة خاصة بالنمط إلى المساحة المشتركة يمكن أن يحسن بشكل كبير من دقة تصنيف نوع الخلية، مما يثبت أن المساحة المحددة يمكنها التقاط المعلومات البيولوجية غير المدرجة في المساحة المشتركة.
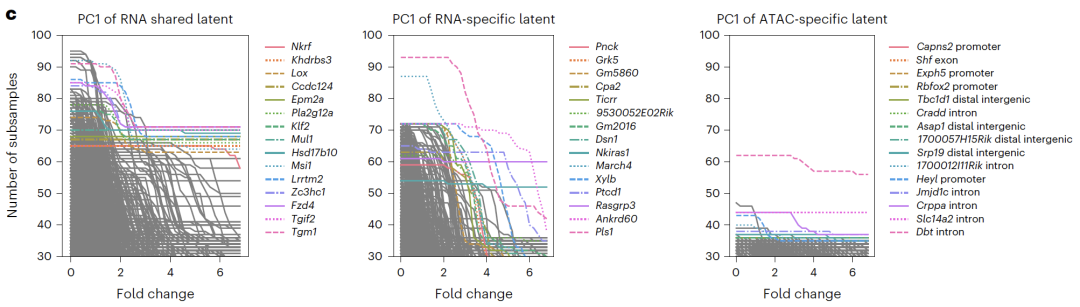
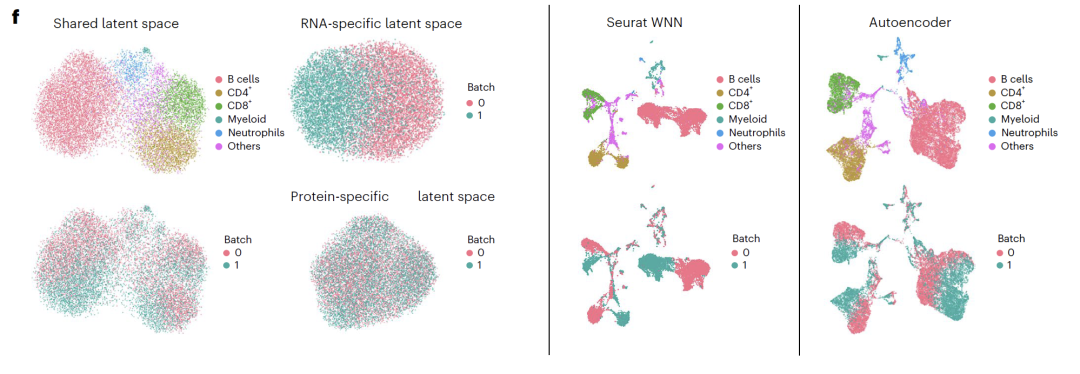
كشف التفسير المكاني المحتمل أن المساحات الخاصة بالحمض النووي الريبوزي (RNA) كانت غنية بالجينات المرتبطة بدورة الخلية، وأن المساحات الخاصة بـ ATAC كانت غنية بمناطق الكروماتين المفتوحة المرتبطة بتنظيم النسخ، وأن المساحات المشتركة كانت غنية بعوامل النسخ المعروفة ومسارات التنظيم، مما يؤكد الأهمية البيولوجية لنتائج الفصل. في تجارب CITE-seq،نجح مشروع APOLLO في فصل تأثيرات نوع الخلية وتأثيرات الدفعة إلى مساحة مشتركة ومساحة خاصة بالحمض النووي الريبي.لا تستطيع طرق التكامل الحالية تحقيق هذا النوع من الفصل، مما يسلط الضوء على المزايا الفريدة للنموذج في دمج بيانات التسلسل.
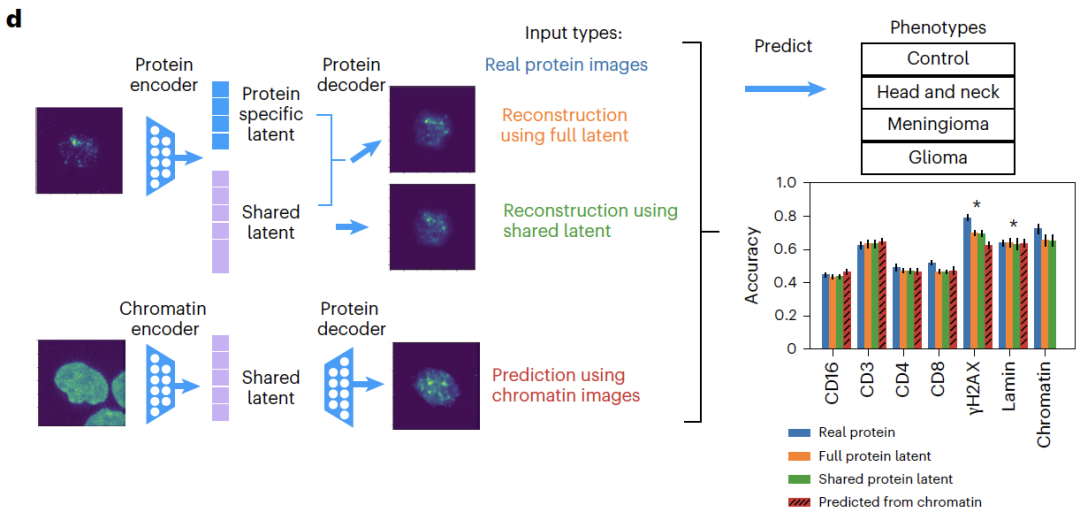
فيما يتعلق ببيانات التصوير،يستطيع نظام أبولو إعادة بناء صور الخلايا بدقة من المرضى الذين لم يشاركوا في التدريب.في مهمة التنبؤ بالبروتينات غير المكتشفة من الكروماتين عبر الوسائط المتعددة، يتفوق برنامج APOLLO بشكل كبير على طرق ترميم الصور التقليدية؛أظهر التصنيف الظاهري اللاحق أن دقة التصنيف القائمة على تصوير البروتين المتوقع كانت مماثلة لتلك الخاصة بالتصوير الفعلي، حيث أظهر بروتين CD3 أفضل أداء تنبؤي، مما يؤكد أنه يمكن استخدام نتائج التنبؤ بشكل فعال للاكتشاف البيولوجي.
في مهام التعرف على السمات المورفولوجية،تُجسّد المساحة المشتركة بشكل أساسي الخصائص المورفولوجية للكروماتين (مثل مساحة النواة وحجم الكروماتين المغاير)، بينما توجد الخصائص الخاصة بالبروتين، مثل عدد بؤر γH2AX، فقط في مساحاتها الخاصة المقابلة. وقد أظهرت تجارب إزالة الخصائص أن إزالة هذه الخاصية قللت بشكل ملحوظ من دقة التصنيف الظاهري، مما يؤكد دقة الفصل.

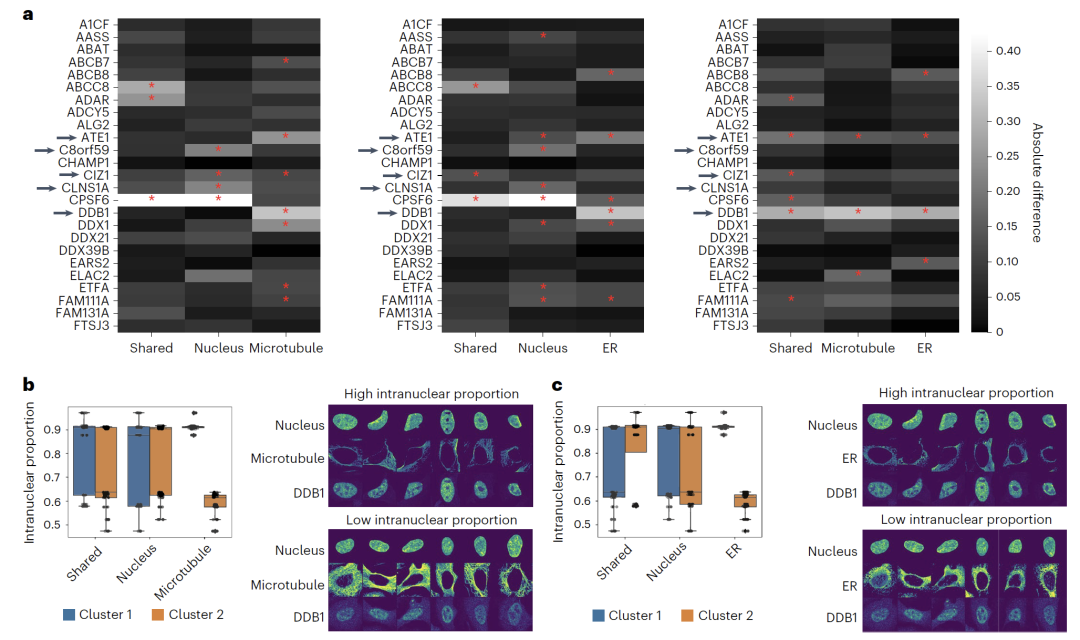
في دراسة التموضع الخلوي الفرعي للبروتينأظهر تطبيق برنامج APOLLO على بيانات تصوير خلايا U2OS أن الاختلافات في تموضع البروتينات داخل النواة يمكن رصدها من خلال خصائص الحجيرات الخلوية المختلفة. على سبيل المثال، يرتبط التموضع النووي لبروتين DDB1 ببنية الشبكة الإندوبلازمية والأنابيب الدقيقة، بينما يرتبط بروتين CLNS1A ببنية النواة فقط. تشير هذه النتيجة إلى أن...يمكن توسيع النموذج ليشمل تركيبات تصوير متنوعة، مما يوفر منظورًا جديدًا لفهم العلاقة بين توضع البروتين وشكل الخلية.
تنفيذ تكامل البيانات متعددة الوسائط للخلايا المفردة
أصبح دمج البيانات متعددة الوسائط للخلايا المفردة اتجاهًا تكنولوجيًا أساسيًا لتحليل عدم تجانس الخلايا، والكشف عن آليات المرض، وتعزيز تطوير الطب الدقيق، وقد حظي باهتمام واسع النطاق من المجتمع الأكاديمي العالمي.
على سبيل المثال، تقنية scMTR-seq التي طورها فريق بيتر روج-جان في معهد بابراهام بجامعة كامبريدج...لأول مرة، تم تحقيق التقاط متزامن لستة تعديلات هيستون والنسخة الكاملة من النسخ الجيني على مستوى الخلية الواحدة.لقد تغلبوا على عقبة تقنية في مجال أبحاث علم التخلق استمرت لعقد من الزمان.
عنوان الورقة:
التحليل التجميعي لتعديلات الهيستون المتعددة والنسخ الجيني في الخلايا المفردة باستخدام تقنية scMTR-seq
رابط الورقة:
https://www.science.org/doi/10.1126/sciadv.adu3308
يقوم إطار عمل CellFuse الذي اقترحه فريق البحث بجامعة ستانفورد بإنشاء مساحة تضمين مشتركة تعتمد على التعلم التبايني الخاضع للإشراف، وهو مصمم خصيصًا لسيناريوهات التكامل متعدد الوسائط مع تداخل محدود في الميزات.يمكنه تحقيق تنبؤ دقيق بنوع الخلية والتكامل السلس عبر مختلف الوسائط والظروف التجريبية.أظهرت الاختبارات التي أجريت على مجموعات بيانات متعددة، بما في ذلك الخلايا الليمفاوية المحيطية السليمة، ونخاع العظم، وعلاج CAR-T لسرطان الغدد الليمفاوية، وأنسجة الورم، أن الإطار يتفوق على الطرق الحالية من حيث جودة التكامل والكفاءة التشغيلية.
عنوان الورقة:
يُمكّن برنامج CellFuse من دمج بيانات البروتينات أحادية الخلية والبروتينات المكانية متعددة الوسائط
رابط الورقة:
في غضون ذلك، تُسرّع شركات التكنولوجيا الحيوية والرعاية الصحية العالمية الرائدة من وتيرة نشر تقنية دمج البيانات متعددة الوسائط للخلايا المفردة، مع التركيز على سيناريوهات أساسية كالتطبيقات السريرية، وتطوير الأدوية، والطب الدقيق، بهدف تحويل الأبحاث المتطورة إلى تطبيقات عملية. وقد طبّقت شركة BioNTech الألمانية هذه التقنية في مجال العلاج المناعي للأورام وتطوير اللقاحات الشخصية. فمن خلال دمج بيانات تسلسل الحمض النووي الريبوزي للخلايا المفردة، وتحليل التعبير البروتيني، وبيانات النسخ المكاني، تُحلّل الشركة بدقة التباين الخلوي في البيئة الدقيقة للورم، وتُحدّد الأنواع الفرعية الرئيسية للخلايا المناعية والمؤشرات الحيوية ذات الصلة، مما يُوفّر دعماً أساسياً للبيانات اللازمة لتصميم وتحسين لقاحات الأورام الشخصية، ويُحسّن بشكل ملحوظ استهداف اللقاح وفعاليته.
من المتوقع أنه بفضل الاختراقات المستمرة في تكنولوجيا التكامل متعدد الوسائط، فإن فك شفرة الحياة على مستوى الخلية الواحدة سينتقل في النهاية من مجرد رؤية إلى واقع، مما سيعطي زخماً أقوى لمستقبل الطب الدقيق.