Command Palette
Search for a command to run...
استنادًا إلى البيانات السريرية من 11647 حالة، حقق فريق فرنسي، ولأول مرة، تنبؤًا دقيقًا بمخاطر الوفاة المزدوجة في زراعة الكبد لسرطان الخلايا الكبدية باستخدام التعلم الآلي.

يُعرف سرطان الكبد منذ زمن طويل بـ"ملك السرطانات" نظراً لمراحله المبكرة الخبيثة وتطوره السريع. ومن بين أنواعه، يُعد سرطان الخلايا الكبدية (HCC) أكثر أنواع سرطان الكبد شيوعاً، إذ يُمثل ما بين 701% و90% من حالات سرطان الكبد الأولي. يحتاج المرضى عادةً إلى زراعة الكبد كعلاج جذري في المراحل المبكرة، وهو أيضاً بمثابة "طوق النجاة" الأخير لكثير من مرضى سرطان الخلايا الكبدية الذين يتمسكون بأمل الحياة.
ومع ذلك، فإن الندرة الشديدة للأعضاء المتبرع بها تجعل هذا الأمل في الحياة أكثر قيمة. ويزداد الأمر صعوبةً مع مواجهة المرشحين لزراعة الكبد المصابين بسرطان الخلايا الكبدية خطرًا مزدوجًا يتمثل في الموت نتيجة فشل الكبد وتفاقم الورم؛ فهذان العاملان مترابطان ومؤثران على بعضهما البعض، مما يزيد بشكل كبير من خطر الوفاة خلال فترة الانتظار. لذلك،إن التقييم الدقيق لمخاطر الوفاة خلال فترة انتظار المرشحين لزراعة الكبد المصابين بسرطان الخلايا الكبدية ليس فقط مفتاحًا لتحسين أولوية قائمة انتظار زراعة الكبد وتحقيق التوزيع العادل للمتبرعين النادرين، ولكنه أيضًا يمثل تحديًا أساسيًا لإنقاذ كل مريض بكفاءة والحفاظ على الأمل الذي تم تحقيقه بشق الأنفس في الحياة.
في السابق، كانت أساليب تقييم المخاطر التقليدية، مثل تصنيف تشايلد-بوغ، ومؤشر الألبومين-البيليروبين (ALBI)، ونموذج مرض الكبد في مراحله النهائية (MELD)، شائعة الاستخدام في تقييم مخاطر أمراض الكبد. إلا أنها أظهرت قصورًا كبيرًا عند التعامل مع الحالة المعقدة لمرضى سرطان الخلايا الكبدية: إذ ركزت هذه الأساليب إما على تقييم وظائف الكبد ودرجة التليف، أو على التنبؤ بتطور الورم فقط، دون معالجة كلا الخطرين في آن واحد. وحتى مع التطور اللاحق لأنظمة تسجيل شاملة، مثل HALT-HCC ونموذج ميهتا، التي تأخذ كلا الخطرين في الاعتبار معًا،أيضًا، نظرًا لقيود النماذج الخطية، وأوزان المتغيرات الثابتة، والقياسات الثابتة عند نقطة زمنية واحدة، فمن المستحيل رصد التفاعلات بين العوامل المؤثرة وتغيرات المخاطر في التطور الديناميكي للمرض، مما يجعل من الصعب تحقيق تقييم دقيق للمخاطر الفردية.
استجابةً لهذه المشكلة السريرية،اقترح فريق بحثي من شركة Telecom Sud-Paris وجامعة Paris-Saclay في فرنسا إطار عمل للتعلم الآلي يدمج التعلم الجماعي (EL) مع تحليل Schapel Additive exPlanations (SHAP).تقدم هذه الدراسة منهجًا جديدًا لتقييم خطر الوفاة لدى المرشحين لزراعة الكبد المصابين بسرطان الخلايا الكبدية. استنادًا إلى بيانات سريرية من 11647 مريضًا، قارنت الدراسة ثلاثة نماذج تجميعية: الغابة العشوائية (RF)، وXGBoost، وLightGBM. علاوة على ذلك، من خلال تضمين قيم SHAP في فضاء UMAP منخفض الأبعاد، ودمجها مع خوارزمية K-medoids للتجميع الخاضع للإشراف، أوضحت الدراسة أن خلل وظائف الكبد وتطور الورم هما العاملان الرئيسيان المؤديان للوفاة لدى مرضى سرطان الخلايا الكبدية.
تسد هذه الدراسة على وجه التحديد ثغرة في نماذج التعلم الآلي السابقة لتقييم المرشحين لزراعة الكبد المصابين بسرطان الخلايا الكبدية بدقة، وخاصة في الدراسات التي تنطوي على مخاطر مزدوجة.تحقق هذه الدراسة تنبؤًا دقيقًا وقابلية تفسير سريرية للوفيات خلال فترة الانتظار التي تبلغ 3 أشهر لمرشحي زراعة الكبد المصابين بسرطان الخلايا الكبدية، مما يوفر أداة جديدة لاتخاذ القرارات السريرية وتصنيف المخاطر لدى مرضى سرطان الخلايا الكبدية الذين يخضعون لزراعة الكبد.
تم نشر النتائج، التي تحمل عنوان "التنبؤ بالوفيات القابلة للتفسير لمرشحي زراعة الكبد المصابين بسرطان الخلايا الكبدية: نهج التجميع الخاضع للإشراف"، في مجلة علوم البيانات الصحية.
أبرز الأبحاث:
* هذه الدراسة هي أول دراسة شاملة تستخدم نماذج التعلم الآلي لتحليل مخاطر الوفاة لدى المرشحين لزراعة الكبد المصابين بسرطان الخلايا الكبدية الموجودين على قائمة الانتظار بشكل معمق.
* باستخدام SHAP + UMAP + K-medoids، تم تصنيف سبع مجموعات فرعية من المخاطر قابلة للتفسير سريريًا لتحديد المحركات الأساسية للمخاطر المزدوجة.
* تُظهر درجة المخاطر الجديدة ELM-HCC، التي تم إنشاؤها بناءً على فحص SHAP لـ 8 متغيرات رئيسية، دقة تنبؤية أعلى بكثير من الدرجات التقليدية.
* هذه الدراسة هي الأولى التي تدمج المتغيرات الديناميكية الرئيسية (مثل AFP_DIFF) في تقييم مخاطر المرشحين لزراعة الكبد المصابين بسرطان الخلايا الكبدية، مما يوضح دورها كمتنبئ رئيسي للوفيات خلال فترة انتظار مرضى سرطان الخلايا الكبدية.
عنوان الورقة:
https://spj.science.org/doi/10.34133/hds.0295
تابع حسابنا الرسمي على WeChat وأجب بكلمة "زراعة كبد" في الخلفية للحصول على ملف PDF كامل.
اطلع على المزيد من الأبحاث الرائدة في مجال الذكاء الاصطناعي:
مجموعة البيانات: استراتيجية العينة الكبيرة + مقدمة عن المتغيرات الديناميكية
لتقليل العوامل المربكة،استخدمت الدراسة استراتيجية عينة كبيرة تعتمد على بيانات قواعد البيانات العامة.
وعلى وجه التحديد، جاءت بيانات الدراسة من ملفات التحليل والبحث القياسي لزراعة الأعضاء (STAR) التابعة لشبكة شراء الأعضاء وزراعتها (OPTN) والشبكة المتحدة لتبادل الأعضاء (UNOS)، والتي تغطي مرضى سرطان الخلايا الكبدية البالغين الذين لم يخضعوا لعمليات زرع أعضاء متعددة وتم تسجيلهم بين 27 فبراير 2002 و30 سبتمبر 2023.
هدفت هذه الدراسة إلى التنبؤ بمعدل الوفيات خلال فترة الانتظار التي تبلغ ثلاثة أشهر لزراعة الكبد لدى مرضى سرطان الخلايا الكبدية. ولذلك، قام فريق البحث بتقسيم عينة الدراسة إلى مجموعتين لتحليل البيانات.يُشار إلى المرضى الذين ظلوا على قائمة الانتظار لأكثر من ثلاثة أشهر باسم "على قائمة الانتظار"؛ ويُشار إلى المرضى الذين يموتون على قائمة الانتظار في غضون ثلاثة أشهر أو الذين تتدهور حالتهم وتجعلهم غير قادرين على تلقي عملية زرع باسم "وفيات قائمة الانتظار".أخير،شملت المجموعة الكاملة للدراسة 11647 مريضًا.من بين هؤلاء، كان 11199 مريضًا على قائمة الانتظار، و448 مريضًا على قائمة انتظار الوفاة. وشملت البيانات متغيرات سريرية ومخبرية ومتغيرات متعددة الأبعاد متعلقة بالمرض.
في مرحلة المعالجة المسبقة للبيانات، ولرصد الخصائص الديناميكية للحالة الصحية للمرضى، قام فريق البحث بحساب الفرق في القياس المستمر (DIFF) لستة متغيرات مختبرية رئيسية متضمنة في التقييم التقليدي، بما في ذلك صوديوم المصل، والكرياتينين، والألبومين، والبيليروبين، وألفا فيتوبروتين (AFP)، والنسبة المعيارية الدولية (INR)، وذلك من أجل رصد المسار الديناميكي للتغيرات في الحالة الصحية للمرضى.وهذا يزيد العدد الإجمالي للميزات إلى 31 (25 متغيرًا ثابتًا أصليًا + 6 متغيرات ديناميكية مضافة حديثًا).
لمعالجة القيم المفقودة، تم تعويض المتغيرات العددية (معدل الفقد < 7%) باستخدام متوسط الفئة؛ وتم حذف سجلات الملاحظات الخاصة بالمتغيرات الفئوية (معدل الفقد < 0.1%) التي تحتوي على قيم مفقودة بشكل مباشر.
بنية النموذج: عملية متكاملة شاملة + مقارنة نماذج التعلم الجماعي المتعددة
لضمان دقة وموثوقية تفسير التنبؤ بمعدل الوفيات خلال فترة الانتظار التي تبلغ 3 أشهر للمرشحين لزراعة الكبد المصابين بسرطان الخلايا الكبدية،قام فريق البحث ببناء عملية متكاملة من البداية إلى النهاية تجمع بين التعلم الجماعي، وتحليل قابلية تفسير SHAP، وتقليل أبعاد UMAP، والتجميع الخاضع للإشراف K-Medoids.كما هو موضح في الشكل التالي:
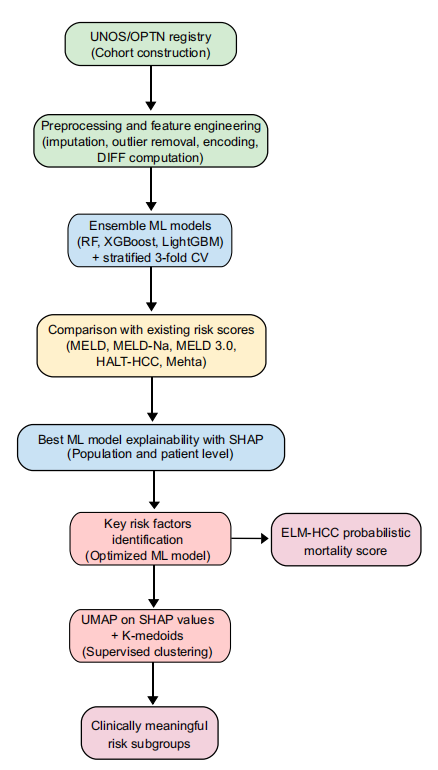
أولاً، يستخدم النموذج الأساسي نموذج شجرة التعلم الجماعي.تُعدّ هذه الأنواع من النماذج فعّالة بشكل خاص في التعامل مع البيانات الجدولية والمتنوعة. وللمقارنة بين أداء هذه النماذج، استخدمت الدراسة ثلاثة نماذج أساسية للتعلم الجماعي: الغابة العشوائية، وXGBoost، وLightGBM. أُجريت التجارب في سيناريوهين تدريبيين: الأول استخدم 25 متغيرًا ثابتًا أصليًا فقط؛ والثاني استخدم 31 متغيرًا مُدمجًا، ثابتًا وديناميكيًا، بما في ذلك المتغيرات الديناميكية.
ثانياً، الغرض من قابلية التفسير هو توفير تفسير علمي ومعقول للنتائج المتوقعة، وبالتالي تعزيز الأساس لاتخاذ القرارات السريرية.ولتحقيق هذه الغاية، قام فريق البحث بدمج تحليل قابلية تفسير SHAP في الإطار لتحديد عوامل الخطر الرئيسية والكشف عن تنبؤات النموذج.
للتفسير الشامل، يُحدد حساب قيم SHAP مساهمة كل خاصية في نتائج تنبؤ النموذج، مما يُساعد في تحديد عوامل الخطر الأساسية للتنبؤ بالوفيات وتوضيح العلاقة بين الخصائص وخطر الوفاة. أما للتفسير المحلي، فتُظهر مخططات ملخص SHAP ومخططات قوة SHAP التأثير المحدد لقيم كل خاصية على نتائج التنبؤ، بالإضافة إلى توزيع مساهمات الخصائص لكل مريض. علاوة على ذلك، تُوفر هذه الخطوة مجموعة خصائص قيم SHAP لتحليل التجميع اللاحق، مما يحل محل البيانات الأصلية ويُحسّن من قابلية تفسير التجميع سريريًا.
وأخيراً، ولتحقيق تصنيف دقيق للمخاطر بالنسبة للمرضى، تحول التركيز من التنبؤ على مستوى السكان إلى التحليل الخاص بالمجموعات الفرعية.تضمنت عملية البحث أساليب تقليل الأبعاد UMAP و K-Medoids للتجميع الخاضع للإشراف.أولًا، تُدمج قيم SHAP المتوقعة في فضاء UMAP المُختزل الأبعاد. ثم، تُستخدم خوارزمية K-Medoids لتجميع قيم SHAP المُدمجة في فضاء UMAP ثلاثي الأبعاد، وذلك لاكتشاف مجموعات فرعية محتملة من المرضى ذوي خصائص سريرية مختلفة. تُسمى هذه الطريقة "التجميع المُشرف" لأن التجميع يعتمد على قيم SHAP وليس على البيانات الأصلية.
تم تحديد العدد الأمثل للمجموعات من خلال الفحص الأولي باستخدام مؤشرات كمية مثل معامل سيلويت ومؤشر ديفيز-بولدين، ثم التحقق سريريًا من خصائص التجميع من خلال تحليل SHAP. وفي النهاية، تم تحديد العدد الأمثل للمجموعات بسبع مجموعات.
النتائج التجريبية: تم تدريب النموذج الجديد باستخدام 8 طرق تقييم تقليدية للمقارنة ومجموعة الميزات المثلى.
مقارنة أداء نقاط المخاطر
تقارن الدراسة أداء الإطار المقترح مع ثمانية أساليب تقليدية لتقييم المخاطر، بما في ذلك ALBI و Child–Pugh و AFP و Hazard associated with LT for HCC (HALT-HCC) و Mehta Model و MELD ومتغيريه MELD-Na و MELD 3.0.
نظراً لعدم توازن الفئات الشديد في مجموعة البيانات، قلّصت الدراسة حجم المجموعة الأكبر (الموجودة على قائمة الانتظار) لإنشاء 30 مجموعة فرعية بحجم مماثل للمجموعة الأصغر (الوفيات خلال فترة الانتظار). أُجري التحقق المتقاطع ثلاثي الطيات على كل مجموعة فرعية متوازنة لضمان تخصيص جميع الملاحظات من المريض نفسه إما لمجموعة التدريب أو مجموعة الاختبار. ثم حُددت أفضل إعدادات المعلمات الفائقة للنماذج التجميعية الثلاثة باستخدام بحث شبكي، كما هو موضح في الشكل أدناه.
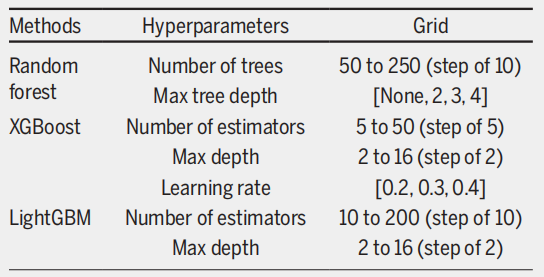
وتظهر النتائج أنفي أنظمة التقييم التقليدية، يحقق نموذج ميهتا أفضل أداء بمساحة تحت منحنى ROC تبلغ 0.782، يليه نموذج HALT-HCC بمساحة تحت منحنى ROC تبلغ 0.763.والأهم من ذلك، أن هذين النموذجين يقدمان أداءً أكثر توازناً من حيث الحساسية والنوعية. فبينما يتفوق نموذج MELD 3.0 على نموذجي MELD وMELD-Na الأساسيين، إلا أنه يعاني من عدم توازن بين الحساسية والنوعية.
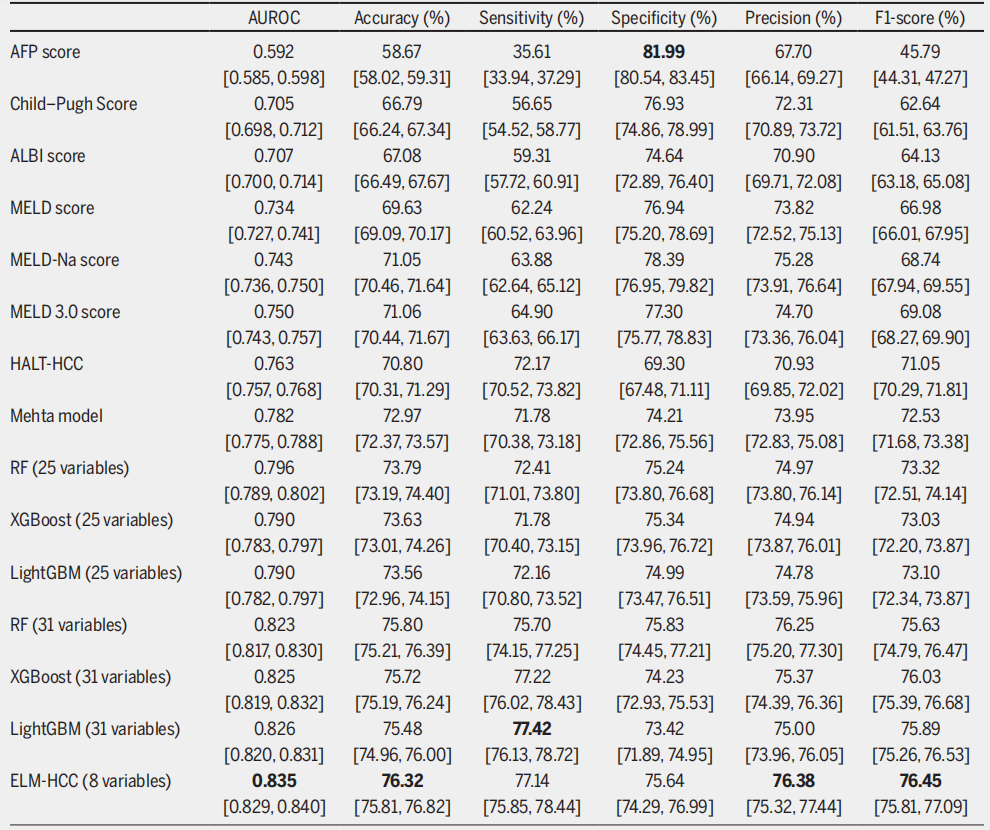
عندما تم توسيع نطاق التجربة لتشمل إطار عمل التعلم الجماعي، تجاوزت دقة جميع النماذج المدربة على 25 متغيرًا ثابتًا دقة أنظمة التقييم التقليدية. حقق نموذج الغابات العشوائية (RF) أفضل أداء، حيث بلغ مؤشر AUROC الخاص به 0.796، كما تميز بتوازن جيد بين حساسيته (72.41%) وخصوصيته (75.24%). بعد إضافة 31 متغيرًا ديناميكيًا وثابتًا، حققت جميع نماذج التعلم الجماعي أداءً أفضل.حقق نموذج LightGBM قيمة AUROC تبلغ 0.826 وأعلى حساسية بلغت 77.42%، مما يجعله النموذج الأكثر فعالية لتحديد المرضى المعرضين لمخاطر عالية.
تحليل القدرة على تحديد عوامل الخطر الرئيسية
بعد تدريب النماذج، سيستخدم البحث أهم الميزات فقط لتقييم أدائها. ولتحقيق هذه الغاية، استخدم فريق البحث طريقتين لتقييم أهمية الميزات، وهما أهمية الربح وأهمية SHAP العالمية، لاختيار الميزات الرئيسية لنموذج LightGBM الأفضل أداءً.
استنادًا إلى نموذج LightGBM (النموذج الأفضل أداءً)، فإن أفضل 8 ميزات تم اختيارها باستخدام الأهمية العالمية لـ SHAP تحقق الأداء الأمثل للنموذج.بمساحة تحت منحنى ROC تبلغ 0.835، وحساسية 77.141، وخصوصية 75.641، لم يتفوق هذا النموذج على نتائج فحص أهمية المكسب (مساحة تحت منحنى ROC تبلغ 0.812 مع 8 خصائص، وبلغت ذروتها عند 0.828 مع 12 خاصية)، بل تجاوز أيضًا أداء نموذج LightGBM على مجموعة كاملة من 31 متغيرًا (مساحة تحت منحنى ROC تبلغ 0.826). لذلك، اختاره فريق البحث كمجموعة الخصائص المثلى.
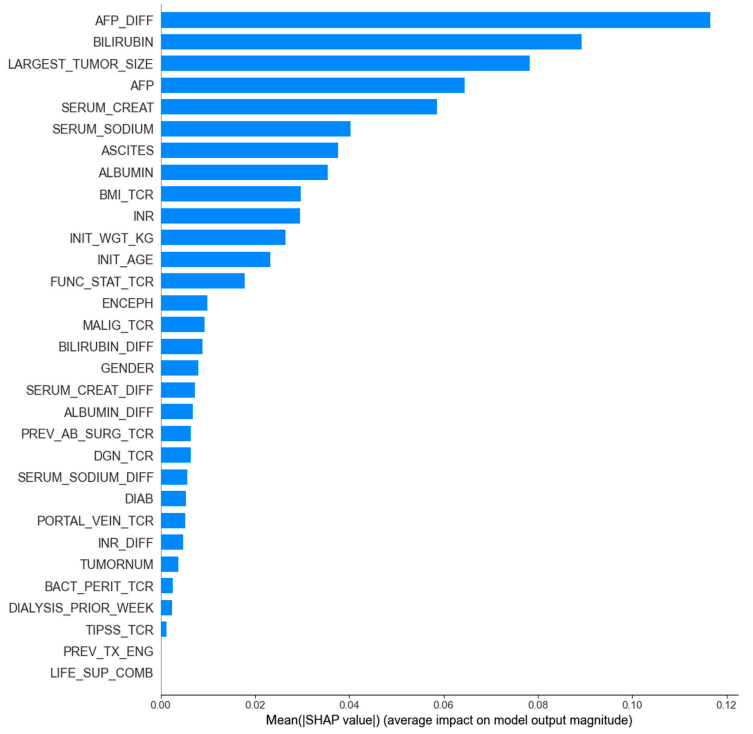
في نهاية المطاف، حددت الدراسة وبنت مؤشرًا احتماليًا للوفيات لدى مرضى سرطان الخلايا الكبدية، أطلق عليه اسم ELM-HCC، استنادًا إلى نموذج LightGBM المدرب باستخدام مجموعة الميزات المثلى. ومن الجدير بالذكر أن...تفوق نموذج LightGBM على نموذج AUROC في مجموعة المتغيرات المبسطة مقارنة بمجموعة المتغيرات الكاملة المكونة من 31 متغيرًا، مما يدل على أن المتغيرات الثمانية المختارة تتمتع بقوة تنبؤية أقوى.وفي الوقت نفسه، فإن ظهور AFP_DIFF في الميزات الرئيسية ذات الصلة يسلط الضوء أيضًا على أهمية دمج المعلومات الديناميكية.
تصنيف المخاطر وتحليل المجموعات الفرعية
حددت الدراسة سبع مجموعات فرعية من المرضى بخصائص سريرية ومستويات خطر مختلفة بناءً على التجميع الخاضع للإشراف باستخدام قيم SHAP. يوضح الشكل (ب) أدناه بوضوح تحليل الوفيات الطبقي مع تزايد احتمالات الوفاة تدريجيًا من المجموعة 1 إلى المجموعة 7.
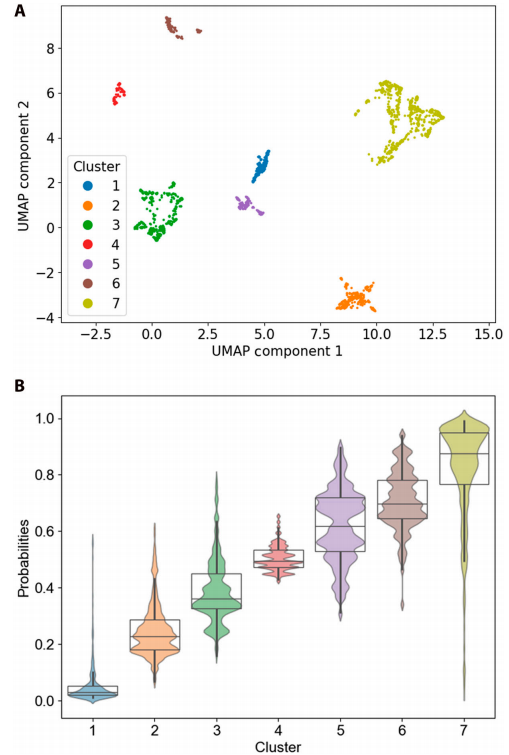
يمثل B مخطط الصندوق ومخطط السكان لاحتمالات الوفيات لـ 7 ملاحظات مجمعة.
أظهر تحليل إضافي باستخدام اختبار كروسكال-واليس اختلافات في المتغيرات بين المجموعات المختلفة. وكما هو موضح في مخطط SHAP، ازداد احتمال الوفاة تدريجيًا من المجموعة 1 إلى المجموعة 7؛ فعلى سبيل المثال، ازداد احتمال الوفاة لمريض نموذجي من 0.03 إلى 0.98.يتوافق هذا الاتجاه مع التصنيفات الملاحظة في مخططات الصندوق، مما يسلط الضوء على فعالية طريقة التجميع.
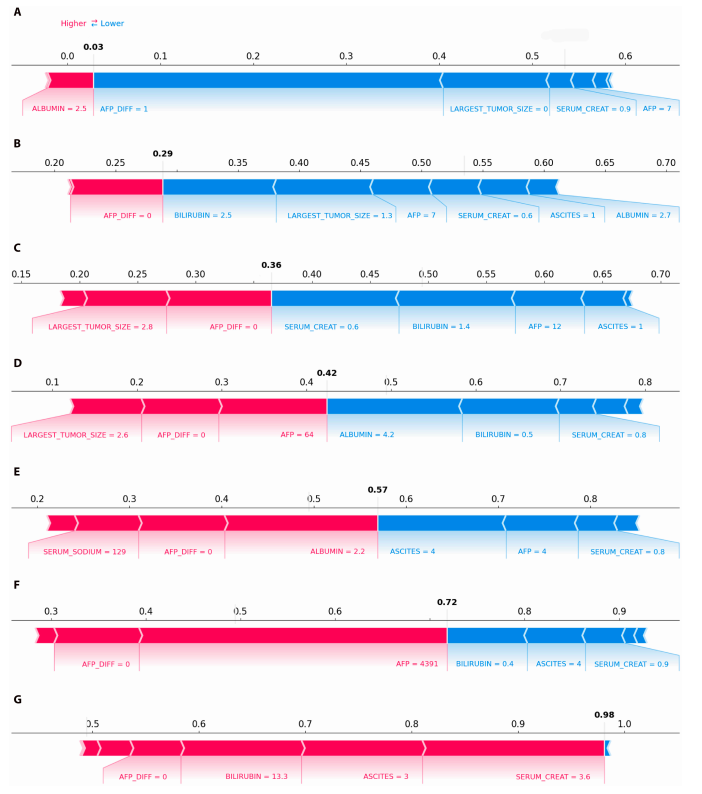
بالإضافة إلى ذلك، كشف تحليل المجموعات الفرعية بوضوح عن سببين رئيسيين لارتفاع خطر الوفاة: الفشل الكبدي الحاد (الذي يتميز بارتفاع البيليروبين، وارتفاع الكرياتينين، والاستسقاء المعتدل، وكلها تتوافق مع قيم SHAP الإيجابية وتزيد بشكل كبير من خطر الوفاة) وتطور الورم النشط (الذي يتميز بارتفاع مستويات AFP).
باختصار، يُظهر إطار عمل التعلم الآلي ELM-HCC، المُعتمد على تحليل قابلية تفسير LightGBM وSHAP والمُقترح في هذه الدراسة، أداءً أفضل بكثير من أنظمة التقييم التقليدية في التنبؤ بخطر الوفاة خلال فترة الانتظار التي تبلغ ثلاثة أشهر لمرشحي زراعة الكبد المصابين بسرطان الخلايا الكبدية. وفي الوقت نفسه، يكشف هذا الإطار عن مجموعات فرعية من المرضى ذوي خصائص خطر مختلفة من خلال التجميع الخاضع للإشراف، مما يوفر أداة تقييم مخاطر أكثر دقة وقابلية للتفسير لدعم اتخاذ القرارات السريرية.
أساليب مبتكرة لتقييم مخاطر المرشحين لزراعة الكبد؛ نهج شامل يسد فجوة بحثية.
كما ذُكر سابقًا، يُصبح سرطان الكبد تحديًا عالميًا للصحة العامة. ونظرًا لتزايد حدة المرض وارتفاع الاحتياجات الطبية، تُعدّ خطة علمية سليمة ومعقولة لقوائم المرشحين لزراعة الكبد بالغة الأهمية. منذ عام ٢٠٠٢، استُخدم نموذج مرض الكبد في مراحله النهائية (MELD) لتحديد أولويات المرشحين لزراعة الكبد. ومع ذلك، وبعد عدة مراجعات، لا يزال توزيع المرضى وفقًا لنموذج MELD غير كافٍ لتلبية احتياجات جميع المرشحين بشكل عادل.
أصبح التعلم الآلي، بقدرته على معالجة البيانات عالية الأبعاد ومتعددة الوسائط، الحل الأمثل للتنبؤ بمخاطر الوفاة لدى المرشحين لزراعة الأعضاء.
سبق تطبيق نماذج التعلم الآلي للتنبؤ بمعدلات وفيات زراعة الكبد. على سبيل المثال، اقترح فريق مشترك من معهد ماساتشوستس للتكنولوجيا وجامعة كاليفورنيا في سان فرانسيسكو وجامعة تكساس نموذج OPOM، وهو نموذج تنبؤ لتحسين معدل الوفيات يعتمد على أشجار التصنيف المثلى (OCTs).استنادًا إلى هذا النموذج لتخصيص الكبد، يمكن تقليل عدد الوفيات سنويًا بحوالي 418 مقارنة بنموذج MELD، مع انخفاض كبير في عدد الوفيات/عمليات الإزالة في جميع مناطق UNOS ومستويات شدة المرض.بالإضافة إلى ذلك، قام النموذج أيضًا بتعديل عدد الكبد المخصصة للمرضى المصابين وغير المصابين بسرطان الخلايا الكبدية، مما أدى إلى تحسين تخصيص زراعة الكبد بشكل كبير وتقليل معدل وفيات المرشحين.
عنوان الأطروحة: تطوير والتحقق من صحة نموذج تنبؤ مُحسَّن لمعدل الوفيات لدى المرشحين المنتظرين لزراعة الكبد
عنوان الورقة:
https://www.sciencedirect.com/science/article/pii/S1600613522090335
مع ذلك، ورغم الأداء الجيد لنموذج OPOM، إلا أنه يعتمد على مجموعة مختلطة من مرضى سرطان الخلايا الكبدية وغير المصابين به، ولا يتناول تحديدًا المخاطر المزدوجة المتمثلة في فشل الكبد وتطور الورم التي يواجهها مرضى سرطان الخلايا الكبدية. ولا شك أن نموذج ELM-HCC يسد هذه الثغرة.
أخيرًا، لا تقتصر هذه الدراسة على تحسين وتوسيع نطاق الأبحاث السابقة فحسب، بل والأهم من ذلك، كما ذكر الباحثون، أنها تسد ثغرة في الأبحاث الحالية. فمن خلال تحقيق أول تنبؤ دقيق وقابل للتفسير لمعدل الوفيات خلال فترة الانتظار التي تبلغ ثلاثة أشهر لمرشحي زراعة الكبد المصابين بسرطان الخلايا الكبدية، فإنها توفر نهجًا جديدًا للتعلم الآلي مقترنًا بتقييم مخاطر مرشحي زراعة الأعضاء.
مراجع:
1. اقترح فريق بحثي من شركة Telecom Sud-Paris وجامعة Paris-Saclay في فرنسا إطار عمل للتعلم الآلي يدمج التعلم الجماعي مع تحليل SHAple Additive exPlanations (SHAP)، مما يوفر حلاً جديداً لتقييم خطر الوفاة لدى المرشحين لزراعة الكبد المصابين بسرطان الخلايا الكبدية.
2.https://www.sciencedirect.com/science/article/pii/S1600613522090335