Command Palette
Search for a command to run...
AIを活用した多様な低分子結合タンパク質の新規設計:韓国の研究チームが、ストレスホルモンを選択的に認識できるタンパク質を発見した。

生命科学や合成生物学の分野において、高い親和性と高い特異性を兼ね備えた低分子結合タンパク質の設計は、バイオセンシングや分子スイッチを実現するための重要な課題であり続けてきた。従来、このアプローチは主に天然タンパク質のスクリーニングと改変、あるいは既存のタンパク質骨格に基づく物理的モデリング設計に依存しており、汎用性と拡張性に限界があった。
これを考慮して、韓国科学技術院(KAIST)生物科学科の研究チームは、深層学習を用いたタンパク質構造生成および配列設計手法を用いて、NTF2様フォールドをコアとなる「普遍的な骨格」として利用し、多様な低分子結合タンパク質を新規に設計した。さらに、研究者らはこれを化学誘導二量体化(CID)に類似したセンサーへと応用した。ストレスホルモンであるコルチゾールを選択的に認識できるタンパク質の設計に成功し、それに基づいた人工知能バイオセンサーを開発した。この事例は、タンパク質設計そのものの枠を超え、実用的な測定可能なセンサー技術へと前進し、タンパク質設計分野における長年の課題であった小分子認識の解決に貢献するものである。
関連する研究成果は、「設計されたタンパク質ファミリーを用いた低分子結合およびセンシング」と題され、Nature Communications誌に掲載された。
研究のハイライト:
人工知能を活用してタンパク質をゼロから(de novoで)設計し、それを機能性バイオセンサーに応用する。
従来の方法では主に天然のタンパク質を探したり、特定の機能を改変したりするのに対し、本研究では人工知能に基づく設計を用いて、望ましい機能を持つタンパク質を「カスタマイズ」する。
* この研究成果は、疾病診断、新薬開発、環境モニタリングなどの分野で幅広く応用できる。

用紙のアドレス:
https://www.nature.com/articles/s41467-026-70953-8
AIフロンティアに関するその他の論文:
https://hyper.ai/papers
データセット:NTF2バックボーンの構築
設計目標を達成するために、研究者らはまず、ファミリーレベルの「幻覚」法を用いてNTF2構造のセット(セット1:1,615個の骨格)を生成し、次にProteinMPNNを用いてこれらの骨格の配列を再設計した。AlphaFoldアルゴリズムを用いて、設計された構造に折り畳まれる可能性のあるタンパク質をスクリーニングした(セット2:3,230個のバックボーン)。さらに、Rosettaパラメータ化を用いてバックボーン構造を生成し、ProteinMPNNを用いて配列を設計した後、AlphaFoldを用いて構造を検証した(セット3:6,838個のバックボーン)。以下に示すとおりである。
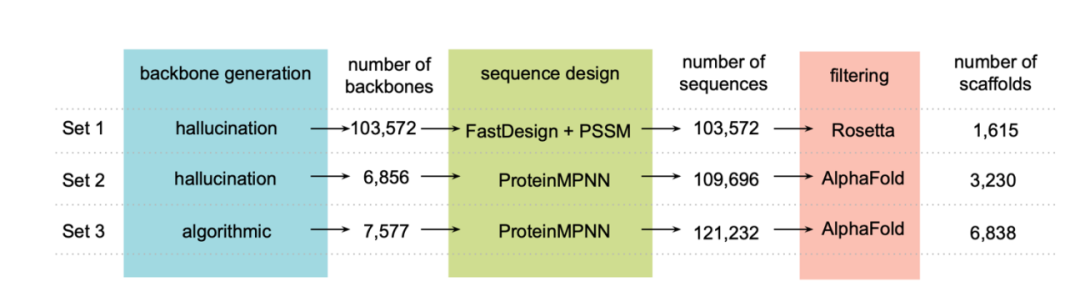
最終的に、スクリーニング後、研究者らは実験的特性評価のために、以下のものを含むエンコードオリゴヌクレオチドも入手した:630個のHCY結合タンパク質、1,661個のROC結合タンパク質、16,276個のWRF結合タンパク質、9,024個のAPX結合タンパク質、19,390個のIRI結合タンパク質、および7,573個のOHP結合タンパク質。
多様なポケット形状を持つNTF2タンパク質ファミリーの設計
NTF2フォールドは、3つのαヘリックスと湾曲した6本鎖βシートから構成される。これらの構造が一体となって、このフォールドファミリーに特徴的な大きな内部連結ポケットを形成する(下図参照)。
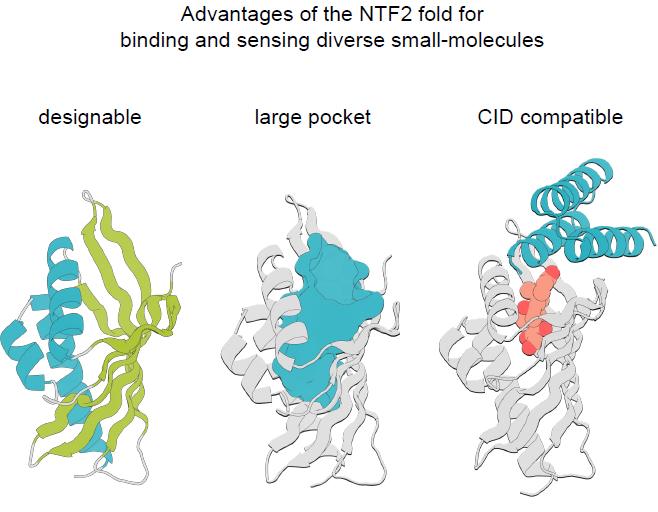
自然界におけるこの折り畳みの多様性は、主に長くて不規則な環状構造と独特な四次構造に起因しており、これらは複合ポケットの形状と機能に影響を与えている。本研究の目的は、多様なポケット形状を持ち、幅広い種類の小分子を収容できるNTF2タンパク質ファミリーを設計すると同時に、モジュール性と設計可能性を維持するためにループ領域を最小限に抑えることである。全体的な設計プロセスを以下の図に示します。
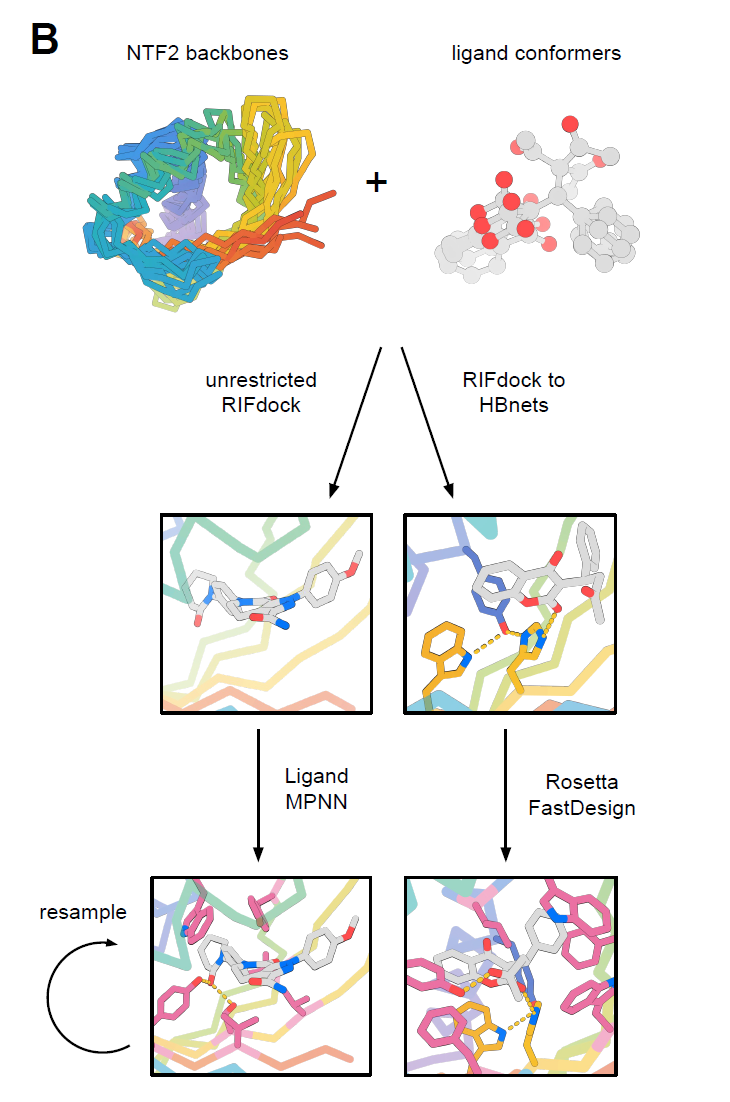
研究者らは、多様なポケット形状を持つ10,000個以上のNTF2設計タンパク質を取得した後、RIFdockを用いて、化学的性質と構造が異なる6つの小分子をこれらの骨格の中央ポケットに配置した。これらの小分子には、ストレスホルモンであるコルチゾール(HCY)、抗凝固剤であるワルファリン(WRF)、筋弛緩剤であるロクロニウム臭化物(ROC)、抗凝固剤であるアピキサバン(APX)、抗がん剤イリノテカン由来の抗腫瘍活性分子SN-38(IRI)、およびホルモンである17-α-ヒドロキシプロゲステロン(OHP)が含まれる。
極性界面の構築は、タンパク質設計、特に低分子結合タンパク質の設計において大きな課題である。そのためには、リガンドの極性官能基と相互作用するために、内部ポケットに極性残基を導入すると同時に、タンパク質全体の安定性を維持する必要がある。この課題に対処するため、研究者らは2つの戦略を採用した。
方法1(RIFdockからHBNetsへ)
研究者らは、HCY、WRF、ROC、APX、およびIRIを1つの骨格に組み込み、HBNet残基を介した少なくとも1つのタンパク質-小分子相互作用を必須とした。次に、天然配列をガイドとしたRosetta設計を用いて設計を最適化した。この設計では、NTF2ファミリータンパク質から得られた位置特異的スコアリングマトリックスを使用して配列設計に偏りを持たせた。
方法2(制限なしRIFdock)
OHP、APX、およびIRIは、制約なしRIFdockを使用してセット2および3のバックボーンに配置され、配列設計はLigandMPNNを使用して実行されました。LigandMPNNは、タンパク質-小分子複合体データで特別にトレーニングされたProteinMPNNのバリアントであり、設計プロセス中にリガンドの存在を明示的に考慮することができます。
研究者らは、設計結果をスクリーニングする際に、Rosettaを使用してタンパク質とリガンド間の水素結合の数、結合エネルギー(ddG)、および接触分子表面積(CMS)を計算しました。方法2では、単一配列のAlphaFold予測結果を組み合わせて、標的フォールド構造と結合部位を同時に再現できる設計をスクリーニングしました(下図参照)。
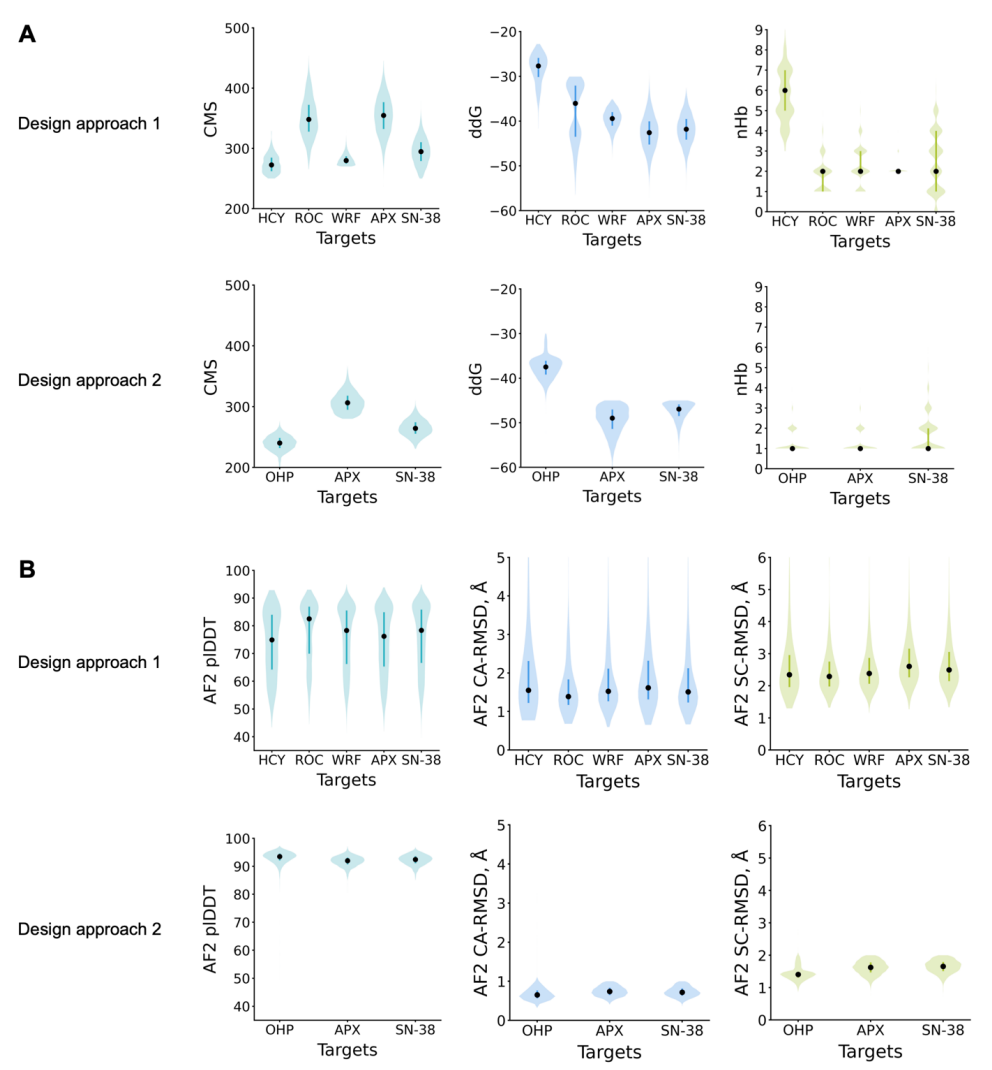
成果紹介:NTF2をベースとした低分子結合タンパク質はバイオセンサーに応用可能
研究者たちは、本研究で提案された設計戦略の有効性を検証するために、一連の実験を設計した。
結合タンパク質の設計と構造特性評価
設計した低分子結合タンパク質の精度を検証するため、2つのタンパク質-リガンド複合体の結晶構造を解析した。すなわち、コルチゾール結合タンパク質hcy129とアピキサバン結合タンパク質apx1049である。具体的には、hcy129はProteinMPNNを用いて表面を再設計し、結晶性を向上させた結果、コルチゾール複合体との1.5 Åの高解像度構造を首尾よく得ることができた。構造アライメントの結果、全体の折り畳みは設計モデルと非常に一致しており、Cα RMSDは1.1 Åであった(下図A)。重要な水素結合残基とリガンドのコンフォメーションも正確に一致しており(下図B)、事前に構築した水素結合ネットワーク(HBNet)が極性相互作用の精密な設計を効果的に実現したことが示された。
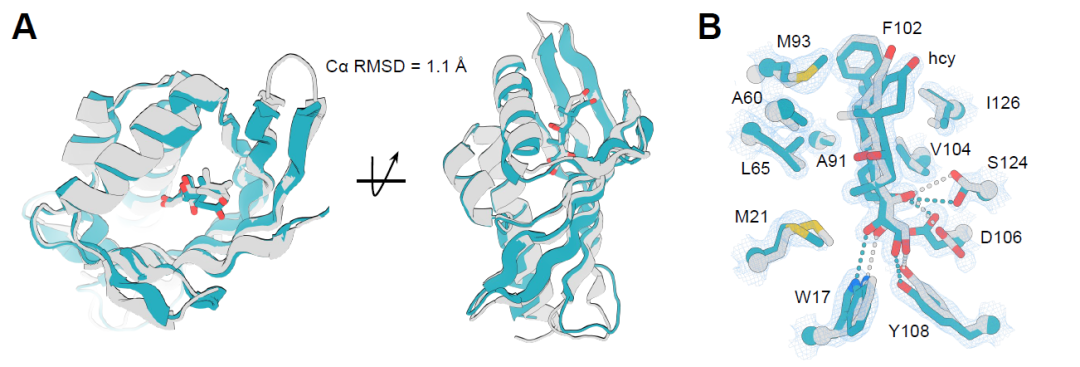
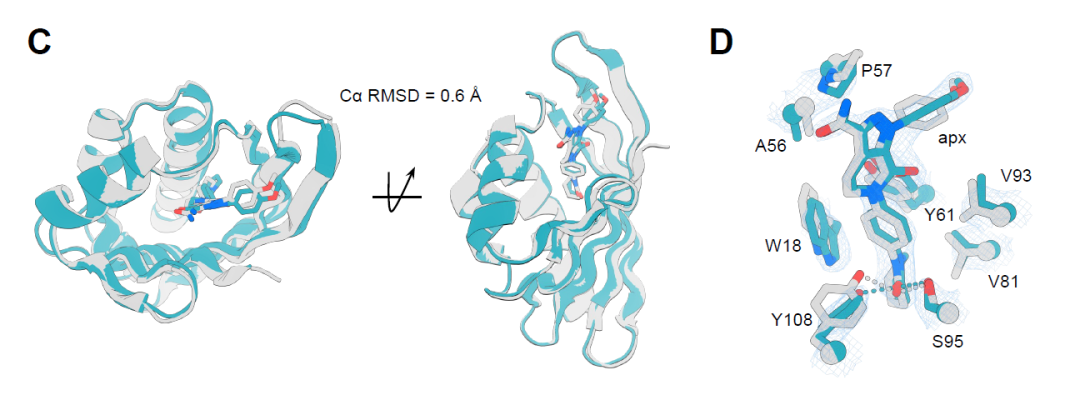
一方、apx1049-アピキサバン複合体の結晶構造は2.1 Åの分解能を持ち、設計モデルとの整合性が高く、113残基にわたるCα RMSDはわずか0.6 Åである(下図C)。タンパク質とリガンドの相互作用は、芳香族残基間の重要な水素結合やπ-πスタッキング相互作用を含め、設計をほぼ完全に再現しており(下図D)、リガンドのコンフォメーションを安定化させ、形状相補性の高い結合ポケットを形成している。これらの結果は、この設計戦略が原子スケールで高精度のタンパク質-リガンド界面構築を実現できることを示している。
結合タンパク質の特異性評価の設計
設計したタンパク質の特異性を評価するため、本研究では、非特異的な結合能を持つアルブミンを対照として用い、6種類の結合タンパク質と6種類のリガンドを系統的に試験した。その結果、hcy129.1、iri807.1、apx1049などの高親和性タンパク質は、それぞれの標的に結合する際に高い特異性を示した一方、アルブミンはほとんどのリガンドにほとんど結合せず、設計戦略の有効性が実証された。
さらに、ワルファリン(WRF)システムでは、アルブミン(KD約5.0μM)の結合親和性は、設計されたタンパク質wrf1071(KD約1.1μM)のそれと類似しており、高度に疎水性のリガンドへの非特異的結合が依然として課題であることを示している。
全体として、この方法は認識において一定の高い特異性を達成しているが、構造的に類似した分子を識別し、疎水性リガンドに対する選択性を向上させるためには、さらなる最適化の余地がまだ残されている。
バイオセンサーの構築(コルチゾール誘導ヘテロダイマーの設計と特性評価)
コルチゾールは通常、生理学的サンプル中に低ナノモル濃度で存在しますが、血漿コルチゾール濃度が38 nMを超えると、クッシング症候群などの疾患の診断基準として使用できます。バイオセンシングにおけるhcy129のコルチゾールに対する結合親和性を向上させるため、研究者らは、一点飽和変異(SSM)実験でスクリーニングされた好ましい変異に基づいて、組み合わせ変異体ライブラリーを構築しました。スクリーニングは酵母ディスプレイを使用して行われ、下の図に示すように、結合親和性の有意な増加が観察されました。
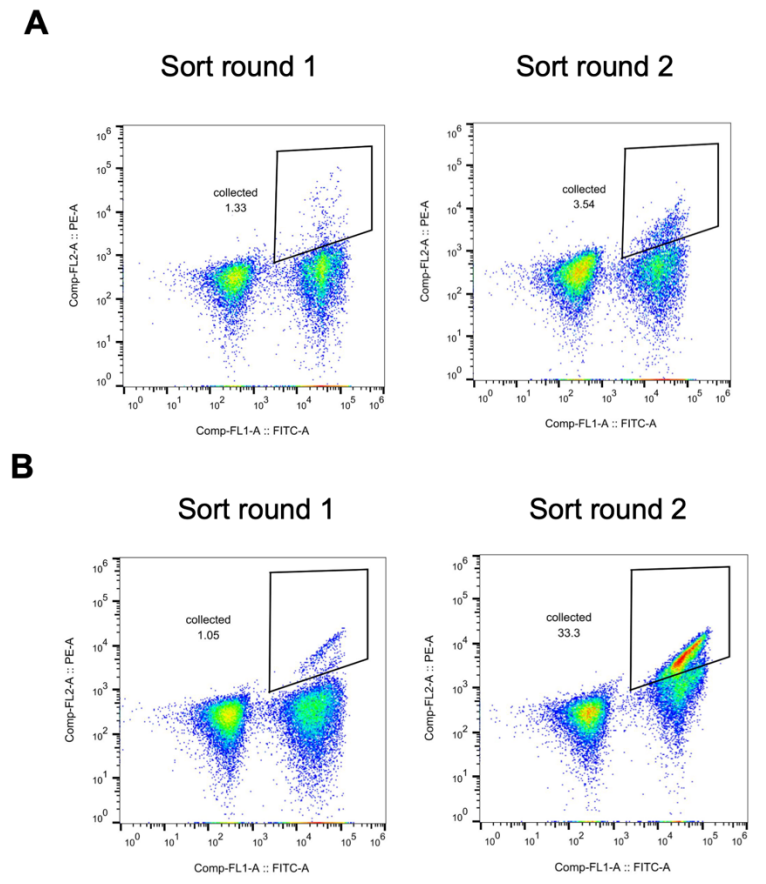
その後、研究者らはライブラリーから最適な変異体を選別し、大腸菌で発現させ、等温滴定カロリメトリー(ITC)を用いて特性評価を行った。この変異体hcy129.1のKD値は68 nMで、元の設計値より31倍高かった(下の図C)。構造解析の結果、親和性の向上は主にコルチゾールとの疎水性相互作用の強化に起因することが示された(下の図D)。
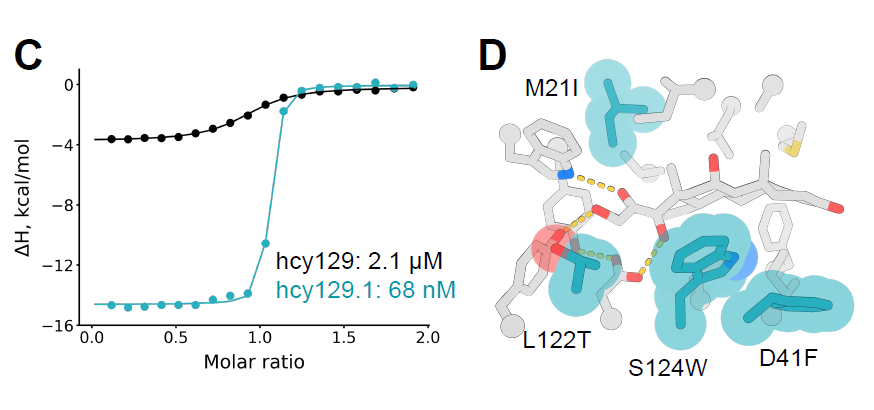
この基礎の上に、本研究ではさらにコルチゾール依存性ヘテロ二量体システムを設計した。hcy129.1の構造を改変し、小さなタンパク質骨格を導入することで、RIFdock、Rosetta、ProteinMPNNなどの手法を用いて計算設計とスクリーニングを行った。最終的に、hcy129.1およびコルチゾールと三元複合体を形成できる小さなタンパク質、miniH11が得られた。
実験の結果、このシステムはコルチゾールが存在する場合にのみ安定な複合体を形成することが示された。さらに、このシステムをNanoBiTルシフェラーゼシステムと融合させてコルチゾールセンシングを実現したところ、EC50値は約72 nM(下図H参照)となり、結合親和性と一致することから、設計の有効性が検証された。同時に、コルチゾールが存在しない場合、システムの親和性は著しく低下し、二量体化プロセスが良好なリガンド依存性を示すことが示された。
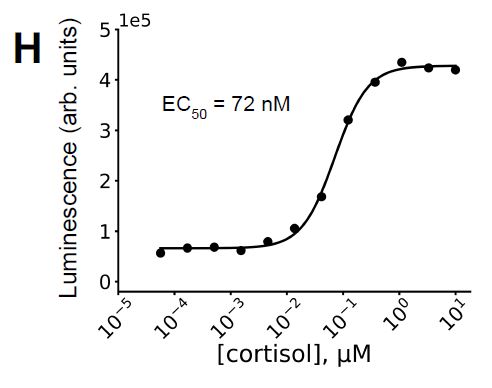
等モル濃度(200 nM)のhcy129.1_CID-SmBiTとminiH11-LgBiTの系において、コルチゾール依存性の発光応答曲線は…
全体、本研究は、NTF2をベースとした低分子結合タンパク質をさらに改良することで、機能的なバイオセンサーへと進化させることができることを示している。
結論
総じて、本研究は低分子結合タンパク質のde novo設計のための新しい道筋を提供する。人工知能モデルを用いてタンパク質とリガンドの相互作用を原子レベルで正確に特徴づけることで、「天然タンパク質の発見や改変」から「ニーズに応じた機能性タンパク質のカスタマイズ」へと転換し、効果的な実験的検証を完了させる。
これはタンパク質設計能力の飛躍的な進歩を示すだけでなく、その応用範囲を大幅に拡大するものです。早期疾患診断におけるバイオマーカーの精密検出から、新薬開発における標的分子認識、環境モニタリングにおける汚染物質のリアルタイム検出まで、幅広い応用が期待されます。この技術が成熟するにつれ、特異性が高くプログラム可能なカスタマイズ可能なバイオセンサーは、生命科学と実世界への応用を結びつける重要な架け橋となるでしょう。
参考文献:
https://www.nature.com/articles/s41467-026-70953-8
https://phys.org/news/2026-04-ai-proteins-built-specific-compounds.html








