Command Palette
Search for a command to run...
تصميم جديد مدفوع بالذكاء الاصطناعي لبروتينات ربط الجزيئات الصغيرة المتنوعة: اكتشف فريق من كوريا الجنوبية بروتينًا يمكنه التعرف بشكل انتقائي على هرمونات التوتر.

في مجالي علوم الحياة والبيولوجيا التركيبية، لطالما شكّل تصميم بروتينات ربط الجزيئات الصغيرة ذات الألفة العالية والنوعية العالية تحديًا رئيسيًا لتحقيق الاستشعار الحيوي والمفاتيح الجزيئية. في الماضي، اعتمد هذا النهج بشكل أساسي على فحص وتعديل البروتينات الطبيعية، أو على تصميمات النمذجة الفيزيائية القائمة على الهياكل البروتينية الموجودة، الأمر الذي حدّ من التنوع وقابلية التوسع.
وفي ضوء ذلك،استخدم فريق بحثي من قسم العلوم البيولوجية في المعهد الكوري المتقدم للعلوم والتكنولوجيا (KAIST) أساليب توليد بنية البروتين وتصميم التسلسل المدفوعة بالتعلم العميق لتصميم بروتينات ربط الجزيئات الصغيرة المتنوعة من الصفر، باستخدام الطي الشبيه بـ NTF2 كـ "عمود فقري عالمي" أساسي.علاوة على ذلك، قاموا بتحويل هذا إلى مستشعر مشابه لتقنية التضاعف المحفز كيميائيًا (CID). نجح الباحثون في تصميم بروتين قادر على التعرف بشكل انتقائي على هرمون الكورتيزول، هرمون التوتر، وطوروا مستشعرًا حيويًا يعتمد على الذكاء الاصطناعي. يتجاوز هذا الإنجاز تصميم البروتينات بحد ذاته، إذ يتجه نحو تقنية استشعار قابلة للقياس عمليًا، ويحل التحدي القائم منذ زمن طويل والمتمثل في التعرف على الجزيئات الصغيرة في مجال تصميم البروتينات.
وقد نُشرت نتائج البحث ذات الصلة، بعنوان "ربط الجزيئات الصغيرة واستشعارها باستخدام عائلة بروتينية مصممة"، في مجلة Nature Communications.
أبرز الأبحاث:
* استخدام الذكاء الاصطناعي لتصميم البروتينات من الصفر (de novo) وتطبيقها على أجهزة الاستشعار الحيوية الوظيفية.
تتضمن الطرق التقليدية في المقام الأول إيجاد البروتينات الطبيعية أو تعديل وظائف معينة، بينما تستخدم هذه الدراسة التصميم القائم على الذكاء الاصطناعي "لتخصيص" البروتينات بالوظائف المطلوبة.
* يمكن تطبيق نتائج البحث على نطاق واسع في مجالات مثل تشخيص الأمراض، وتطوير الأدوية الجديدة، والرصد البيئي.

عنوان الورقة:
https://www.nature.com/articles/s41467-026-70953-8
مزيد من أوراق البحث الرائدة في مجال الذكاء الاصطناعي:
https://hyper.ai/papers
مجموعة البيانات: بناء العمود الفقري لـ NTF2
لتحقيق أهداف التصميم،قام الباحثون أولاً بإنشاء مجموعة من هياكل NTF2 (المجموعة 1: 1615 هيكلًا أساسيًا) باستخدام طريقة "الهلوسة" على مستوى العائلة، ثم استخدموا ProteinMPNN لإعادة تصميم تسلسلات هذه الهياكل الأساسية.استُخدمت خوارزمية AlphaFold لفحص البروتينات التي يمكن أن تتخذ البنى المصممة (المجموعة 2: 3230 هيكلًا أساسيًا). علاوة على ذلك، استُخدمت معلمات Rosetta لإنشاء الهيكل الأساسي، واستُخدمت ProteinMPNN لتصميم التسلسل، ثم استُخدمت AlphaFold للتحقق من صحة البنية (المجموعة 3: 6838 هيكلًا أساسيًا)، كما هو موضح في الشكل أدناه:
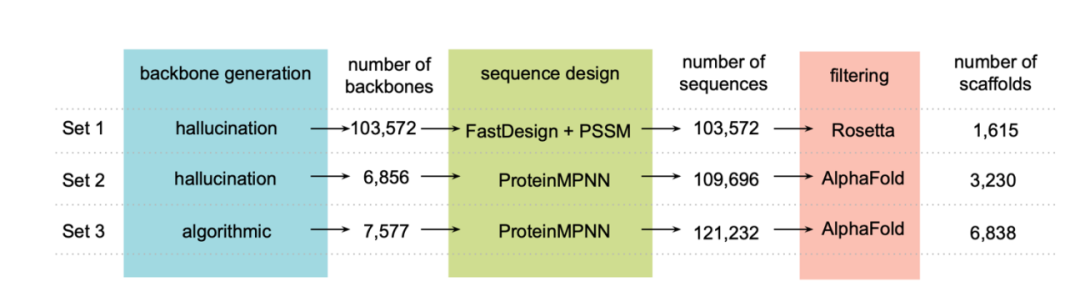
في النهاية، وبعد الفحص، حصل الباحثون أيضًا على النيوكليوتيدات المشفرة للتوصيف التجريبي، بما في ذلك: 630 بروتينًا مرتبطًا بـ HCY، و1661 بروتينًا مرتبطًا بـ ROC، و16276 بروتينًا مرتبطًا بـ WRF، و9024 بروتينًا مرتبطًا بـ APX، و19390 بروتينًا مرتبطًا بـ IRI، و7573 بروتينًا مرتبطًا بـ OHP.
تصميم عائلة بروتين NTF2 بأشكال هندسية متنوعة للجيب
يتكون طي NTF2 من ثلاثة حلزونات ألفا وصفيحة بيتا منحنية مكونة من ستة خيوط. تشكل هذه البنى معًا الجيب الداخلي الكبير الرابط الذي يميز هذه العائلة من الطيات، كما هو موضح في الشكل أدناه:
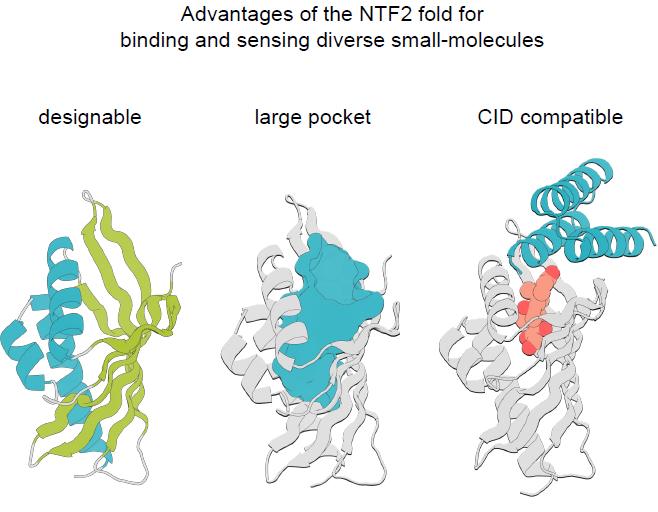
ينبع تنوع هذا الطي في الطبيعة بشكل أساسي من الحلقات الطويلة وغير المنتظمة والبنية الرباعية الفريدة، وكلاهما يؤثر على هندسة ووظيفة الجيب المدمج.الهدف من هذه الدراسة هو تصميم عائلة من بروتينات NTF2 ذات أشكال هندسية متنوعة للجيب لاستيعاب مجموعة واسعة من الجزيئات الصغيرة، مع تقليل مناطق الحلقة للحفاظ على نمطيتها وقابليتها للتصميم.يوضح الرسم التخطيطي التالي عملية التصميم الشاملة:
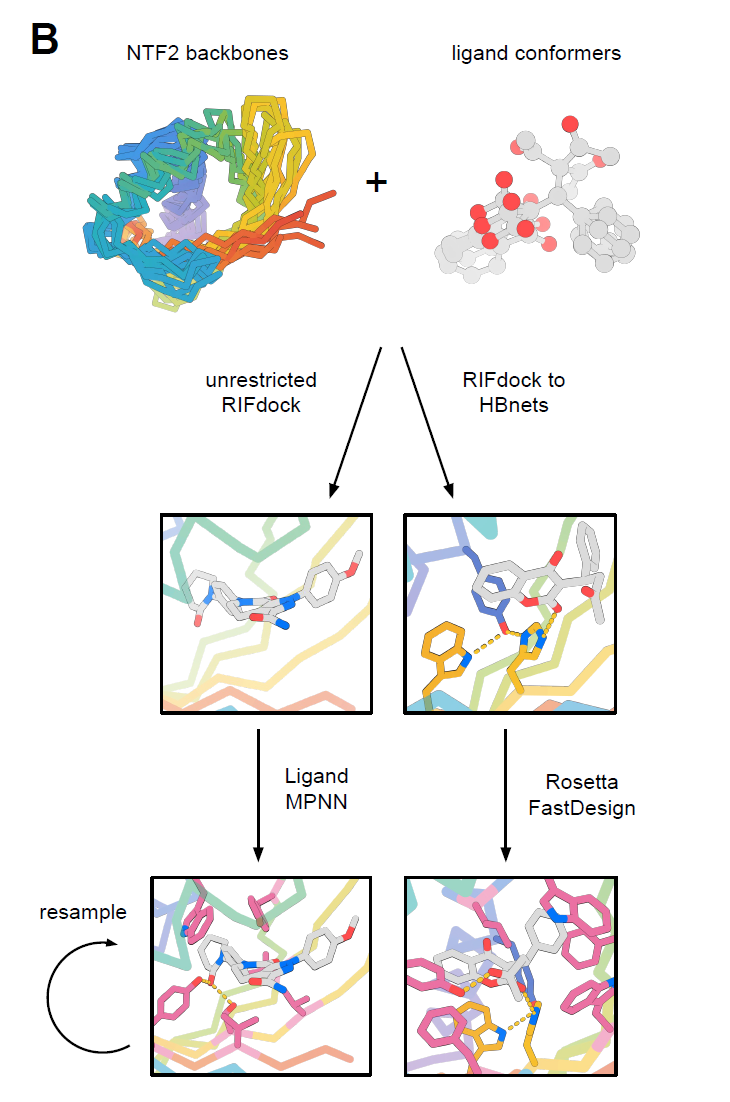
بعد الحصول على أكثر من 10000 بروتين مصمم بتقنية NTF2 ذات أشكال هندسية متنوعة للجيوب، استخدم الباحثون برنامج RIFdock لوضع ستة جزيئات صغيرة، تختلف في خصائصها الكيميائية وبنيتها، في الجيوب المركزية لهذه البروتينات. وشملت هذه الجزيئات الصغيرة هرمون الكورتيزول (HCY)، ومضاد التخثر الوارفارين (WRF)، ومرخي العضلات روكورونيوم بروميد (ROC)، ومضاد التخثر أبيكسابان (APX)، والجزيء النشط المضاد للأورام SN-38 (IRI) المشتق من دواء إيرينوتيكان المضاد للسرطان، وهرمون 17-ألفا-هيدروكسي بروجستيرون (OHP).
يُعدّ بناء واجهات قطبية تحديًا كبيرًا في تصميم البروتينات، لا سيما البروتينات التي ترتبط بالجزيئات الصغيرة. ويتطلب ذلك إدخال بقايا قطبية في الجيب الداخلي للبروتين للتفاعل مع المجموعات الوظيفية القطبية للروابط، مع الحفاظ في الوقت نفسه على استقرار البروتين بشكل عام. ولمعالجة هذا التحدي، استخدم الباحثون استراتيجيتين:
الطريقة الأولى (RIFdock إلى HBNets)
قام الباحثون بربط بروتينات HCY وWRF وROC وAPX وIRI بالهيكل الأساسي، واشترطوا وجود تفاعل واحد على الأقل بين البروتين والجزيء الصغير بوساطة بقايا HBNet. ثم قاموا بتحسين التصميم باستخدام برنامج Rosetta، الذي يعتمد على التسلسلات الطبيعية، ويستخدم مصفوفة تسجيل خاصة بالموقع مستمدة من بروتينات عائلة NTF2 لتوجيه تصميم التسلسل.
الطريقة الثانية (RIFdock غير المقيد)
تم دمج OHP وAPX وIRI في الهياكل الأساسية للمجموعتين 2 و3 باستخدام برنامج RIFdock غير المقيد، وتم تصميم التسلسل باستخدام LigandMPNN. يُعد LigandMPNN نسخة معدلة من ProteinMPNN، تم تدريبها خصيصًا على بيانات معقدات البروتين والجزيئات الصغيرة، مما يتيح مراعاة وجود الليجاند بشكل صريح أثناء عملية التصميم.
عند فحص نتائج التصميم، استخدم الباحثون Rosetta لحساب عدد الروابط الهيدروجينية بين البروتين والرابط، وطاقة الربط (ddG)، ومساحة سطح التلامس الجزيئي (CMS)؛ بالنسبة للطريقة 2، قاموا أيضًا بدمج نتائج التنبؤ بتسلسل AlphaFold الفردي لفحص التصاميم التي يمكنها إعادة إنتاج بنية الطي المستهدفة وموقع الربط في وقت واحد (انظر الشكل أدناه).
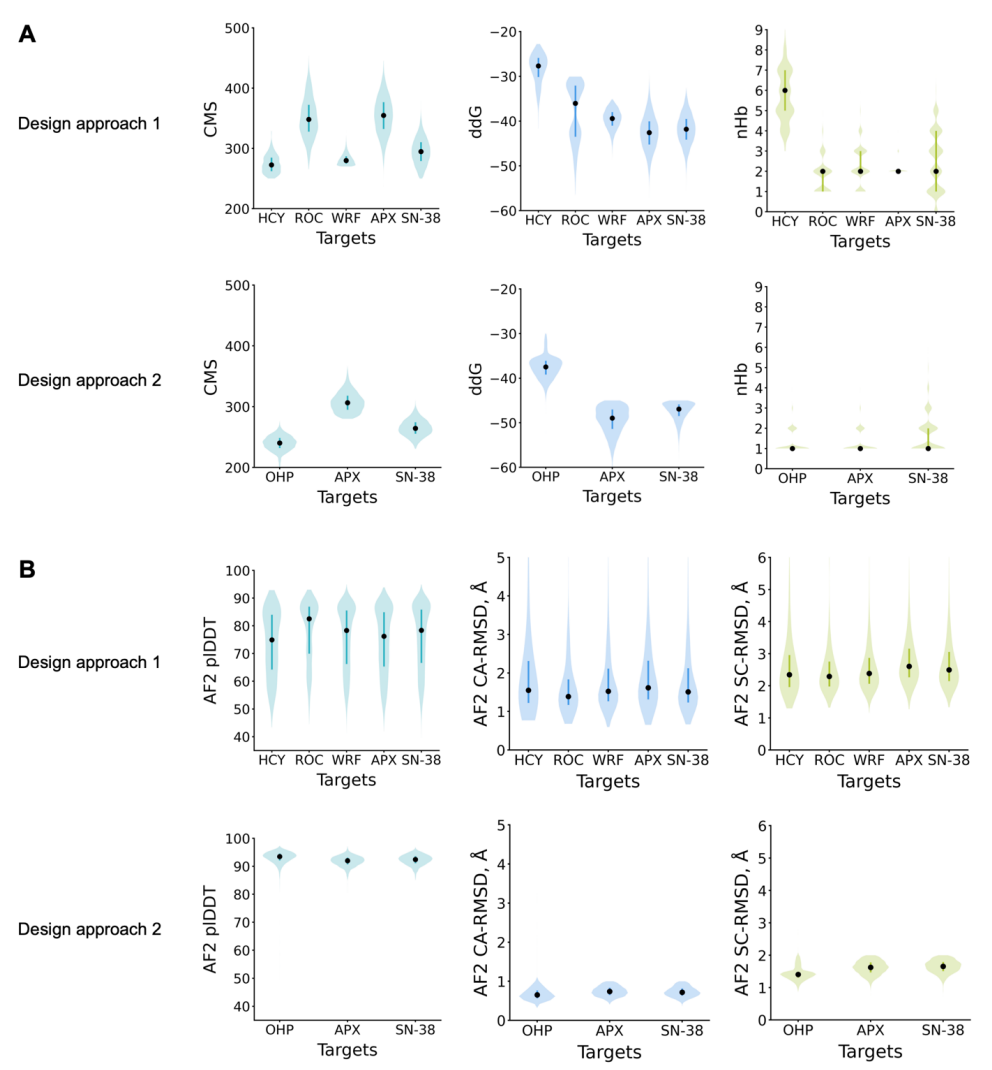
عرض النتائج: يمكن تطبيق البروتينات الرابطة للجزيئات الصغيرة القائمة على NTF2 في أجهزة الاستشعار البيولوجية
قام الباحثون بتصميم سلسلة من التجارب للتحقق من فعالية استراتيجية التصميم المقترحة في هذه الدراسة:
تصميم وتوصيف بنيوي للبروتينات الرابطة
للتحقق من دقة البروتينات المصممة لربط الجزيئات الصغيرة، تم تحديد البنية البلورية لمركبين من البروتين والربيطة: بروتين ربط الكورتيزول hcy129 وبروتين ربط أبيكسابان apx1049. وبالتحديد، خضع hcy129 لإعادة تصميم سطحية باستخدام ProteinMPNN لتحسين التبلور، مما أدى إلى الحصول بنجاح على بنيته عالية الدقة (1.5 أنغستروم) مع مركب الكورتيزول. أظهرت المحاذاة البنيوية أن الطي العام كان متوافقًا إلى حد كبير مع نموذج التصميم، بانحراف معياري جذري متوسط (RMSD) لذرات الكربون ألفا (Cα) قدره 1.1 أنغستروم (الشكل أ أدناه). كما تطابقت بقايا الروابط الهيدروجينية الرئيسية وتكوينات الربيطة بدقة (الشكل ب أدناه)، مما يشير إلى أن شبكة الروابط الهيدروجينية (HBNet) المُنشأة مسبقًا قد حققت تصميمًا دقيقًا للتفاعلات القطبية.
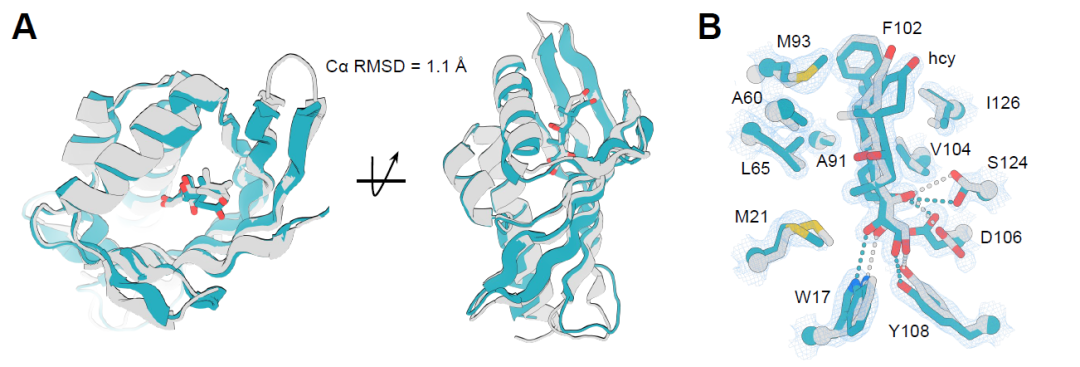
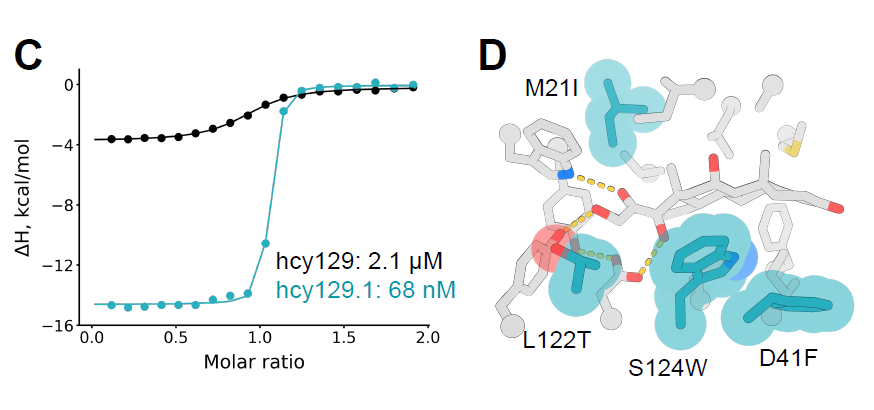
من جهة أخرى، يتميز التركيب البلوري لمركب apx1049-apixaban بدقة 2.1 أنغستروم، مما يُظهر توافقًا أكبر مع نموذج التصميم، وانحرافًا معياريًا متوسطًا (RMSD) لذرات الكربون ألفا (Cα) لا يتجاوز 0.6 أنغستروم على مدى 113 حمضًا أمينيًا (الشكل C أدناه). وتُحاكي تفاعلات البروتين مع الرابطة التصميم بدقة متناهية، بما في ذلك الروابط الهيدروجينية الرئيسية وتفاعلات التراص π–π بين الأحماض الأمينية العطرية (الشكل D أدناه)، مما يُساهم في استقرار هيئة الرابطة وتكوين جيب ارتباط مُتكامل الشكل. تُبرهن هذه النتائج على أن استراتيجية التصميم هذه تُحقق بناءً عالي الدقة لواجهة البروتين-الرابطة على المستوى الذري.
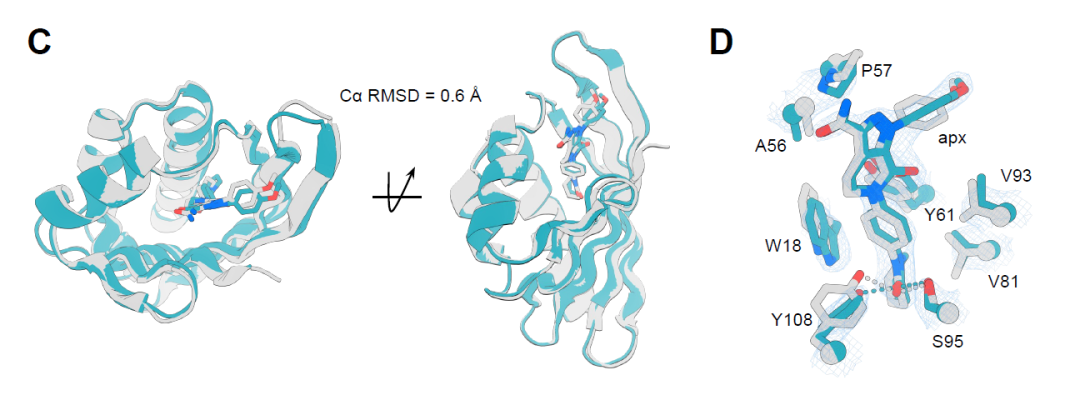
تصميم تقييم الخصوصية لبروتينات الربط
لتقييم خصوصية البروتينات المصممة، اختبرت الدراسة بشكل منهجي ستة بروتينات رابطة مع ستة ليجاندات، باستخدام الألبومين، الذي يتميز بقدرة ارتباط غير نوعية، كعنصر تحكم. أظهرت النتائج أن البروتينات ذات الألفة العالية، مثل hcy129.1 و iri807.1 و apx1049، أظهرت خصوصية جيدة عند ارتباطها بأهدافها، بينما لم يُظهر الألبومين أي ارتباط تقريبًا بمعظم الليجاندات، مما يؤكد فعالية استراتيجية التصميم.
علاوة على ذلك، في نظام الوارفارين (WRF)، فإن تقارب ارتباط الألبومين (KD حوالي 5.0 ميكرومتر) به مشابه لتقارب ارتباط البروتين المصمم wrf1071 (KD حوالي 1.1 ميكرومتر)، مما يشير إلى أن الارتباط غير المحدد بالروابط شديدة الكراهية للماء لا يزال يمثل تحديًا.
بشكل عام، حققت هذه الطريقة درجة معينة من الخصوصية العالية في التعرف، ولكن لا يزال هناك مجال لمزيد من التحسين في تمييز الجزيئات المتشابهة هيكليًا وتحسين الانتقائية للروابط الكارهة للماء.
بناء المستشعرات الحيوية (تصميم وتوصيف ثنائيات غير متجانسة ناتجة عن الكورتيزول)
يوجد الكورتيزول عادةً في العينات الفيزيولوجية بتراكيز نانومولية منخفضة، ولكن يمكن استخدام مستويات الكورتيزول في البلازما التي تتجاوز 38 نانومول كمعيار تشخيصي لأمراض مثل متلازمة كوشينغ. ولتحسين قدرة بروتين hcy129 على الارتباط بالكورتيزول لأغراض الاستشعار الحيوي، أنشأ الباحثون مكتبة طفرات تركيبية بناءً على الطفرات المواتية التي تم فحصها في تجارب طفرة التشبع أحادية النقطة (SSM). أُجري الفحص باستخدام تقنية عرض الخميرة، ولوحظت زيادة ملحوظة في قدرة الارتباط، كما هو موضح في الشكل أدناه.
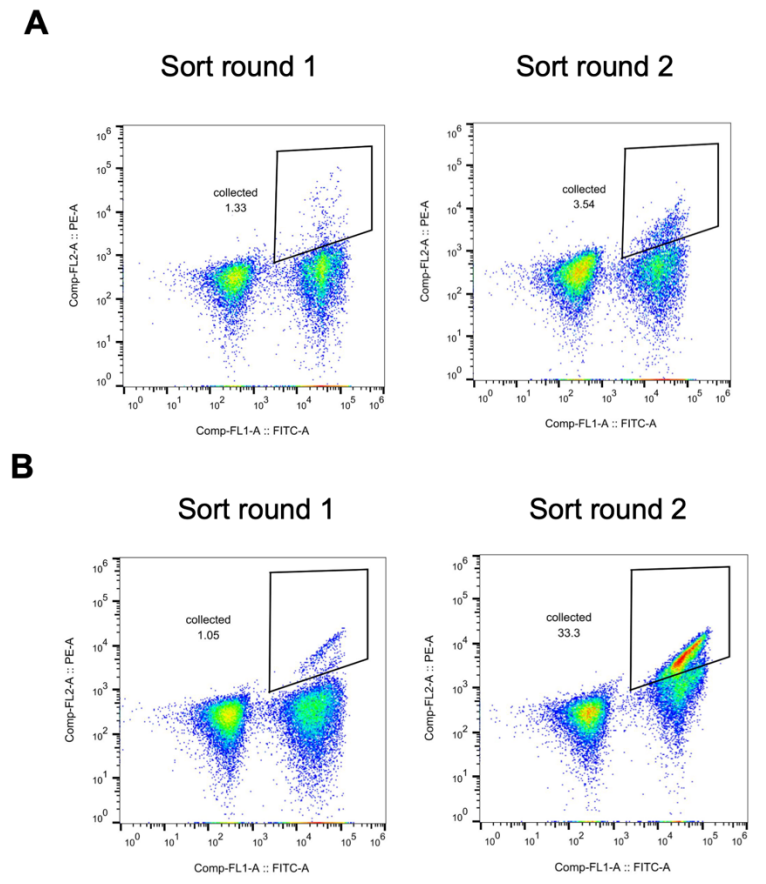
بعد ذلك، قام الباحثون بفحص المتغير الأمثل من المكتبة، وعبروا عنه في بكتيريا الإشريكية القولونية، ودرسوا خصائصه باستخدام قياس السعرات الحرارية بالمعايرة متساوية الحرارة (ITC). بلغت قيمة ثابت التفكك (KD) لهذا المتغير hcy129.1 68 نانومتر، أي أعلى بـ 31 ضعفًا من التصميم الأصلي (الشكل C أدناه)؛ وأظهر التحليل البنيوي أن زيادة الألفة ناتجة بشكل أساسي عن تفاعل كاره للماء أقوى مع الكورتيزول (الشكل D أدناه).
انطلاقًا من هذا الأساس، صممت الدراسة نظامًا ثنائيًا غير متجانس يعتمد على الكورتيزول. ومن خلال تعديل بنية hcy129.1 وإضافة هيكل بروتيني صغير، أُجري تصميم حاسوبي وفحص باستخدام طرق مثل RIFdock وRosetta وProteinMPNN. وفي النهاية، تم الحصول على بروتين صغير، miniH11، قادر على تكوين مركب ثلاثي مع hcy129.1 والكورتيزول.
أظهرت التجارب أن النظام لا يُشكّل مُركّبًا مُستقرًا إلا في وجود الكورتيزول. علاوة على ذلك، دُمج النظام مع نظام لوسيفيراز NanoBiT لاستشعار الكورتيزول، حيث تم الكشف عن قيمة EC50 تُقارب 72 نانومتر (الشكل H أدناه)، وهو ما يتوافق مع قوة الارتباط، مما يُؤكد فعالية التصميم. في الوقت نفسه، انخفضت قوة ارتباط النظام بشكل ملحوظ في غياب الكورتيزول، مما يُشير إلى أن عملية التضاعف تُظهر اعتمادًا جيدًا على الربيطة.
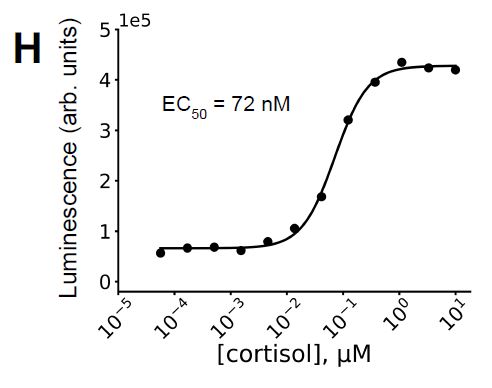
في نظام hcy129.1_CID-SmBiT و miniH11-LgBiT متساوي المولات (200 نانومتر)، منحنيات استجابة التألق المعتمدة على الكورتيزول...
إجمالي،يوضح هذا العمل أنه يمكن هندسة البروتينات الرابطة للجزيئات الصغيرة القائمة على NTF2 بشكل أكبر لتصبح أجهزة استشعار حيوية وظيفية.
خاتمة
بشكل عام، توفر هذه الدراسة مسارًا جديدًا للتصميم الجديد للبروتينات الرابطة للجزيئات الصغيرة: من خلال استخدام نماذج الذكاء الاصطناعي لتوصيف تفاعلات البروتين والرابط بدقة على المستوى الذري، فإنها تحقق تحولًا من "اكتشاف أو تعديل البروتينات الطبيعية" إلى "تخصيص البروتينات الوظيفية حسب الطلب"، وتكمل التحقق الفعال على المستوى التجريبي.
لا يُمثل هذا إنجازًا كبيرًا في مجال تصميم البروتينات فحسب، بل يُوسع أيضًا نطاق تطبيقاتها بشكلٍ ملحوظ، بدءًا من الكشف الدقيق عن المؤشرات الحيوية في التشخيص المبكر للأمراض، وصولًا إلى التعرف الجزيئي المُستهدف في تطوير الأدوية الجديدة، والرصد الفوري للملوثات في المراقبة البيئية. ومع نضوج هذه التقنية، يُتوقع أن تُصبح أجهزة الاستشعار الحيوية المُخصصة عالية التخصص والقابلة للبرمجة جسرًا حيويًا يربط علوم الحياة بالتطبيقات العملية.
مراجع:
https://www.nature.com/articles/s41467-026-70953-8
https://phys.org/news/2026-04-ai-proteins-built-specific-compounds.html