Command Palette
Search for a command to run...
من خلال دمج البيانات المتعلقة بتسلسلات البروتين والهياكل ثلاثية الأبعاد والخصائص الوظيفية، قام فريق ألماني ببناء "نظرة بانورامية" لإنزيمات E3 Ubiquitin Ligases البشرية استنادًا إلى التعلم المتري.
في الكائنات الحية، يُعدّ التحلل والتجديد المنتظم للبروتينات الخلوية أمرًا بالغ الأهمية للحفاظ على توازن البروتينات. ويُعتبر نظام اليوبيكويتين-بروتيازوم (UPS) آلية أساسية لتنظيم نقل الإشارات وتحلل البروتينات. ضمن هذا النظام، تُعدّ إنزيمات E3 ليغاز اليوبيكويتين، كوحدات تحفيزية رئيسية، مسؤولة عن التعرّف على ركائز محددة وتحفيز وسم اليوبيكويتين، وبالتالي تنظيم تحلل البروتينات وتحديد موقعها وحالتها الوظيفية. علاوة على ذلك، تُنظّم إنزيمات E3 ليغاز أيضًا مسارات المناعة والالتهاب. ونظرًا لتعبيرها النسيجي النوعي وارتباطها بمتلازمات النمو والتمثيل الغذائي (بما في ذلك تطور السرطان)، فقد أصبحت إنزيمات E3 ليغاز أهدافًا دوائية واعدة، لا سيما للأهداف التي كان من الصعب استهدافها دوائيًا في السابق.
بالمقارنة مع إنزيمات E1 (حوالي 10 أنواع) وE2 (حوالي 50 نوعًا)، تم تحديد عدد كبير من إنزيمات E3 ليغاز البشرية (حوالي 600 نوع). ومع ذلك، لا تزال العديد من إنزيمات E3 ليغاز البشرية غير موصوفة بشكل كامل، ولا يزال عدد كبير منها افتراضيًا أو مجهولًا. حتى الآن،أظهرت إنزيمات E3 ليغاز المدروسة تباينًا كبيرًا.وهذا ما يجعلها واحدة من أكثر فئات الإنزيمات تنوعًا، مما يُشكل عائقًا أمام التعرف على الأنماط وإجراء البحوث واسعة النطاق. لذا، يُعدّ التوصيف والتحليل الدقيقان لجينوم إنزيمات E3 ليغاز البشرية - أي المجموعة الكاملة من إنزيمات E3 ليغاز المشفرة في الجينوم البشري - أمرًا بالغ الأهمية لفهم وظائفها البيولوجية فهمًا شاملًا.
وفي هذا السياق،قام فريق بحثي من جامعة غوته في ألمانيا بتصنيف "الليغوم البشري E3".وهي تدمج البيانات متعددة المستويات، بما في ذلك تسلسلات البروتين، وتكوين النطاق، والبنية ثلاثية الأبعاد، والوظيفة، وأنماط التعبير.تعتمد طريقة التصنيف الخاصة بالفريق على نموذج التعلم المتري وتستخدم إطارًا هرميًا ضعيف الإشراف لالتقاط العلاقات الحقيقية بين عائلة E3 وعائلاتها الفرعية.يتوسع هذا النهج في التصنيف التقليدي لإنزيمات E3 (فئات RING و HECT و RBR)، ويميز بين المركبات متعددة الوحدات الفرعية والإنزيمات أحادية الوحدة، ويرسم خريطة لإنزيمات E3 على الركائز والأهداف الدوائية المحتملة.
وقد نُشرت نتائج البحث ذات الصلة، بعنوان "التصنيف متعدد المقاييس يفك شفرة تعقيد مجموعة E3 البشرية"، في مجلة Nature Communications.
أبرز الأبحاث:
* رسم خريطة لبنية المجال، والبنية ثلاثية الأبعاد، والوظيفة، وشبكة الركيزة، وتفاعلات الجزيئات الصغيرة لإنزيمات E3 ligases الموجودة في إطار تصنيفي لاكتساب رؤى عامة وخاصة بالعائلة.
* يغطي إطار التصنيف متعدد المقاييس الذي تم تطويره آليات E3 النموذجية وغير النموذجية، مما يوفر خارطة طريق كاملة لفهم المشهد البيولوجي الواسع لإنزيمات E3 ligases.
* يفتح آفاقاً جديدة لتطوير استراتيجيات التدخل الدوائي القائمة على شبكات الركيزة E3.

عنوان الورقة:
https://www.nature.com/articles/s41467-025-67450-9
تابع حسابنا الرسمي على WeChat وأجب بـ "E3 enzyme" في الخلفية للحصول على ملف PDF كامل.
مزيد من أوراق البحث الرائدة في مجال الذكاء الاصطناعي:
https://hyper.ai/papers
مجموعة البيانات: بناء بيانات إنزيم يوبيكويتين ليغاز E3 البشري
قام فريق البحث أولاً بدمج بيانات إنزيم يوبيكويتين ليغاز E3 البشري من ثمانية مصادر بيانات مستقلة.بالاستناد إلى التقارير المنشورة سابقًا وقواعد البيانات العامة (E3Net، UbiHub، UbiNet 2.0، UniProt، BioGRID، وغيرها)، تم تكوين مجموعة بيانات أولية تضم 1448 مدخلًا بروتينيًا. وتم استبعاد المدخلات المكررة والتي قد تكون نتائج إيجابية خاطئة من خلال المقارنة المتبادلة وتقييم اتساق البيانات من مصادر مختلفة. بعد ذلك، وباستخدام خصائص النطاقات التحفيزية RING وHECT وRBR التي يوفرها InterPro، تم فحص 462 من إنزيمات E3 ubiquitin ligase التحفيزية عالية الموثوقية، لتشكل بذلك الجينوم النهائي لإنزيمات E3 ligase البشرية.
في معقدات E3 متعددة الوحدات الفرعية (مثل ليغازات كولين-رينغ)، تعمل ثلاث وحدات فرعية متميزة وظيفيًا (بروتين السقالة، وبروتين الأبتامر، وبروتين المستقبل) معًا لتحديد موقع جزيئات E2~Ub على ركائز محددة. تُنظم بروتينات السقالة الكبيرة والصلبة والمركزية (مثل عائلة كولين، Cul1-Cul5) معقد الليغاز بأكمله من خلال الارتباط المتزامن بمواقع الالتحام لوحدة نطاق إصبع رينغ التحفيزية والأبتامر/المستقبل. يربط بروتين الأبتامر الوحدات، موصلًا وجه الالتحام الطرفي N لبروتين السقالة بمستقبلات الركيزة الفردية. يحدد بروتين المستقبل خصوصية الركيزة، حيث يتعرف مباشرةً على إشارات التحلل (ديغرونات) على الركيزة ويرتبط بها لتحديد الركائز التي ستخضع لعملية اليوبيكويتين (مثل Skp2 وKeap1 وVHL).قام فريق البحث بشكل مستقل بتصنيف وتصنيف ثلاث وحدات فرعية: 151 أبتامير، و106 مستقبلات، و8 بروتينات سقالة.كما استخدموا تفاعلات البروتين-البروتين (PPIs) لرسم خريطة ركائز E3 متعددة الوحدات الفرعية.
وفي وقت لاحق، في مرحلة فحص المجالات التحفيزية، استخدم الباحثون القدرة التحفيزية كمعيار أساسي لتصفية البروتينات المرشحة بدقة.باستخدام قواعد بيانات النطاقات مثل InterPro، حدد النظام النطاقات التحفيزية الرئيسية المرتبطة مباشرة بنشاط E3، بما في ذلك RING وHECT وRBR.لا تُحتفظ إلا بالبروتينات التي تحتوي صراحةً على هذه المجالات وتدعم وظيفتها في ربط اليوبيكويتين على المستويين التسلسلي والبنيوي، وذلك لبناء "إنزيم E3 المحفز" النهائي. وتؤدي هذه العملية إلى استبعاد البروتينات المساعدة التي تشارك فقط في التنظيم دون أن تمتلك قدرة تحفيزية مباشرة، مما يضمن التناسق الوظيفي لمجموعة E3 الأساسية.
إطار تصنيف متعدد المقاييس قائم على تعلم المقاييس
لفهم العلاقات المعقدة داخل جينوم إنزيم E3 ليغاز البشري،استخدم الباحثون أساليب التعلم الآلي لتعلم مقياس المسافة الناشئ.يُوضح الرسم التخطيطي التالي الإطار العام:
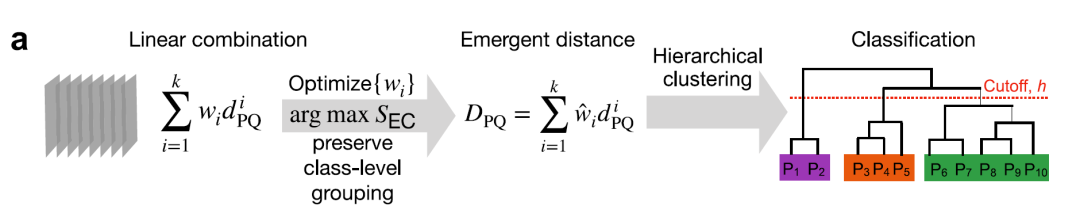
① قياس المسافة متعدد المقاييس
قام الباحثون بترميز العلاقات الزوجية بين إنزيمات E3 ligases عن طريق حساب 12 مسافة مختلفة.تغطي هذه المسافات مستويات حبيبية متعددة: التسلسل الأولي، وبنية المجال، والبنية الثلاثية، والوظيفة، والتوطين الخلوي، والتعبير عن خط الخلية/النسيج.يتم تحويل جميع مقاييس المسافة إلى الفترة [0,1] للمقارنة والدمج، كما هو موضح في الشكل أدناه:
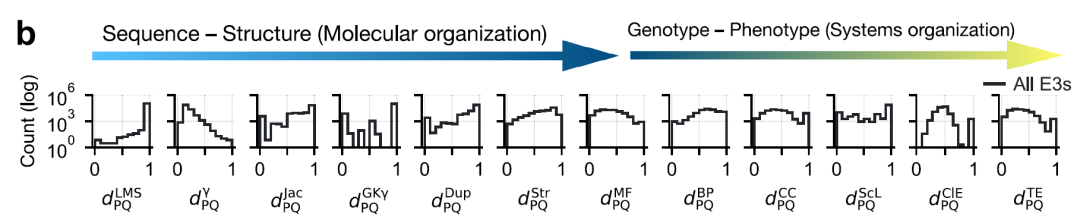
* مستوى التسلسل: تم استخدام مسافة درجة المطابقة المحلية (LMS) (بدون مطابقة زوجية) ومسافة γ القائمة على المحاذاة.
* على مستوى بنية المجال: تم حساب ثلاث مسافات - مسافة جاكارد، مسافة جودمان-كروسكال γ، ومسافة تكرار المجال.
* المستوى الهيكلي ثلاثي الأبعاد: باستخدام نموذج AlphaFold2 TM-score
* المستوى الوظيفي: يتم قياس المسافة الوظيفية بين البروتينات و P و Q باستخدام التشابه الدلالي لتعليقات GO، والتي تغطي ثلاثة أنطولوجيات: * الوظيفة الجزيئية (MF) والعملية البيولوجية (BP) والمكون الخلوي (CC).
* مسافة التوطين دون الخلوي
* مسافة التعبير المشترك بين الأنسجة وخطوط الخلايا
② تحسين المقاييس، والتجميع، والتمهيد، والتصنيف
يتم ترجيح المسافات الرئيسية الأربعة (γ، جاكارد، البنية، والوظيفة الجزيئية) ودمجها، مع تحسين الأوزان من خلال التعلم الخاضع للإشراف الضعيف ومؤشر تشابه مركز العنصر (SEC)، كما هو موضح في الشكل أدناه، للحصول على المؤشر المدمج الأمثل.
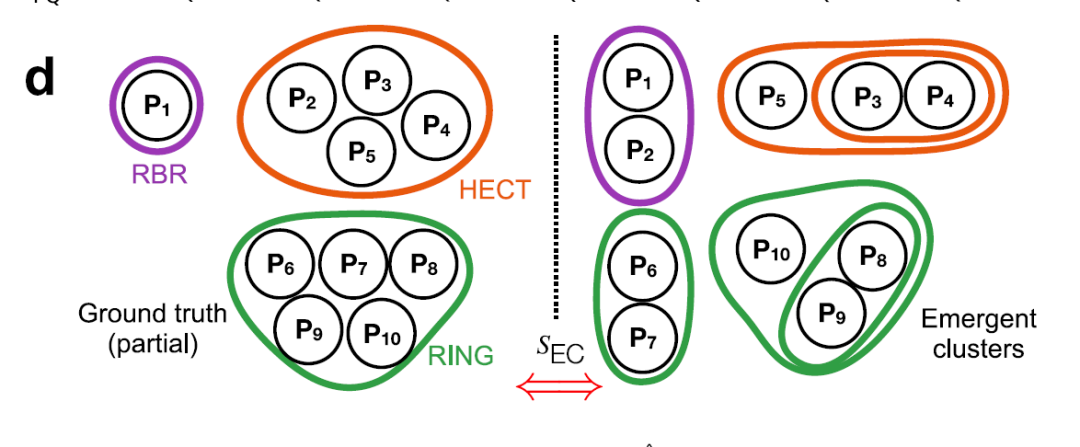
تم إجراء التجميع الهرمي باستخدام طريقة وارد للحد الأدنى من التباين.يتم حساب الدعم باستخدام طريقة إعادة التوزيع العشوائي (bootstrapping) لإنشاء مخطط التفرع النهائي E3. يتم الحصول على المجموعات الناشئة المثلى باستخدام عتبة تقطيع الشجرة h = 0.25، مما يؤدي إلى تقسيم مجموعات E3 البالغ عددها 462 مجموعة بشكل منهجي إلى 13 عائلة: 10 عائلات RING، وعائلتان HECT، وعائلة RBR واحدة، كما هو موضح في الشكل أدناه.
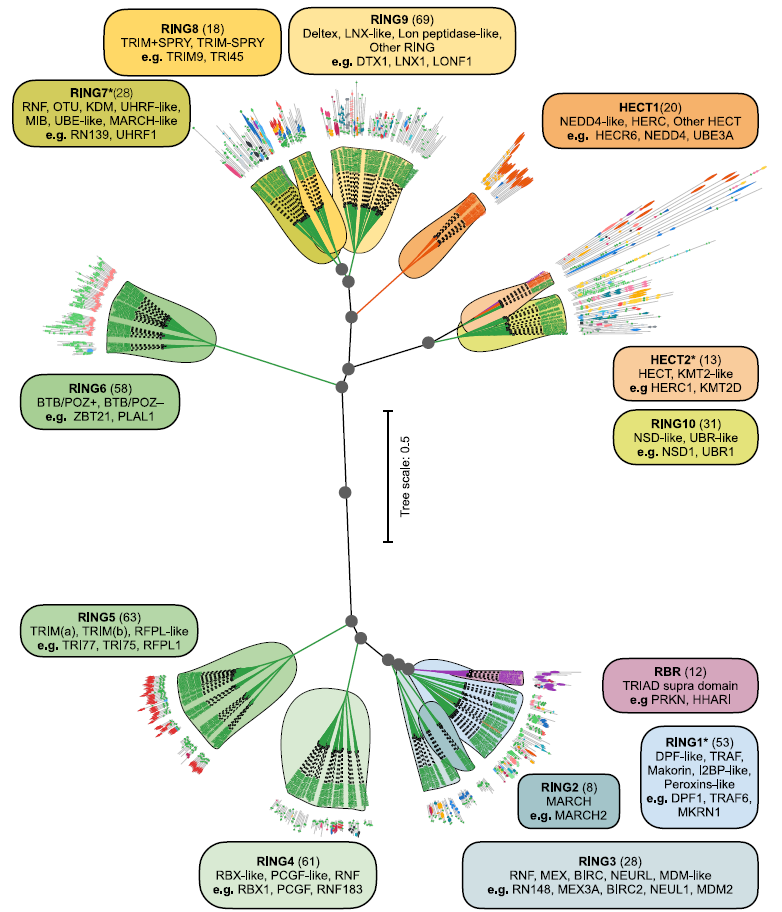
تخضع كل عائلة لمزيد من التحليل اليدوي لخصائص التسلسل والمجال لتحديد العائلات الفرعية والبروتينات الشاذة.
③ تكتل الجزيئات الصغيرة واحتمالية الارتباط
إسقاط UMAP ثنائي الأبعاد متكامل لتجميع الجزيئات الصغيرةتم تحديد عشرين مجموعة جزيئية صغيرة نموذجية من خلال دمج قمم الكثافة المحلية.تم تحديد احتمالية ارتباط كل مجموعة ببروتين E3 من خلال الميول المحولة لوغاريتميًا (LPij)، مما يوفر إرشادات لتطوير PROTAC اللاحق وتصميم الجزيئات الصغيرة المستهدفة.
تم تقديم تقييم مفصل لسلامة جينوم إنزيم E3 ليغاز البشري.
① التنظيم التفصيلي لجينوم إنزيم E3 ليغاز البشري
لمعالجة التحديات التي تفرضها الاستراتيجيات المتنوعة والتعريفات غير المتسقة المستخدمة في الدراسات الحالية عند تنظيم نظام E3، حدد فريق البحث هذا المكونات التحفيزية لنظام E3 تعريفًا دقيقًا على أنها تسلسلات عديد الببتيد تحتوي على نطاق تحفيزي واحد أو أكثر. يُمكّن هذا المعيار الموضوعي من التوصيف الصحيح والتحليل المُوجّه لنظام E3.في النهاية، وجد الباحثون أن 462 تسلسلًا من عديد الببتيد عبر مجموعة البيانات بأكملها تحتوي على مجال تحفيزي واحد على الأقل.تشكل هذه الببتيدات المتعددة جينومًا منظمًا بدقة لإنزيم E3 ليغاز البشري، كما هو موضح في الشكل أدناه:
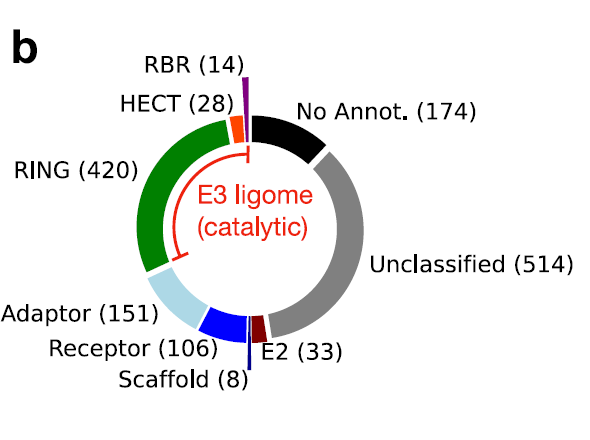
وللتحقق من موثوقية عملية الفرز، حدد الباحثون درجة توافق لكل بروتين بناءً على تكرار حدوثه في مجموعات البيانات من مصادر مختلفة.أظهرت النتائج أن إنزيمات الربط من الفئة E3 من نوع HECT و RBR كانت متسقة للغاية في مجموعة البيانات (درجة الإجماع ≥ 0.6، أشرطة برتقالية وأرجوانية).تتوزع نتائج الإجماع لفئة RING (الأشرطة الخضراء) على نطاق واسع، مما يشير إلى وجود تحدٍ في عملية الشرح، كما هو موضح في الشكل أدناه:
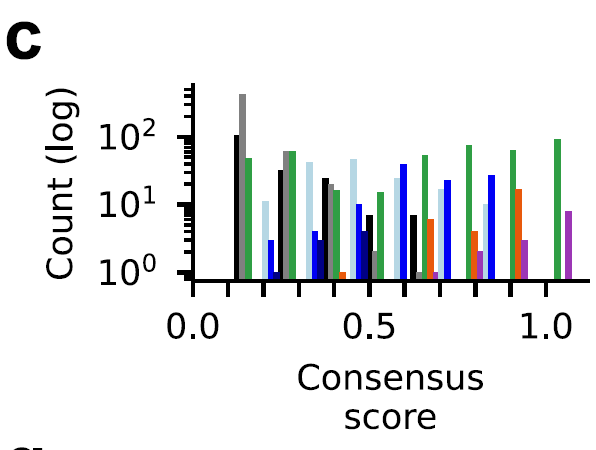
باستخدام هذه الطريقة، قلل الباحثون من النتائج الإيجابية الكاذبة والنتائج السلبية الحقيقية، وأدرجوا إنزيمات E3 النشطة تحفيزيًا ذات الموثوقية العالية، وأخذوا في الاعتبار إنزيمات E3 الزائفة وغيرها من إنزيمات E3 التي لم يتم التحقق من نشاطها التحفيزي، مما يوفر تقييمًا مفصلاً لسلامة جينوم إنزيم E3 ليغاز البشري.
② التمايز الوظيفي لإنزيم E3 ليغاز البشري
لتقييم وظيفة إنزيم E3 ليغاز البشري، قام الباحثون بفحص حذف CRISPR-Cas9 في جين UPS، باستخدام حيوية الخلية كنمط ظاهري أساسي. وأظهرت النتائج أن...تم تحديد ما مجموعه 53 مكونًا محفزًا و 32 مكونًا غير محفز من مكونات E3 باعتبارها ضرورية لبقاء الخلية على قيد الحياة.كما هو موضح أدناه:
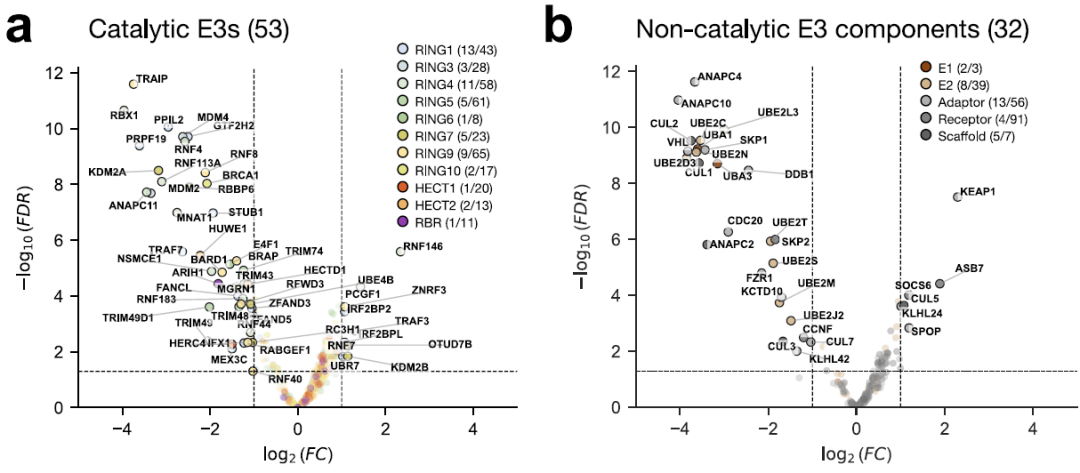
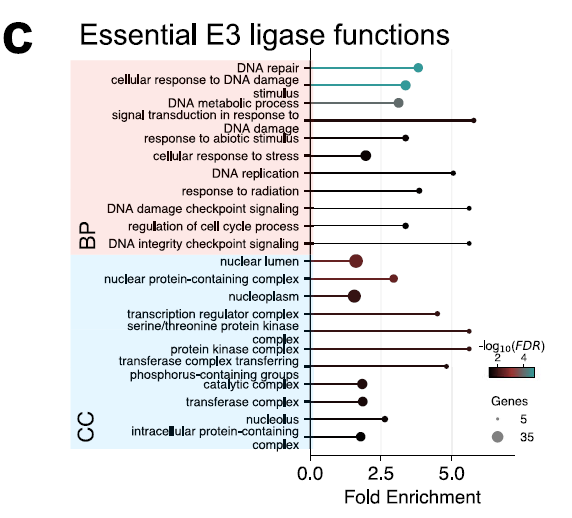
أظهر تحليل وظائف الجينات (GO) لـ 53 من إنزيمات E3 الرئيسية أنها تتواجد بكثرة في المكونات النووية وفي عمليات تلف الحمض النووي وتضاعفه وإصلاحه، كما هو موضح في الشكل أدناه، مما يشير إلى دورها المحوري في الحفاظ على سلامة الجينوم والتنظيم النووي. تكشف هذه النتائج عن مكونات E3 الضرورية لبقاء الخلية.
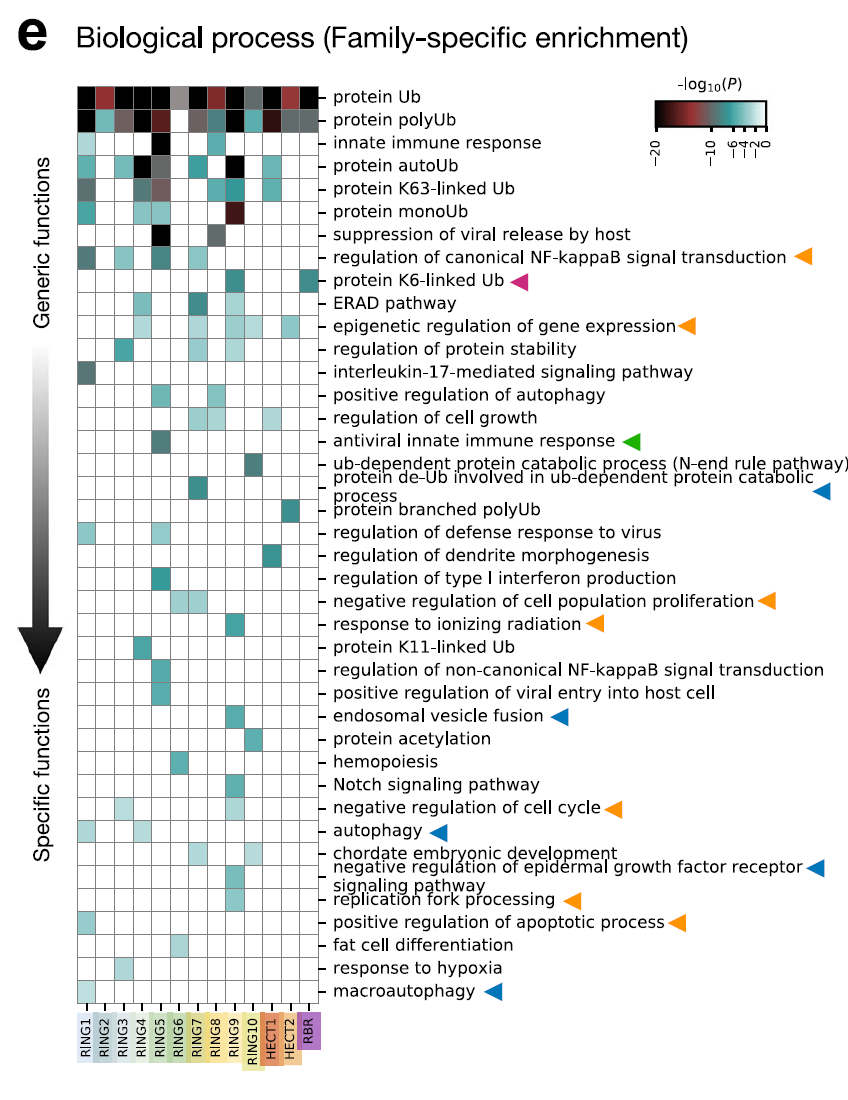
أُجري تحليل إثراء وظائف الجينات (GO) على 13 عائلة من عائلة E3 باستخدام برنامج Metascape، وتم تصوير الشبكة باستخدام برنامج Cytoscape. تُظهر النتائج أن...تُظهر العائلات المختلفة تخصصات متميزة في اختيار الركيزة، والتوطين الخلوي، والوظيفة التحفيزية.كما هو موضح في الشكل أدناه. على سبيل المثال، فإن أفراد عائلة RBR، RNF14 وRNF144A وPRKN، متخصصون في اليوبيكويتين المرتبط بـ K6. يمكن لسلسلة K6 المرتبطة أن تحدد معقدات البروتين-RNA المتوقفة (RNF14)، ومحول استشعار الحمض النووي STING (RNF144A) لتنشيط إشارات الإنترفيرون، والميتوكوندريا التالفة لإزالتها (PRKN). وبالمثل،تتواجد بروتينات TRIM E3 (RING5) بكثرة في الاستجابات المناعية الفطرية المضادة للفيروسات، وهي تنظم نشاط مستقبلات التعرف على الأنماط في الخلايا.مثل التفاعلات التي تتوسطها RIG-1 و MDA5.
④ خريطة قابلية استهداف إنزيمات E3 ليغاز البشرية بالأدوية
لاستكشاف مسارات علاجية محتملة تعتمد على التأثير المباشر، قام الباحثون برسم خرائط لجزيئات E3 الموجودة والمشتقة من بروتينات هجينة معروفة تستهدف تحلل البروتين (PROTACs) وجزيئات E3 الرابطة، وذلك لتحديد ارتباطها بمختلف أنواع E3 وعائلاتها. حاليًا، لا يمكن استهداف سوى 16 بروتينًا (9 بروتينات E3 محفزة و7 بروتينات محولة) بشكل مباشر بواسطة جزيئات E3 الموجودة. تستهدف معظم جزيئات E3 المصممة البروتينات المحولة (مثل VHL وCRBN)، بينما يستهدف عدد قليل جدًا منها بروتينات E3 المحفزة بشكل مباشر (مثل XIAP وMDM2/4/7 وBIRC2/3/7).
كشف تحليل أقرب جار باستخدام إنزيم E3 ليغاز البشري من هذه الدراسة عن خمسة بروتينات مترابطة للغاية (BIRC8 و RN166/181/141 و UBR2).كما هو موضح أدناه:
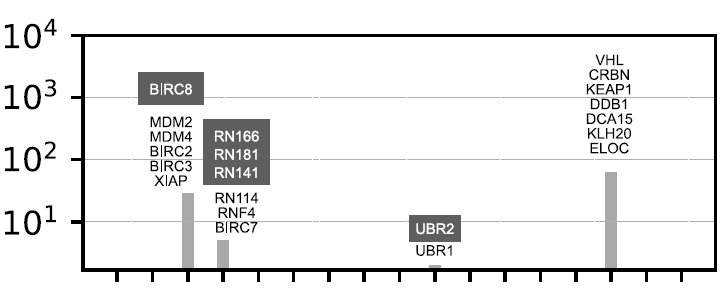
بسبب التشابه الهيكلي العالي (غالبًا ما تكون بروتينات متماثلة)، يمكن إعادة استخدام معاملات E3 الموجودة لاستهداف هذه البروتينات.لقد أتاح رسم خرائط لجزيئات E3 الصغيرة للباحثين الوصول إلى مجموعة محتملة من المركبات التي يمكنها استهداف 25 جزيئًا إضافيًا من E3 و15 مكونًا غير محفز.يكشف هذا الاكتشاف عن أهداف غير مستغلة، مما يوفر مسارًا للتصميم العقلاني للمركبات الرائدة لعامل E3، كما هو موضح في الشكل أدناه:
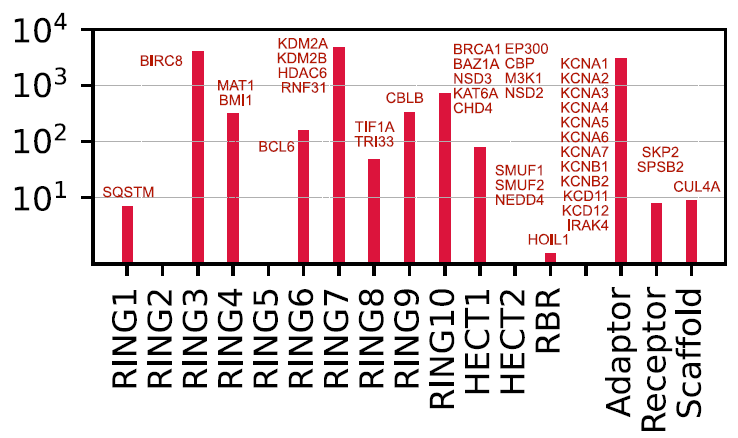
توفر الأطر متعددة المقاييس أدوات قوية لتحليل الأنظمة البيولوجية المعقدة.
في مجال التعلم الآلي، يشير إطار العمل متعدد المقاييس إلى أسلوب نمذجة أو استراتيجية تحليل قادرة على معالجة البيانات على مستويات تجريد مختلفة أو مقاييس سمات مختلفة. وهو ليس خوارزمية ثابتة، بل مفهوم تصميم يُستخدم لدمج المعلومات المحلية والعالمية، والسمات العامة والخاصة، مما يُحسّن من قدرة النموذج على التعبير والتعميم.
لا تقتصر قيمة إطار التصنيف متعدد المستويات على المراجعة المنهجية لعائلة إنزيمات E3 ليغاز فحسب، بل تكمن أهميته الأكبر في توفير نموذج قابل للتطبيق والتوسع لتكامل البيانات الجينومية. ويتيح هذا النهج التكاملي متعدد المستويات إمكانية توسيعه ليشمل بيانات جينومية متعددة الوسائط أخرى، مما يوفر أداة شاملة للتحليل المنهجي للأنظمة البيولوجية المعقدة.
فعلى سبيل المثال، تُعدّ الخلية الوحدة الأساسية للحياة، وتتحدد وظيفتها ومصيرها بواسطة شبكات جزيئية معقدة. ورغم أن أساليب التعلم العميق التقليدية تُحقق أداءً جيدًا في تحديد أنواع الخلايا من بيانات النسخ الجيني للخلايا المفردة، إلا أنها تفتقر إلى التفسير البيولوجي. في 20 أكتوبر 2025، اقترح باحثون من المركز الوطني لعلوم البروتين في الصين (بكين) وجامعة تسينغهوا برنامج Cell Decoder، وهو إطار عمل للتعلم العميق متعدد المقاييس وقابل للتفسير يدمج المعرفة البيولوجية المسبقة.فهو يتيح التوصيف الهرمي والاستدلال من الجينات والمسارات إلى العمليات البيولوجية، مما يوفر نهجًا جديدًا لفك شفرة أنواع الخلايا على مستوى الخلية الواحدة. يقوم برنامج Cell Decoder بإنشاء رسم بياني للمعرفة البيولوجية عبر المقاييس من خلال تضمين شبكات تفاعل البروتين، وتعيينات مسار الجينات، والعلاقات الهرمية للمسارات في بنية شبكة عصبية بيانية.قام فريق البحث بتقييم برنامج Cell Decoder بشكل منهجي مقارنةً بتسع طرق شائعة على عينات بشرية وفئران من سبع مجموعات بيانات متاحة للعموم للخلايا المفردة. وأظهرت النتائج أن برنامج Cell Decoder تصدّر القائمة من حيث دقة التنبؤ (0.87) ومؤشر F1 الكلي (0.81)، وحافظ على أداء مستقر حتى في ظل ظروف معقدة مثل التشويش، وعدم توازن أنواع الخلايا، وتغير توزيع البيانات بين الدفعات.
عنوان الورقة:فك شفرة الخلية: فك تشفير هوية الخلية باستخدام التعلم العميق القابل للتفسير متعدد المقاييس
عنوان الورقة:
https://link.springer.com/article/10.1186/s13059-025-03832-y
من منظور طويل الأمد، يمكن دمج إطار العمل متعدد المقاييس بشكل أكبر مع بيانات البروتينات المكانية، ومكتبات الأدوية الجزيئية الصغيرة، والمعلومات الكيميائية المكانية، مما يزيل حواجز البيانات بين البحوث البيولوجية الأساسية، وتحليل آليات الأمراض، والتطبيقات السريرية. ومع التراكم المستمر لبيانات علم الجينوم المتعدد، يُتوقع أن يلعب هذا الإطار دورًا داعمًا متزايد الأهمية في بحوث علوم الحياة والابتكار الطبي الحيوي.
مراجع:
1.https://www.nature.com/articles/s41467-025-67450-9
2.https://blog.csdn.net/qazplm12_3/article/details/153948711
3.https://link.springer.com/article/10.1186/s13059-025-03832-y