Command Palette
Search for a command to run...
أطلقت مائة جامعة أكبر دراسة متعددة المجموعات في العالم في مجال علم البروتينات الجينومية، والتي تكشف عن الجينات المسببة للأمراض وتعيد استخدام الأدوية الموجودة بناءً على بيانات من حوالي 80 ألف مشارك.
يُشبه الجينوم البشري دليلاً شاملاً للحياة، إذ يُسجّل جميع المعلومات الوراثية كالمظهر والطول والبنية الجسدية واحتمالية الإصابة بالأمراض. مع ذلك، فإن فك شفرة هذا الدليل ليس بالأمر الهيّن؛ فقد تحدث أحداث غير متوقعة، بما في ذلك طفرات مُمرضة تُهيّئ الأفراد للإصابة بأمراض مُعينة. والأكثر صعوبة هو...تقع معظم المتغيرات المسببة للأمراض في مناطق غير مشفرة من الجينوم لا تقوم بتشفير البروتينات بشكل مباشر.إن آلية "الصندوق الأسود" هذه، التي لا تحدد الجين المسبب للمرض أو الآلية التي يُسببه، تُحدّ بشدة من قدرتنا على استنتاج الجينات والآليات المسببة للمرض. وباعتبارها المنفذين المباشرين الذين يُفعّلون وظائف الجينات،تُعد آلاف البروتينات المنتشرة في دم الإنسان مفتاحًا لكشف آليات الصندوق الأسود وربط الاختلافات غير المشفرة بالآليات المرتبطة بالأمراض.
حققت أبحاث علم البروتينات الجينومية تقدماً ملحوظاً في فهم الأمراض السريرية والأهداف الدوائية المحتملة، إلا أن هناك قيوداً لا تزال تعيق تطبيقها المنهجي والواسع النطاق في علم الأحياء البشري. أولاً، ركزت الأبحاث السابقة بشكل شبه كامل على المتغيرات الجينية القريبة المؤثرة في نفس الجين (أي مواقع السمات الكمية للبروتين في نفس الجين، cis-pQTLs).قد توجد الاختلافات غير المشفرة في المناطق التنظيمية، مما يؤثر بشكل مباشر على العديد من الجينات المشفرة المجاورة.ويمكنها أيضًا تنظيم البروتينات المشفرة بواسطة الجينات في مواقع أخرى في الجينوم بشكل غير مباشر عن بعد؛ ثانيًا، لا تزال الأبحاث السابقة حول البنية الجينية متعددة الجينات للعلامات الحيوية البروتينية التي تؤثر على تشخيص الأمراض والتنبؤ بها غير كافية؛ أخيرًا، لتحديد مواقع السمات الكمية للبروتين بشكل مستقر وعام، يلزم التحقق المتكرر في مجموعات سكانية مختلفة.حالياً، يتم إجراء عدد قليل جداً من الدراسات البشرية للتحقق من صحة هذا النوع في مجال البروتينات واسعة النطاق.
وفي ضوء ذلك،نشر فريق من أكثر من مائة جامعة ومؤسسة بحثية، بما في ذلك جامعة كوين ماري في لندن وجامعة كامبريدج، أكبر دراسة متعددة المجموعات في علم البروتينات الجينومية في العالم حتى الآن.استنادًا إلى تحليل تلوي واسع النطاق لجينومات البروتيوغليسيميك التي تغطي 38 مجموعة بحثية مستقلة وما مجموعه 78664 شخصًا، تم تحديد 24738 موقعًا للسمات الكمية للبروتينات بشكل منهجي وربطها بـ 1116 بروتينًا متداولًا، مما يكشف بشكل شامل عن السمات التنظيمية الجينية الواسعة النطاق للتقارب والمسافة على مستوى البروتين.
استُخدمت تقنيات التعلّم الآلي لتحليل المسارات الرئيسية وأنواع الخلايا وأصول الأنسجة التي تنظم وفرة البروتينات المنتشرة في الدم، مما أوضح الدور المحوري لعملية الغلكزة المرتبطة بالنيتروجين في شبكة تنظيم البروتينات. علاوة على ذلك، يُسهم التمييز بين الاختلافات التنظيمية في مواقع الارتباط الموضعية (cis) والمواقع البعيدة (trans) في البروتينات في توضيح الآليات الجوهرية للأنماط الظاهرية البيولوجية المختلفة، مما يوفر أدلةً لفحص أهداف دوائية بروتينية محتملة لأمراض معينة. كما كشف تحليل التثليث للمواقع البعيدة عن أدلة أعمق على "إعادة استخدام الأدوية".
تم نشر نتائج البحث ذات الصلة، بعنوان "تحليلات البروتيوجينوم متعددة المجموعات تكشف عن تأثيرات جينية عبر البروتوم والديسازوم"، في مجلة Cell.
أبرز الأبحاث:
* أكبر دراسة متعددة المجموعات في علم البروتينات الجينومية حتى الآن، تشمل 38 مجموعة دراسة مستقلة وتضم ما مجموعه 78664 مشاركًا.
* تم تحديد 24738 موقعًا للسمات الكمية للبروتينات وربطها بـ 1116 بروتينًا متداولًا، مما كشف بشكل شامل عن مجموعة واسعة من السمات التنظيمية الجينية القريبة والبعيدة المدى على مستوى البروتين.
* توضح هذه الدراسة بشكل منهجي الآليات التنظيمية للبروتينات المنتشرة على المستوى الجيني، مما يوفر أساسًا نظريًا مهمًا وموارد بيانات لفهم الآليات الجزيئية للأمراض البشرية، وتحديد الأهداف العلاجية المبتكرة، وإجراء أبحاث إعادة توظيف الأدوية.

عنوان الورقة:
https://www.cell.com/cell/fulltext/S0092-8674(26)00385-5
أكبر قاعدة بيانات أساسية: 38 مجموعة دولية، ما يقرب من 80,000 مشارك
تمثل هذه الدراسة أكبر تحليل تجميعي بروتيني متعدد المجموعات في العالم.دمج 38 مجموعة دولية، تغطي 78664 مشاركًا من أصل أوروبي،استنادًا إلى تحليل 1161 هدفًا من بروتينات الدم باستخدام تقنية البروتينات عالية الإنتاجية Olink، تم تحديد 24738 موقعًا كميًا للبروتينات (pQTLs) تم تحديدها بدقة (بما في ذلك 5040 موقعًا كميًا للبروتينات cis-pQTLs و 19698 موقعًا كميًا للبروتينات trans-pQTLs)، وتم الحصول على بيانات تنظيمية جينية لـ 1116 بروتينًا فعالًا.
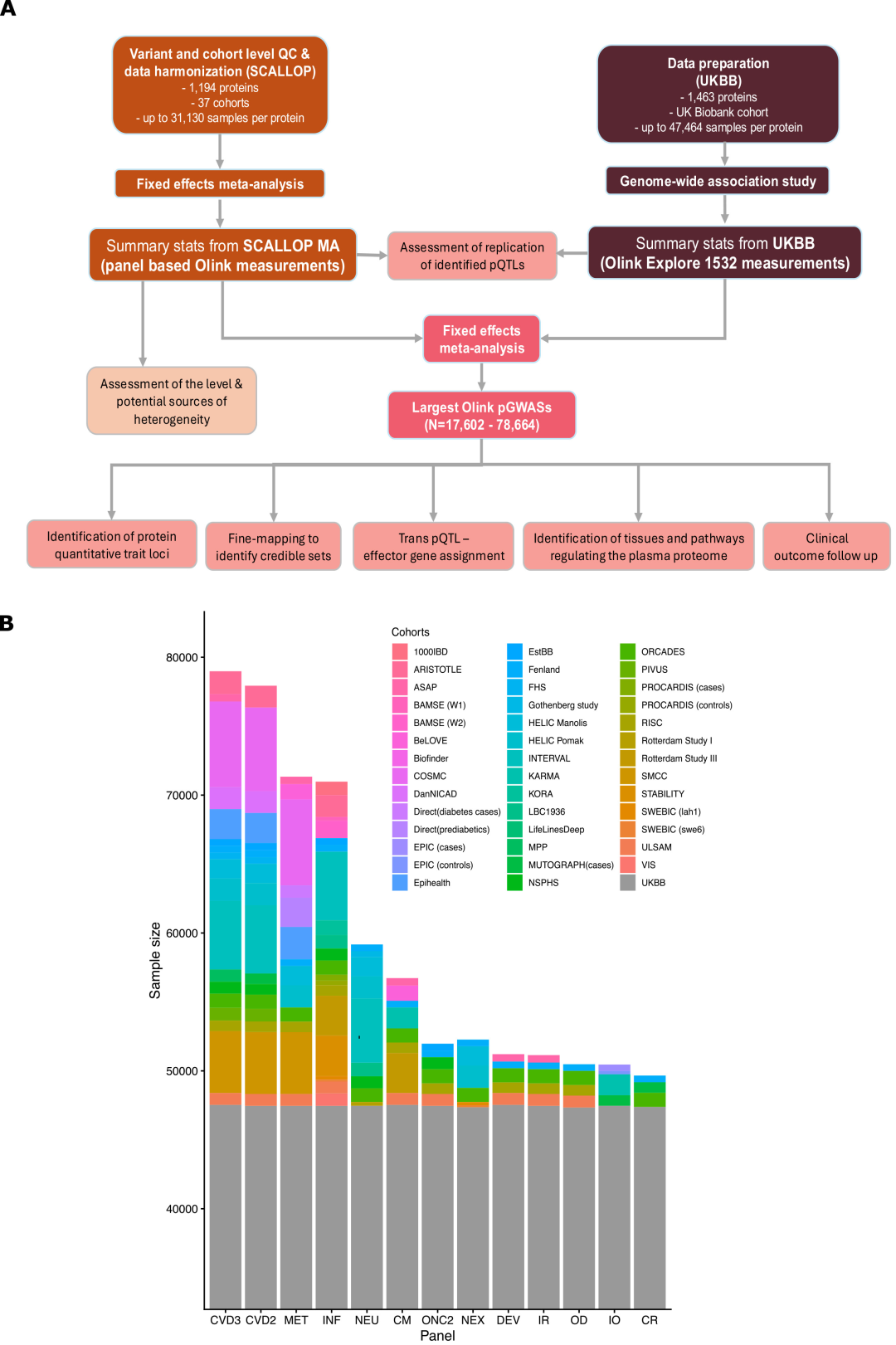
التحليلات التلوية لـ SCALLOP:تتضمن هذه البيانات إحصاءات الجينوم الكامل من 37 مجموعة و1194 بروتينًا مستهدفًا في الدم، حيث أن غالبية المشاركين من أصول أوروبية. أُجريت فحوصات البروتينات القائمة على الأجسام المضادة باستخدام لوحة واحدة على الأقل من لوحات فحص Target-96 البالغ عددها 13 لوحة، والمقدمة من شركة Olink، والتي تتميز كل منها بقدرتها على الكشف عن 92 بروتينًا مستهدفًا تغطي مجالات القلب والأوعية الدموية، والمناعة، والالتهابات، والجهاز العصبي، والتمثيل الغذائي.
بنك المملكة المتحدة الحيوي (UKBB):شملت الدراسة 48,017 مشاركًا من أصول أوروبية. وللحصول على هذه البيانات، تم توليد قياسات البروتينات المستخدمة في الدراسة عبر منصة Olink Explore 1536، والتي استخدمت أيضًا تقنيات تعتمد على الأجسام المضادة لقياس 1,463 بروتينًا مستهدفًا.
مصنف التعلم الآلي المرحلي
يتمثل الهدف الرئيسي لهذه الدراسة، التي تستخدم نماذج التعلم الآلي، في تحديد "الجينات المؤثرة" بشكل منهجي ودقيق وعلى نطاق واسع لجميع مواقع السمات الكمية للبروتين (trans-pQTLs) الواقعة خارج منطقة معقد التوافق النسيجي الرئيسي (MHC). ويعالج هذا التحدي القائم منذ فترة طويلة والمتمثل في تحديد مواقع الجينات المؤثرة في المناطق الجينومية البعيدة عن مواقع السمات الكمية للبروتين المرتبطة بمستويات بروتينات الدم. ولتحقيق هذه الغاية،استلهاماً من بنية ProGeM، قام الباحثون ببناء مصنف تعلم آلي مرحلي.
أولًا، فيما يتعلق بمصادر السمات والتعليقات التوضيحية، قام الباحثون بدمج تعليقات توضيحية بيولوجية وجينومية متعددة الأبعاد لكل متغير جيني أو متغيراته البديلة (r² > 0.6). وشملت التعليقات التوضيحية على مستوى المتغير المسافة بين المتغير والجينوم ضمن نافذة أساسية تبلغ 1 ميجابايت، والتأثير الوظيفي المحتمل المستنتج بناءً على أداة التنبؤ بتأثير المتغير (VEP).
في الوقت نفسه، تم إجراء عملية توصيف على مستوى الجين لكل جين ضمن نافذة أساسية 1 ميجابايت، بما في ذلك الحصول على أدلة ذات صلة بالتوطين المشترك لـ QTL بناءً على وفرة البروتين GTEx v8 وتعبير الجين، وارتباط حمل المتغيرات النادرة، باستخدام حزمة OmnipathR الإصدار 3.10.1 لمراجعة الأدبيات وتحديد ما إذا كانت هناك معقدات ربيطة-مستقبل/بروتين تتوافق مع البروتينات cis المشفرة بواسطة الجينات trans، وتحديد ما إذا كانت الجينات ذات الصلة تشارك في نفس المسار البيولوجي بناءً على معلومات توصيف KEGG/REACTOME.
ثم ننتقل إلى بناء مجموعة التدريب اللازمة لنموذج التعلم الآلي، ولكن نظرًا لعدم وجود متغيرات معيارية ذهبية شائعة الاستخدام لتخصيص الجينات،استخدم الباحثون المعرفة المسبقة بعلم الأحياء وعلم الجينوم للحصول على ثلاث مجموعات مستقلة جزئيًا من "الإيجابيات الحقيقية المفترضة (PTPs)".لتجنب التحيز، تم الاحتفاظ ببروتين واحد فقط من نوع cis ضمن كل مجموعة PTP، واعتُبرت الجينات الأخرى ضمن نطاق 1 ميجابايت عينات سلبية. وشمل ذلك تحديدًا الجينات من نوع trans التي تُشفّر أزواجًا من الليجاندات والمستقبلات أو تُشكّل مُركّبات بروتينية عالية الموثوقية مع بروتينات cis (عددها 540)، ومواقع pQTLs من نوع trans التي تم تحديد مواقعها على المتغيرات الوظيفية (عددها 1747)، والجينات من نوع trans ذات أحمال متغيرات نادرة كبيرة (عددها 1049). ثم قُسّمت مجموعات التدريب والاختبار بنسبة 7:3 بناءً على المناطق الجينومية، وكُرّرت النتائج 10 مرات لضمان استقرارها.
علاوة على ذلك، فيما يتعلق ببنية النموذج وعملية التدريب، تعتمد خوارزمية النموذج في هذه الدراسة على مصنف الغابة العشوائية. ومن خلال إدخال 10 مجموعات تدريب، يتم إجراء التحقق المتقاطع ثلاثي الطيات بشكل متكرر، بالإضافة إلى استراتيجية أخذ عينات فرعية، مما يعالج مشكلة عدم توازن مجموعات البيانات أثناء التدريب.تم تنفيذ تدريب النموذج باستخدام مجموعة أدوات caret v6.0.94 للغة R، ثم تم اختيار أفضل نموذج غابة عشوائية أداءً في كل مجموعة تدريب من خلال تقييم درجة كابا.
بعد ذلك، وباستخدام عشرة مصنفات للغابات العشوائية، لكل مجموعة بيانات افتراضية إيجابية حقيقية، تم تقييم جميع الجينات المؤثرة المرشحة لـ trans-pQTL واحدًا تلو الآخر. تم أولًا حساب متوسط درجات المصنفات العشرة لنفس مجموعة البيانات الافتراضية الإيجابية الحقيقية، ثم جُمعت مجموعات الدرجات المتوقعة الثلاث. في الوقت نفسه، عند بناء نموذج التصنيف لكل مجموعة بيانات افتراضية إيجابية حقيقية، تم حذف متغيرات الميزات المستخدمة لتحديد العينات الإيجابية الحقيقية.
في النهاية، أظهرت جميع نماذج التصنيف الثلاثة أداءً مستقرًا وموثوقًا به، حيث تراوحت معاملات كابا الوسيطة من 0.54 إلى 0.57.
إن فك شفرة آلية التسبب في المرض يوفر أدلة جينية لتطوير الأدوية وإعادة استخدام الأدوية الموجودة.
أجرت هذه الدراسة، التي استندت إلى 38 مجموعة دولية وشملت 78664 مشاركًا، تحليلًا تلويًا متعدد المجموعات للبروتين الجينومي يستهدف 1161 هدفًا من بروتينات الدم، مما أدى إلى توضيح أنماط التنظيم الجيني لمستويات البروتين المنتشرة وارتباطها بالأمراض بشكل منهجي.
تحديد وخصائص pQTL
حددت الدراسة 14690 متغيرًا إقليميًا مؤشرًا، وأسفرت عملية التحديد الدقيق باستخدام منهج بايزي عن 24738 مجموعة متغيرات مستقلة وموثوقة، تشمل 5040 موقعًا كميًا للبروتين في الموقع cis-pQTL و19698 موقعًا كميًا للبروتين في الموقع trans-pQTL، وتغطي 1116 هدفًا بروتينيًا. من بين هذه المواقع، وُجدت مواقع cis-pQTL في البروتين عند الموقع 87.1%، ومواقع trans-pQTL في البروتين عند الموقع 94.1%؛ وكانت مواقع cis-pQTL عند الموقع 82.3% ومواقع trans-pQTL عند الموقع 83.3% مواقع عالية الموثوقية، تحتوي على 278 موقعًا جديدًا من مواقع cis-pQTL و4013 موقعًا من مواقع trans-pQTL. علاوة على ذلك، في مجموعة الأصول غير الأوروبية، أظهرت أحجام التأثير للمواقع المحددة ارتباطًا معتدلًا مع المجموعة الأوروبية (r = 0.6).وهذا يؤكد متانة النتائج عبر مختلف المجموعات السكانية.
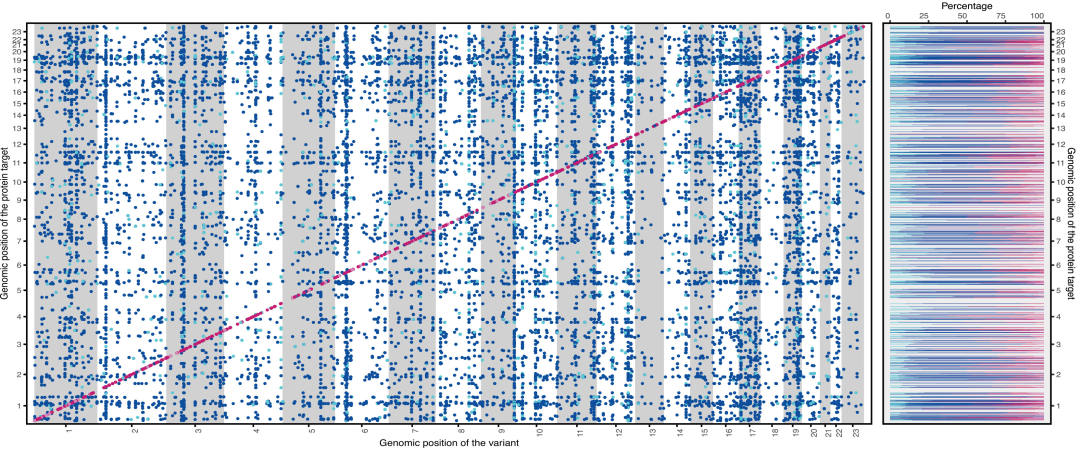
مواقع الصفات الكمية للبروتين المحددة بدقة في التحليلات التلوية لـ SCALLOP و UKBB
علاوة على ذلك، توجد اختلافات كبيرة في القدرة التفسيرية للمواقع الجينية لتغيرات مستويات بروتينات الدم. تفسر مواقع cis-pQTLs ما معدله 8.41 TP3T من تباين البروتين، وهو أعلى بكثير من مواقع trans-pQTLs. مع ذلك، تُنظَّم بروتينات مثل ICAM2 وFUCA1 بشكل رئيسي بواسطة مواقع trans-pQTLs، بقدرة تفسيرية تبلغ 52.71 TP3T و68.41 TP3T على التوالي، بينما تفسر مواقع cis-pQTLs ما لا يزيد عن 0.31 TP3T و6.31 TP3T.
علاوة على ذلك، كشفت الملاحظة الإضافية لـ 261 هدفًا بروتينيًا عن عدم وجود ارتباط خطي كبير بين القدرة التفسيرية لتغيرات pQTL الخاصة بها وقابلية التوريث متعددة الجينات، مما يشير إلى أن هذه الدراسة ربما تكون قد وصلت إلى حد التشبع تقريبًا في تحديد pQTLs لهذه البروتينات.
خصائص البروتينات المستهدفة الخاضعة لتنظيم الجينات
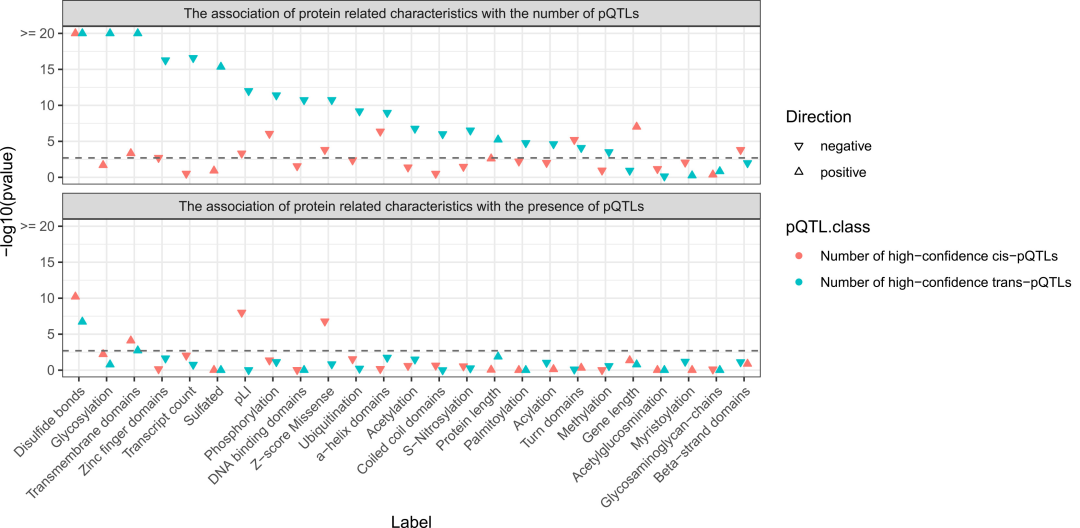
خصائص البروتين المتعلقة بوجود وكمية pQTLs بناءً على نموذج انحدار بواسون ذي التضخم الصفري.
تحتوي البروتينات التي تحتوي على روابط ثنائية الكبريتيد ومجالات عبر الغشاء على عدد أكبر بكثير من pQTLs، مما قد يفسر سبب سهولة تنظيم هذه البروتينات وراثيًا؛ في حين أن قوة القيد الوظيفي للجينات المشفرة للبروتين ترتبط بشكل سلبي كبير بعدد cis-pQTLs.
البروتينات التي تحتوي على عدد كبير من مواقع التعبير الجيني الكمي العابر (trans-pQTLs) غنية بشكل كبير بخصائص البروتينات الإفرازية مثل الغلكزة والكبرتة، ولكنها تفتقر إلى خصائص البروتينات داخل الخلايا مثل هياكل أصابع الزنك ومجالات ربط الحمض النووي، مما يشير إلى أن التنظيم الجيني بعيد المدى للبروتينات المنتشرة يرتبط ارتباطًا وثيقًا بالمسار الإفرازي.
تحليل جينات المؤثرات عبر pQTL والمسارات التنظيمية
استنادًا إلى دمج المعرفة البيولوجية السابقة في إطار التعلم الآلي، تم تحديد جين مؤثر واحد على الأقل بدرجة ثقة معتدلة لأكثر من نصف مواقع trans-pQTLs (n = 11261)، منها 1534 موقعًا بدرجة ثقة عالية؛ بالنسبة لثلثي المواقع (n = 13881)، أشار توزيع درجات المرشحين عبر الجينات إلى أن جينًا سببيًا واحدًا هو الجين الممرض الأكثر احتمالًا.
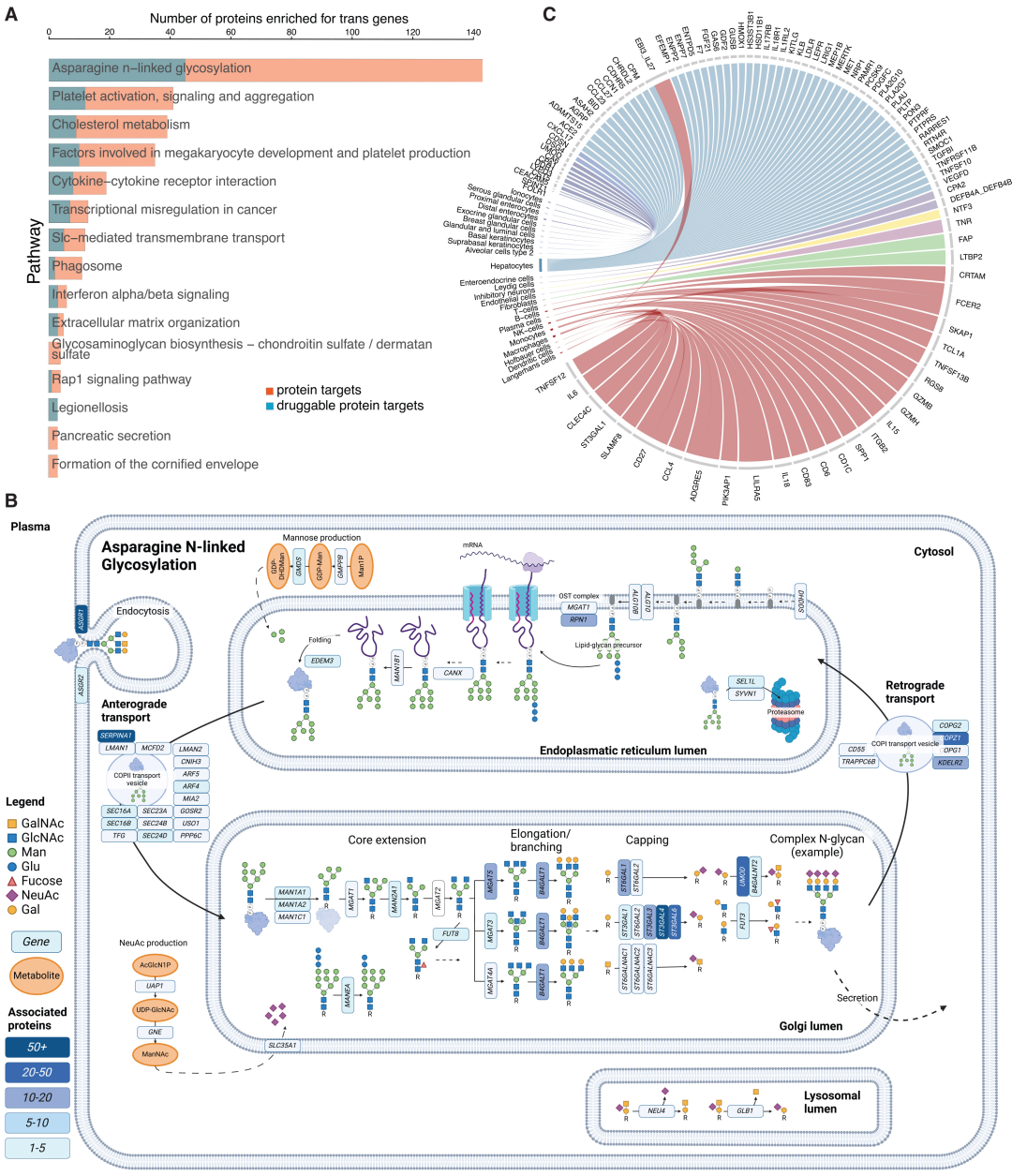
أظهر تحليل الإثراء الوظيفي أن الجينات ذات التأثير العابر كانت غنية بشكل كبير في مسار الأسباراجين N-جليكوزيل (الذي يشمل 143 هدفًا بروتينيًا) وتنشيط الصفائح الدموية (الذي يشمل 41 هدفًا بروتينيًا)، من بين أمور أخرى.يُعدّ الغليكوزيل N المسار التنظيمي الأكثر شيوعًا وأساسيًا.
أظهرت نتائج إثراء الخلايا والأنسجة أن الجينات ذات التأثير العابر كانت معبرة بشكل كبير في خلايا الكبد، والخلايا القاتلة الطبيعية، والخلايا البطانية، والخلايا السنخية من النوع الثاني، مما يكشف أن الكبد والخلايا المناعية مواقع رئيسية للتنظيم عن بُعد للبروتينات المنتشرة في الدم. وكانت 44 زوجًا من البروتين والنسيج، و76 زوجًا من البروتين ونوع الخلية، ذات أصل إفرازي غير تقليدي، مما يؤكد الدور المهم للتواصل بين الأعضاء في تنظيم استتباب البروتين.
التأثيرات المتعددة على المستويين الجزيئي والظاهري
من بين جميع مواقع pQTL المستقلة المحددة، أظهر 43.41 موقعًا من مواقع TP3T تأثيرات متعددة، حيث أظهرت مواقع pQTL العابرة تأثيرات متعددة أعلى بشكل ملحوظ من مواقع pQTL المجاورة. صنّفت الدراسات اللاحقة التباينات الجينية متعددة التأثيرات إلى ثلاثة أنواع: "التأثيرات الجزيئية المتعددة"، و"التأثيرات الظاهرية المتعددة"، و"التأثيرات غير النوعية المتعددة". أظهر أكثر من نصفها (332 من أصل 533) تأثيرات ظاهرية متعددة.وعلى وجه الخصوص، تم تعزيز تعبيره بمقدار الضعف في الخلايا الكبدية، وقام بتنظيم البروتين المستهدف بشكل تفضيلي من خلال المركبات البروتينية، وتفاعلات الربيطة والمستقبل، وتآزر المسار.
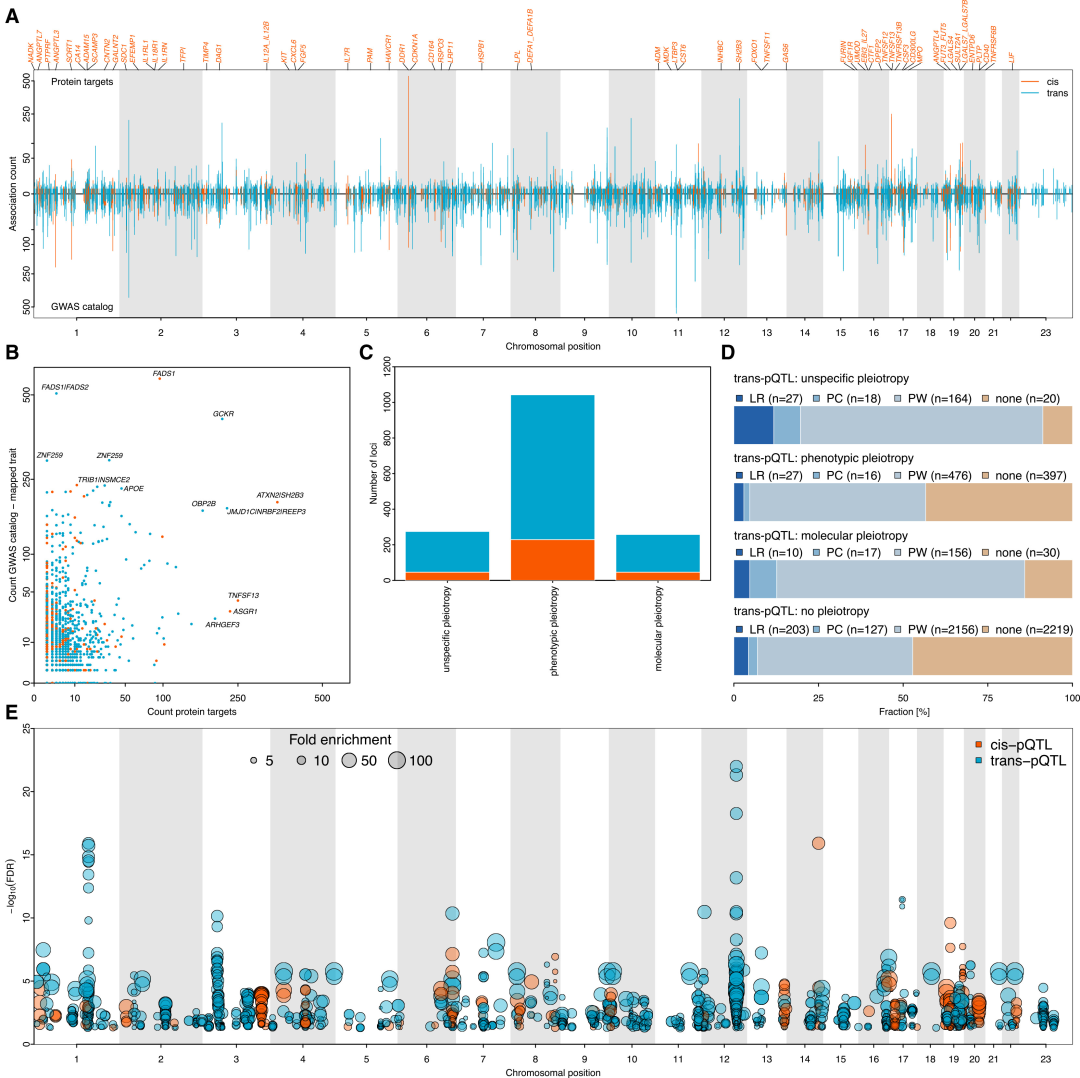
تتداخل 285 من مواقع pQTL متعددة التأثيرات مع مواقع GWAS للأمراض، والبروتينات المرتبطة بها غنية بشكل كبير في مسارات محددة، مما يوفر أدلة جديدة لتوضيح آليات مواقع GWAS للأمراض.
الاختلافات في الأنماط الظاهرية للأمراض في ظل التنظيم الموضعي والتنظيم البعيد
قام الباحثون بدمج 300 ارتباط محدد بين البروتين والأمراض، مدفوعة بمواقع cis-pQTL، مع أكثر من 700 مجموعة بيانات للأمراض من مشروع FinnGen. وقد أسفر 73 ارتباطًا فقط من هذه الارتباطات عن تحليلات إحصائية للتوطين المشترك، والتي رصدت كلاً من التوزيع العشوائي المندلي (MR) وإشارات المخاطر الجينية.يشير هذا إلى أن هناك حاجة إلى أدلة تكميلية عند تحديد أولويات الجينات المسببة للأمراض المحتملة.
من بين 115 ارتباطًا قابلاً للتقييم، أظهر 31 ارتباطًا تأثيرات تنظيمية متسقة في الموقع والمواقع البعيدة، ولم يكن لدى 41 ارتباطًا أي دليل داعم، وأظهر 14 ارتباطًا تأثيرات معاكسة، مما يشير إلى وجود فرق كبير في تأثير التنظيم القريب والتنظيم البعيد على النمط الظاهري للمرض.
تحليل ارتباط البروتين بالمرض في الاستدلال الجيني والدراسات الرصدية
تدمج هذه الدراسة بيانات رصدية من 52,164 مشاركًا في دراسة UKBB وبيانات جينية من أكثر من 1.29 مليون فرد في قاعدة بيانات PanBio، تغطي 517 مرضًا. من بين 193 ارتباطًا جينيًا عالي الموثوقية، لم يدعم سوى 52 ارتباطًا منها بشكلٍ ثابت من خلال الدراسات الرصدية؛ ومن بين 52,887 ارتباطًا رصديًا هامًا، لم يحصل سوى 0.061 من جين TP3T على دليل جيني. والجدير بالذكر أن بروتين فورين الدم يُعدّ من الأهداف القليلة المرتبطة باستمرار بارتفاع ضغط الدم، واحتشاء عضلة القلب، والرجفان الأذيني في كلٍ من الدراسات الجينية والرصدية، مما يكشف عن قيمته المحتملة في تطوير الأدوية.
تُسهم تقنية trans-pQTL في اكتشاف المؤشرات الحيوية للأمراض وإعادة توجيه الأدوية.
أظهرت الدراسة وجود وفرة ملحوظة في أكثر من 901 مؤشر حيوي بروتيني لأمراض TP3T (280 من أصل 307 أمراض) ضمن البروتينات المرتبطة بـ trans-pQTL، مما يؤكد أن التنظيم الجيني العابر هو الأساس الجيني الرئيسي للمؤشرات الحيوية البروتينية للأمراض. ووجدت الدراسة أن طفرة rs34536443 في جين TYK2، باعتبارها trans-pQTL، تنظم العديد من البروتينات الالتهابية مثل BST2 وCXCL9/10/11. وترتبط المستويات المرتفعة لهذه البروتينات بزيادة خطر الإصابة بالتهاب المفاصل الروماتويدي والصدفية والتهاب الغدة الدرقية المناعي الذاتي، مما يوفر دليلاً جينياً لإعادة توظيف مثبطات TYK2 لعلاج أمراض المناعة الذاتية.
خاتمة
كشفت هذه الدراسة، التي استندت إلى أكبر تحليل بروتيوجينومي متعدد المجموعات في العالم، بشكل منهجي عن أنماط التنظيم الجيني للبروتينات المنتشرة في الدم لدى الإنسان. وقد تجاوزت الدراسة قيود الدراسات السابقة التي ركزت فقط على التنظيم الموضعي، وكشفت لأول مرة بشكل شامل عن الدور المحوري للتنظيم الجيني العابر في تنظيم وفرة البروتينات المنتشرة في الدم على مستوى عينة كبيرة. علاوة على ذلك، استخدمت الدراسة تقنيات التعلم الآلي لتحديد مواقع الجينات المؤثرة بدقة، مما ساهم في توضيح المسارات الأساسية مثل الغلكزة المرتبطة بالنيتروجين وبيولوجيا الصفائح الدموية، بالإضافة إلى المواقع التنظيمية الرئيسية مثل الكبد والخلايا المناعية.
على الرغم من وجود بعض القيود في هذه الدراسة، مثل اقتصار تقنية البروتينات على بعض الأنواع الفرعية والتعديلات اللاحقة للترجمة للبروتينات المنتشرة في الدم، وكون غالبية المشاركين من أصول أوروبية، مما يستدعي توسيع نطاق الدراسة ليشمل المزيد من المجموعات العرقية، إلا أنها تُرسّخ إطارًا متكاملًا يربط بين التغيرات الجينية غير المشفرة، والبروتينات المنتشرة في الدم، وآليات الأمراض. ولا يقتصر الأمر على توفير منظور جديد لتوضيح الآليات الجزيئية للأمراض المعقدة، بل يُرسّخ أيضًا أهدافًا رئيسية مثل فورين البلازما وTYK2 من خلال أدلة جينية، مما يُوفر أدلة جينية موثوقة للغاية لتطوير أدوية مبتكرة وإعادة استخدام الأدوية، ويُعزز خطوة حاسمة في ترجمة علم البروتينات الجينومية من الاكتشافات الأساسية إلى التطبيقات السريرية.