Command Palette
Search for a command to run...
قامت مجموعة أبحاث لي هونغلين في جامعة شرق الصين للعلوم والتكنولوجيا بتطوير Macformer لتسريع اكتشاف الأدوية الحلقية الكبيرة

المركبات الحلقية الكبيرة هي جزيئات صغيرة أو ببتيدات تتكون من أكثر من 12 ذرة. بالمقارنة مع المركبات الجزيئية الصغيرة الأخرى، تتمتع المركبات الحلقية الكبيرة بالعديد من المزايا من حيث البنية والأداء، وبالتالي تعتبر أدوية علاجية محتملة لأهداف مختلفة.
تشكل النظائر الحلقية الكبيرة المعتمدة على تركيب الكيمياء الطبية مصدرًا رئيسيًا للأدوية الحلقية الكبيرة. ومع ذلك، بسبب الافتقار إلى الأساليب التركيبية، والصعوبة الكبيرة في التركيب، وقلة المواد المرجعية، لم يحظ تطوير الأدوية الحلقية الكبيرة إلا باهتمام ضئيل.
ولتحقيق هذه الغاية، قامت مجموعة البحث التابعة للي هونغلين في جامعة شرق الصين للعلوم والتكنولوجيا بتطوير Macformer استنادًا إلى Transformer. نجح ماكفورمر في تحويل عقار فيزوتينيب اللاحلقي إلى مركبات جديدة ذات فعالية أقوى، مما يوفر نهجًا جديدًا لتطوير الأدوية.
المؤلف | شيويه تساي
المحرر | سانيانغ
تاريخ الأدوية كبيرة الحلقات
الحلقات الكبيرة هي جزيئات صغيرة أو ببتيدات تتكون من أكثر من 12 ذرة.. يتميز هذا النوع من المركبات بوزن جزيئي مرتفع وعدد كبير من مانحي الروابط الهيدروجينية، كما يتمتع بتقارب وانتقائية وخصائص دوائية أقوى.تم اعتبار الأدوية الحلقية الكبيرة بمثابة أدوية علاجية محتملة لأهداف مختلفة، مثل الكينازات والبروتيازات ومستقبلات البروتين ج المقترنة.

بالإضافة إلى الأدوية الكبيرة الحلقية الطبيعية، فإن النظائر المعتمدة على التركيب الكيميائي الصيدلاني تشكل أيضًا مصدرًا رئيسيًا للأدوية الكبيرة الحلقية.من خلال تحويل الأدوية غير الحلقية المعروفة إلى أدوية حلقية كبيرة الحجم، يمكن الحصول على أدوية حلقية كبيرة الحجم جديدة بشكل مباشر وفعال.، وتحقيق الخصائص الدوائية المطلوبة. لكن،بسبب نقص الطرق التركيبية والصعوبة الكبيرة في التركيبلا تزال الأدوية ذات الحلقات الكبيرة تحظى باهتمام ضئيل في تصميم الأدوية.
في الوقت الحالي، تعتمد عملية تكوين الجزيئات الخطية على الاستدلال التجريبي بشكل أساسي. علاوة على ذلك، حتى لو قدمت الأدبيات نتائج التوليف النهائية، فإن عملية التوليف والاستنتاج للدواء تكون غامضة دائمًا. لقد أدت عملية التركيب غير الشفافة وغير القياسية إلى رفع عتبة الصناعة وإعاقة تطوير الأدوية الحلقية الكبيرة.
على الرغم من أن التعلم العميق أظهر إمكانات كبيرة في مراحل مختلفة من تطوير الأدوية،لكن تدريب الشبكات العصبية يتطلب قدرًا كبيرًا من البيانات. نظرًا لوجود أقل من 90 دواءً كبيرًا حلقيًا معتمدًا سريريًا، فلا يوجد بحث حول تحويل الأدوية إلى أدوية كبيرة حلقية باستخدام خوارزميات التعلم العميق.
تحقيقا لهذه الغاية،قامت مجموعة البحث التابعة للي هونغلين في جامعة شرق الصين للعلوم والتكنولوجيا بتطوير Macformer استنادًا إلى Transformer، لتحقيق تكوين حلقات كبيرة من الجزيئات الخطية. قاموا بتوسيع البيانات من خلال تمثيل نفس المركب باستخدام مواصفات الإدخال الخطية الجزيئية المبسطة المختلفة (SMILES).
وبعد ذلك، تم أخذ Fedratinib، وهو مثبط JAK2 معتمد من قبل إدارة الغذاء والدواء الأمريكية (FDA)، كمثال، وتم استخدام Macformer لتحويله إلى حلقات كبيرة للحصول على مركب حلقي كبير جديد.يتمتع هذا المركب بانتقائية وخصائص حركية دوائية أفضل، لذا فإن الجرعة المطلوبة أقل من جرعة الفوزوتينيب.. وقد نشرت هذه النتيجة في مجلة "Nature Communication".

احصل على الورقة:https://www.nature.com/articles/s41467-023-40219-8
اتبع الحساب الرسمي ورد "الأدوية الحلقية الكبيرة" للحصول على الورقة الكاملة بصيغة PDF
الإجراءات التجريبية
مجموعة البيانات:توسيع نطاق بيانات مجموعة بيانات ChEMBL
في البداية، جمع الباحثون 18,357 مركبًا حيويًا حيويًا نشطًا من قاعدة بيانات ChEMBL وقاموا بفحصها. بعد ذلك، يتم عبور أي رابطتين كيميائيتين للمركب الحلقي الكبير، ويتم تقسيم روابطه للعثور على المركب غير الحلقي المقابل.وأخيرًا، تم الحصول على إجمالي 237,728 زوجًا من المركبات الحلقية الكبيرة-اللاحلقية كمجموعة بيانات لهذه الدراسة..
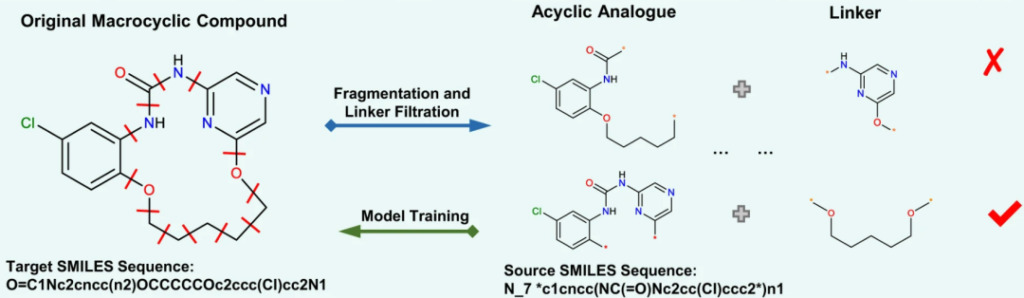
كل مركب لديه تعبير SMILES محدد. ومع ذلك، أظهرت الدراسات الحديثة أنتدريب النموذج باستخدام مجموعة من تعبيرات SMILES العشوائية المتطابقة كيميائيًا ولكنها مختلفة نحويًا، مما يمكن أن يحسن بشكل كبير أداء نماذج التعلم العميق. قام الباحثون بمقارنة البيانات الموسعة بمقدار 2 و5 و10 مرات مع البيانات الأصلية، وأظهرت جميع البيانات تقاربًا جيدًا بعد 50 ألف خطوة.
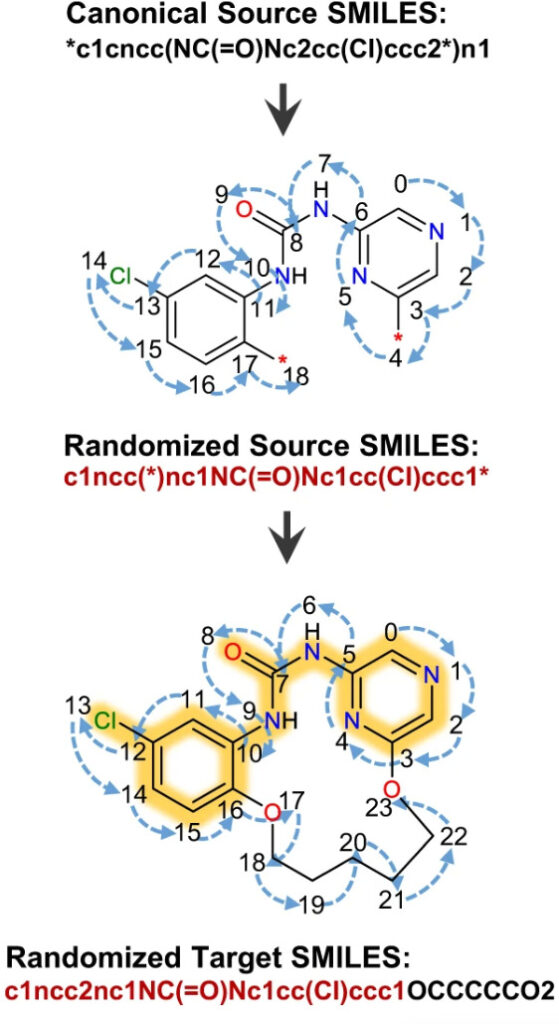
الهندسة المعمارية النموذجية:ترميز وفك تشفير المحولات
يعتمد Macformer على بنية Transformer. يتم تضمين تسلسلات SMILES لكل من المركبات المدخلة والهدف في مصفوفة قابلة للتدريب ويتم ترميزها موضعيًا باستخدام وظائف الجيب وجيب التمام.
يتم إدخال مصفوفة التضمين للمركب المدخل إلى المشفر لتوليد تمثيل كامن لبدء عملية الترميز. تتكون كل طبقة ترميز من طبقة انتباه متعددة الرؤوس وشبكة تغذية أمامية للموضع.
الهدف النهائي لـ Macformer هو تقليل الفجوة بين التسلسل المتوقع وتسلسل الهدف المقابل من خلال دالة فقدان الإنتروبيا المتقاطعة وإخراج المركب الحلقي الكبير المتوقع..

دراسة مقارنة:مجموعات بيانات ChEMBL
قام الباحثون بمقارنة Macformer مع نموذج التعلم غير العميق، MacLS. بعد إدخال مركب غير حلقي، يمكن لكليهما إخراج نظير حلقي كبير. لذلك،سيتم استخدام الصلاحية الكيميائية والحداثة والتفرد للحلقات الكبيرة كمعايير تقييم لأداء النموذج.
وبالمقارنة مع مجموعة البيانات الأصلية، أدى التوسع المزدوج لمجموعة البيانات إلى تحسين الأداء العام للنموذج، وخاصة من حيث معدل الاسترداد (96.09% مقابل 54.85%)، والفعالية (80.34% مقابل 66.74%) وحداثة الموصل (58.91% مقابل 40.56%)، في حين أن التوسع الإضافي لمجموعة البيانات لم يستمر في تحسين أداء النموذج.
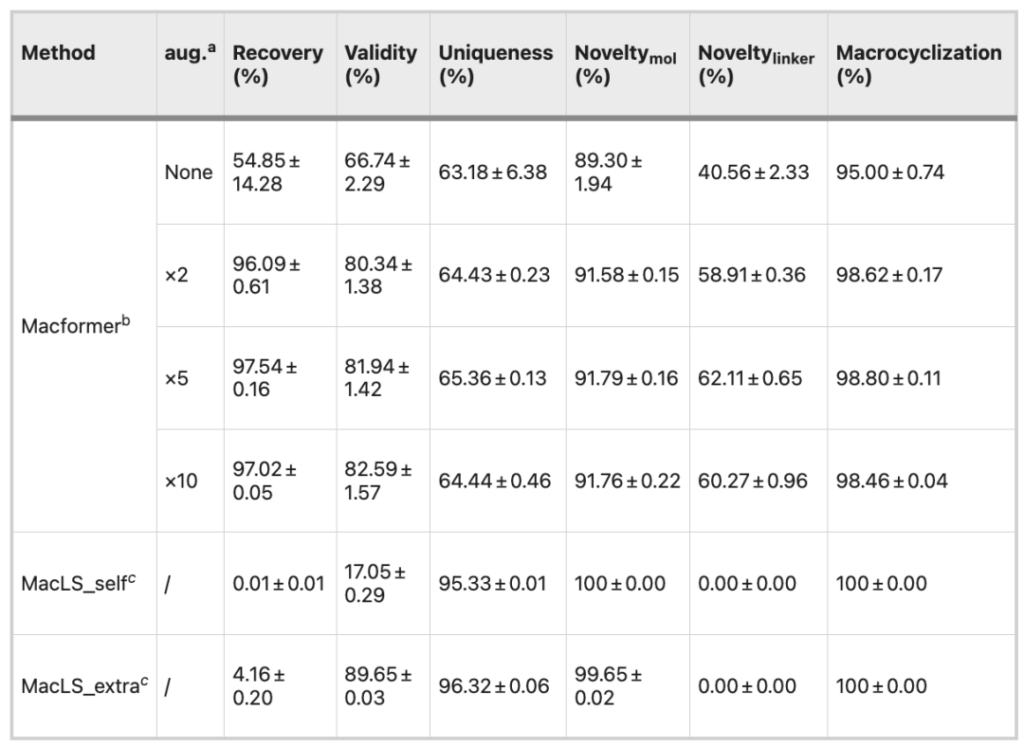
يقوم MacLS_self بإنشاء تكوينات جديدة باستخدام SMILES غير دورية، بينما يستخرج MacLS_extra التكوينات من الهياكل ثلاثية الأبعاد منخفضة الطاقة لدورات الماكرو المستهدفة.
تبلغ فعالية MacLS_self 17.05% فقط، في حين أن حداثة وتميز مركب MacLS_extra يتفوق على مركب Macformer. ومع ذلك، لا يمكن لـ MacLS البحث إلا عن اتصالات من مجموعة التدريب، وبالتالي فإن حداثة الاتصالات هي 0. علاوة على ذلك، فإن معدل استرداد المركبات الحلقية الكبيرة بواسطة MacLS منخفض للغاية أيضًا، أقل من 5%.
دراسة مقارنة:مجموعة بيانات الزنك
علاوة على ذلك، تمت مقارنة النموذجين على مجموعة البيانات الخارجية ZINC. يتمتع نموذج Macformer المدرب بمجموعة بيانات موسعة بمقدار 5 أضعاف بمعدل استرداد يزيد عن 80%، وفعالية تزيد عن 84%، وحداثة تزيد عن 99%.تظهر النتائج أعلاه أن Macformer يتمتع بقدرة تعميم ممتازة بعد توسيع البيانات.
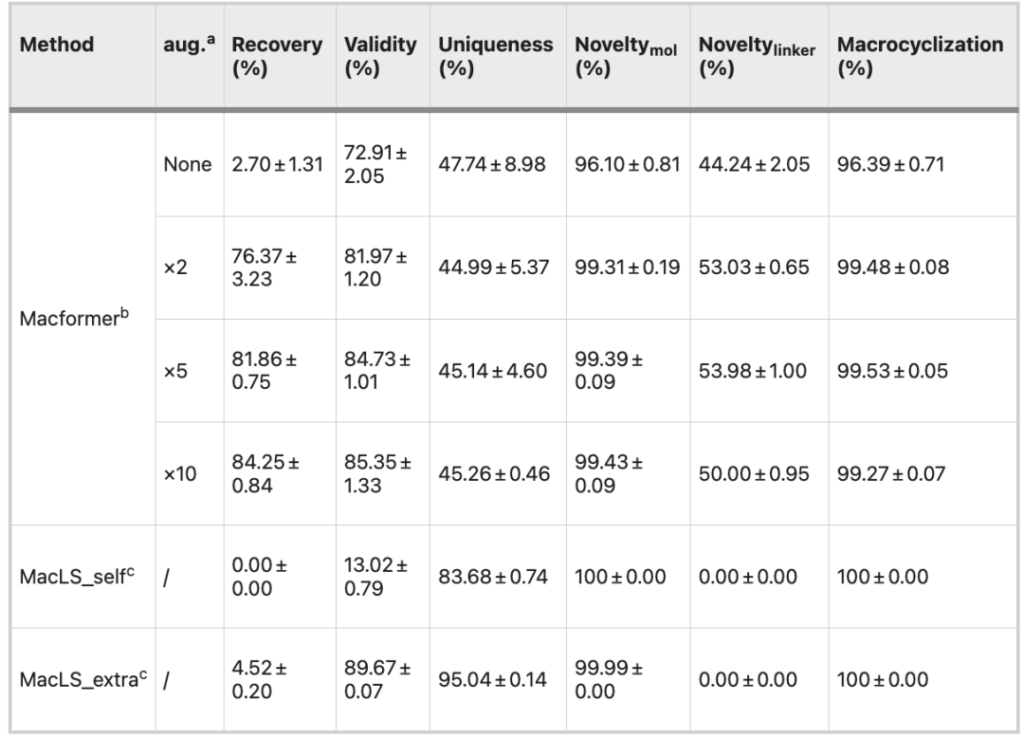
نظرًا لأن MacLS لا يتمتع بقدرة التعلم التي يتمتع بها Macformer، فإن نتائجه على مجموعات البيانات المختلفة متشابهة بشكل أساسي.
التوزيع الكيميائي:Macformer يشبه الإدخال أكثر
بغض النظر عن حداثة الرابط، يتمتع كل من Macformer وMacLS بالقدرة على إنشاء دورات كبيرة جديدة. ولذلك، قام الباحثون بمقارنة توزيع المركبات التي ينتجها الاثنان في الفضاء الكيميائي.
أولاً، تمت مقارنة أوجه التشابه بين المركبات باستخدام معامل تانيموتو. وبسبب التشابه البنيوي بين المركبات غير الحلقية والمركبات الحلقية الكبيرة، فإن معاملات تانيموتو لمعظم المركبات التي تم إنشاؤها بواسطة النموذج أعلى من 0.7. ومع ذلك، كان التشابه البنيوي للمركبات التي تم إنشاؤها بواسطة Macformer مع المركبات الأصلية أعلى من تلك الموجودة في MacLS_extra.
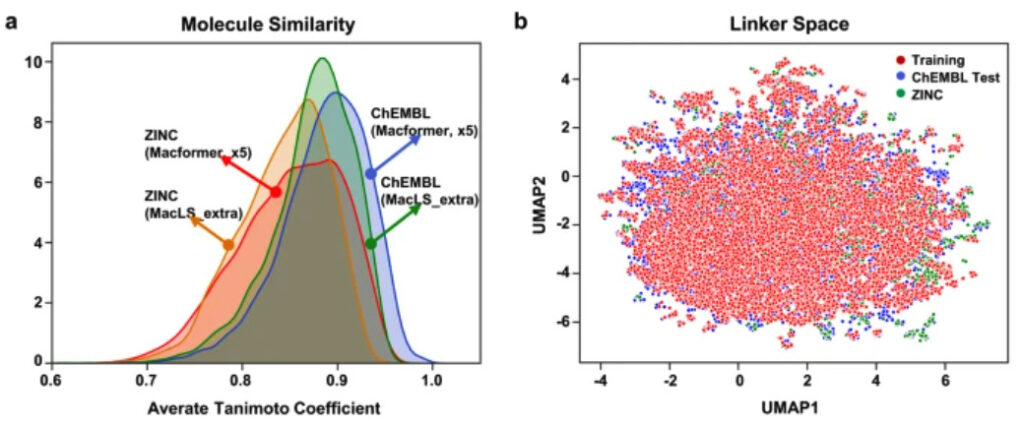
تعتبر هذه النتيجة غير عادية إلى حد ما لأن Macformer قادر على استنتاج الاتصالات غير الموجودة في مجموعة التدريب، في حين أن MacLS لا يمتلك هذه القدرة. ولتحقيق هذه الغاية، استخدم الباحثون خوارزمية التقريب والإسقاط المتعدد الموحد (UMAP) لتقليل أبعاد البيانات. وتظهر النتائج أنيتم توزيع الروابط الجديدة التي تم إنشاؤها بواسطة Macformer بالقرب من مجموعة تدريب ChEMBL..
التحقق التجريبي
تطوير الأدوية:تحويل الفوزوتينيب إلى جزيئات كبيرة
في السنوات الأخيرة، جذبت المركبات الحلقية الكبيرة الكثير من الاهتمام باعتبارها مثبطات كيناز محتملة. وللتحقق من الأداء التنبئي للنموذج، استخدم الباحثون برنامج Macformer لتصميم مثبطات JAK2. ينتمي JAK2 إلى عائلة JAK من الكينازات وهو هدف مهم لعلاج الأورام التكاثرية النقوية والتهاب المفاصل الروماتويدي.
وكان المدخل إلى النموذج هو الفوزوتينيب، وهو دواء جزيئي صغير يستخدم لعلاج التليف النقوي. يتمتع فيلتراتينيب بانتقائية أفضل لـ JAK2 مقارنة بـ JAK kinases الأخرى، لكن انتقائيته ضعيفة للكينازات الأخرى، مما يؤدي إلى آثار جانبية أخرى.
تم ضبط نقاط الارتباط للتكوين الحلقي الكبير على حلقتي الفينيل الطرفيتين، وتم إزالة زانثاميد التيرت بوتيل الذي قد يكون ضارًا عند ملامسته لموقع هدف Asp994. ولزيادة تنوع الأدوية الكبيرة الحلقية المتوقعة، تم توسيع كل تسلسل SMILES المصدري 10 مرات.في النهاية، أنتجت Macformer 10700 نتيجة، بما في ذلك 281 دواءً جديدًا من فئة الأدوية الكبرى الحلقية.
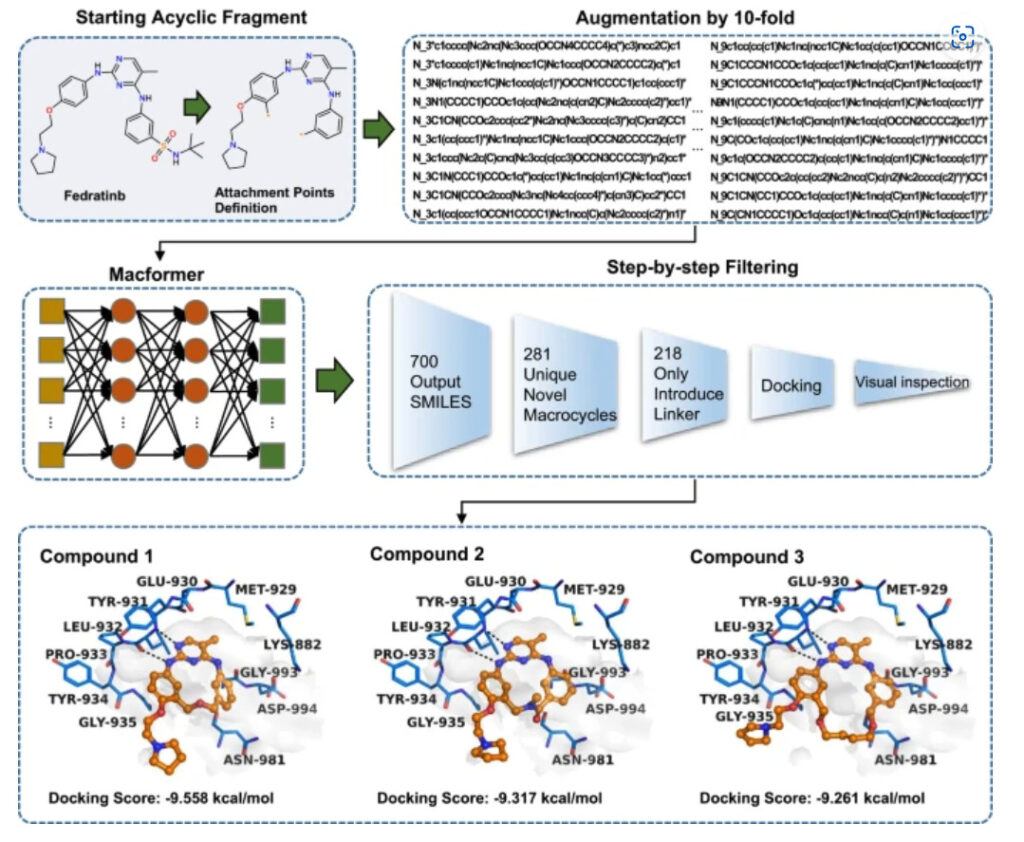
بعد تقييم ارتباط الأدوية الحلقية الكبيرة بالأهداف وإمكانية تصنيعها، اختار الباحثون أخيرًا ثلاثة مركبات لاختبار التقييم الصناعي.ومن بينها، لم يتم الإبلاغ عن رابط المركب 1 في تصميم الأدوية الحلقية الكبيرة أو تطوير مثبطات JAK2..
من بين 300 دواء كبير الحلقات صممته شركة MacLS،لم يتم العثور على هذه المركبات الثلاثة، وهو ما يثبت مرة أخرى إمكانات خوارزميات التعلم العميق في تصميم الأدوية الجديدة.
التقييم المختبري:النشاط على مستوى الإنزيم والخلوية
وبعد ذلك، تم تقييم أنشطة هذه المركبات الثلاثة ضد JAK2.وكانت نصف التركيزات المثبطة (IC50) 0.07 و 0.364 و 0.006 ميكرومولار على التوالي. . تم تقييم المركبات الأكثر فعالية 1 و 3 من حيث الخصوصية عند 100 ميكرومولار، وتم تثبيط 10 و 17 كيناز من النوع البري فقط، على التوالي، في حين تأثر 34 كيناز من النوع البري بالفيريتينيب، مما يشير إلى أن المركبات 1 و 3 كانت أكثر انتقائية.
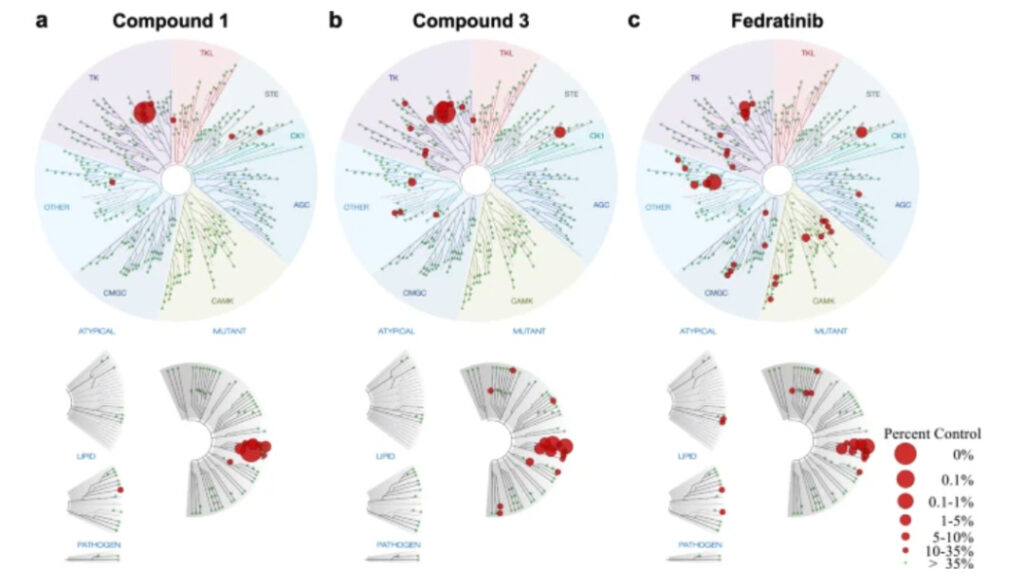
وفي الوقت نفسه، تم أيضًا تقييم الخصائص المضادة للانتشار للمركبات 1-3 ضد الخلايا المعتمدة على JAK2. وتظهر النتائج أنيمكن للمركبات 1 و3 تثبيط تكاثر الخلايا المعتمدة على JAK2 بجرعة أقل من الفوزوتينيب.
التقييم الحيوي:اختبار الحركية الدوائية
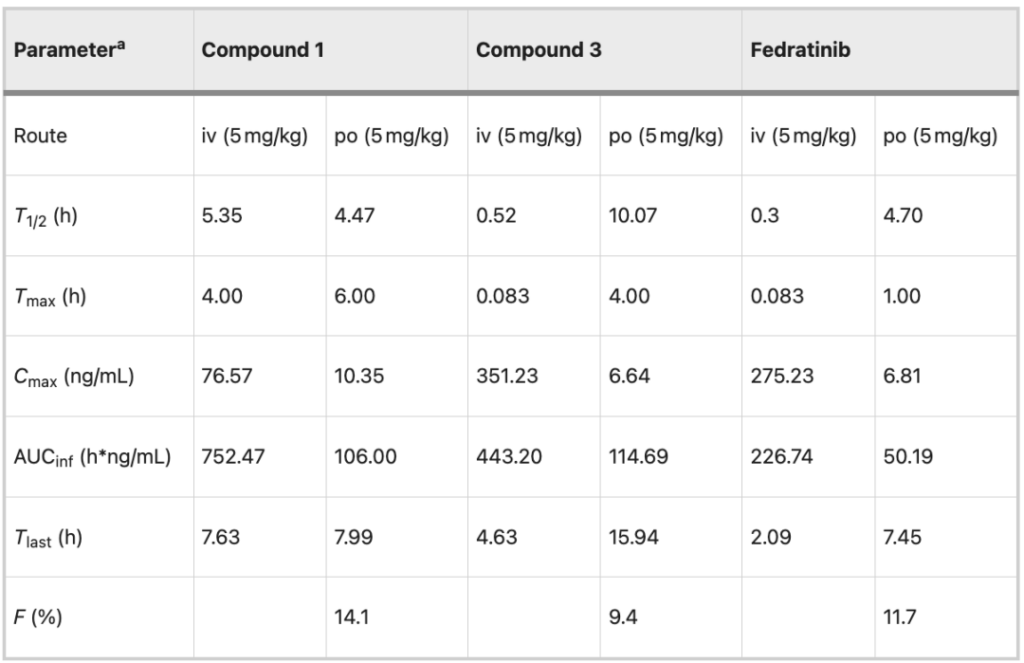
وأخيرًا، تمت دراسة الحركية الدوائية للمركبات 1 و3 والفوزيتينيب بعد الإعطاء الوريدي (5 مجم/كجم) والفموي (5 مجم/كجم).
كان المركب 3 متفوقًا على الفوزوتينيب في جميع الجوانب باستثناء التوافر البيولوجي (9.4% مقابل 11.7%). في الوقت نفسه، يتمتع المركب 1 أيضًا بمزايا في الخصائص الفموية، مثل التعرض الجهازي (106.00 مقابل 50.19 h*ng/mL) والتوافر البيولوجي (14.1% مقابل 11.7%). وتظهر النتائج أعلاه أنإن عملية التدوير الكبيرة مفيدة لتحسين الاستقرار الأيضي للأدوية من نوع الفوزوتينيب.
الاختبار الحيوي:المركب 3 يمنع الالتهاب
لقد تم الإبلاغ عن أن الإفراط في التعبير عن JAK2 يمكن أن يؤدي إلى مرض التهاب الأمعاء (IBD)، مما يعني أن تثبيط نشاط JAK2 قد يكون مفيدًا في علاج مرض التهاب الأمعاء.قام الباحثون باختبار الأدوية الكبيرة الحلقية في نماذج الفئران لتقييم دورها في علاج مرض التهاب الأمعاء.
وفقًا لنتائج اختبار الحركية الدوائية، كانت جرعة فيزوتينيب ضعف جرعة المركب 3. وأظهرت النتائج أن كل من المركب 3 وفيوزيتينيب خفف من فقدان الوزن الناجم عن IDB، وانخفض مؤشر نشاط المرض للمجموعة التجريبية بشكل كبير من اليوم الثامن.
وأخيرا، تم استخدام صبغة HE لتحليل شدة الالتهاب. وأظهرت المجموعة الضابطة استجابة التهابية كبيرة، بما في ذلك تسلل الخلايا الالتهابية وفقدان الخلايا الكأسية، في حين كانت الاستجابة الالتهابية في التجربة أخف وكان هيكل القولون سليما.

وتظهر النتائج أعلاه أن المركبات الحلقية الكبيرة المستنتجة بواسطة ماكفورمر تتفوق على الأدوية التقليدية في الحركية الدوائية والانتقائية، ويمكنها تحقيق علاج المرض بجرعات أقل.
فعالية عالية، تركيب صعب، فرحة وحزن الحلقات الكبيرة
اعتبارًا من عام 2020،وافقت إدارة الغذاء والدواء الأمريكية (FDA) على 67 دواءً من الأدوية الكبيرة الحلقية، وهو ما يمثل 41% من جميع الأدوية المعتمدة. . ومن بينها 59 دواءً طبيعياً من فئة الأدوية الكبيرة الحلقية و8 فقط من الأدوية غير الطبيعية. في عام 2008، وافقت إدارة الغذاء والدواء على أول دواء غير طبيعي من سلسلة كبيرة من الجزيئات، وهو بليكسافور، لعلاج السرطان.
المؤشرات الرئيسية للأدوية ذات الحلقات الكبيرة هي الأمراض المعدية، والتي تمثل 44.4%، تليها الأورام (20.8%) ومضادات الفطريات (8.3%). في السنوات الأخيرة، زاد استخدام الأدوية ذات الحلقات الكبيرة في مجال مكافحة الأورام بشكل كبير. ولم يكن هناك سوى أربعة تشريعات قبل عام 2007، في حين تمت الموافقة على 11 تشريعاً منذ ذلك الحين.

يمكن للأدوية الكبيرة الحلقية أن توفر وظائف متنوعة وهياكل كيميائية معقدة في بنية شبه صلبة ومنظمة مسبقًا، مما قد يزيد من تقارب وانتقائية الأدوية الكبيرة الحلقية للأهداف التي يصعب على الجزيئات الصغيرة التقليدية الارتباط بها، وبالتالي تحسين فعالية الدواء. علاوة على ذلك، فإن بعض الأدوية الكبيرة الحلقية قادرة على تعديل تكوينها للتكيف مع البيئة الخارجية. وتؤدي هذه القدرة إلى زيادة قابليته للذوبان في الماء ونفاذيته للخلايا.
لكن،إن تركيب الأدوية الحلقية الكبيرة معقد للغاية. في حين أن البنية الحلقية الكبيرة تعزز القدرة على الارتباط بأهداف محددة، فإنها تؤدي أيضًا إلى إجهاد الحلقة، والتفاعلات المكانية، والتفاعلات غير التساهمية عبر الحلقات.وهذا يجعل من الصعب التنبؤ بالبنية الجزيئية وخصائصها..
أصبح استخدام الذكاء الاصطناعي في تطوير الأدوية أكثر انتشارًا. ومع ذلك، فإن البيانات المحدودة غالباً ما تحد من أداء الذكاء الاصطناعي. في هذه الدراسة،أجرى الباحثون عملية تكبير البيانات باستخدام تعبيرات SMILES العشوائيةمع ضمان ثراء مجموعة البيانات، تم تحسين أداء التنبؤ الخاص بـ Macformer.
في المستقبل، ومع استمرار تعمق فهم الناس لبنية الدواء وخصائصه، سيكون للذكاء الاصطناعي مستوى أعلى من المشاركة في تطوير أدوية جديدة، مما يحمي صحة الناس.
روابط مرجعية:
[1]https://www.cambridgemedchemconsulting.com/resources/hit_identification/macrocycles/macrocycles.html
[2]https://pubs.acs.org/doi/10.1021/acs.jmedchem.3c00134