Command Palette
Search for a command to run...
Nature誌に掲載されました!華中科技大学は、複数のセンターと専門分野における敗血症性ショックの死亡リスクの正確な予測を達成するための融合戦略AIモデルを提案した。

感染性ショック(敗血症性ショックとも呼ばれる)は、敗血症によって引き起こされる重度の循環障害と細胞代謝障害の症候群を指し、臨床症状においては敗血症の進行の「末期段階」とみなすことができます。敗血症性ショックの死亡率は極めて高く、現在、集中治療室で最も致命的な病気の一つです。英国の国立集中治療データベースに基づく研究報告によると、敗血症性ショックの患者の院内死亡率は 55.5% にも達する可能性がある。
死亡率の高い進行性の病気に直面して、敗血症性ショックに対する臨床的重点は「時は命なり」であり、死亡率を下げるために早期発見、早期介入、早期治療が提唱されています。しかし、敗血症性ショック患者の病状の複雑性と臨床医学データの不足により、敗血症性ショック患者の病状の進行を早期に警告することは非常に困難です。これは、敗血症が敗血症性ショックに悪化するのを効果的に阻止するための重要なボトルネックでもあります。
現在、集中治療医療における情報技術の深化に伴い、人工知能と集中治療医療の相互統合により敗血症の早期警告は困難ではなくなりましたが、敗血症性ショックに関する研究は遅れています。これは、ほとんどの研究がサンプル数が少なく、単一の機械学習アルゴリズムに依存しており、多施設検証に合格していないため、敗血症性ショックの患者の早期リスク予測の臨床実践に推進することが困難であるためです。
こうした状況を踏まえ、華中科技大学同済医学院付属同済病院の葉青教授と医療健康管理学院の呉紅教授は、ICUにおける敗血症性ショックの患者の28日以内の死亡リスクを予測するために、TOPSIS(理想解との類似性による順序選好法)に基づく分類融合(TCF)モデルを開発しました。このモデルは 7 つの機械学習モデルを統合しており、専門家間および多施設検証において高い安定性と精度を備えています。これは、敗血症性ショックによる死亡リスクを早期に警告するための信頼性の高い補助ツールを臨床医に提供します。
研究結果は、「多施設遡及研究における敗血症性ショックに対する人工知能ベースの多専門分野死亡率予測モデル」というタイトルで、Natureの関連誌npj Digital Medicineに掲載されました。
研究のハイライト:
* この研究では、複数の基本分類モデルに基づいて、高い一般化能力と堅牢性を備えた融合モデルを構築するための効率的な融合戦略を採用し、臨床シナリオにおける小規模サンプルコホートと単一分類モデルのパフォーマンスが低い問題を克服しました。
* この研究結果は、敗血症性ショックにおける早期死亡リスクの予測の難しさに画期的な進歩をもたらし、医師が患者の病状の進行を早期に綿密に監視し、より積極的な治療措置を講じるのに役立つ、効率的で安定した信頼性の高い臨床意思決定ツールを臨床医に提供しました。

用紙のアドレス:
https://go.hyper.ai/faMLL
オープンソース プロジェクト「awesome-ai4s」は、100 を超える AI4S 論文の解釈をまとめ、大規模なデータ セットとツールを提供します。
https://github.com/hyperai/awesome-ai4s
データセット: 膨大なデータ、正確な処理
広範囲に適用可能な敗血症性ショック予測モデルを構築するために、研究チームは、2003年2月から2023年11月までの3つの病院のICUの敗血症性ショック患者4,872人の臨床データを統合した。参加者の背景は複雑かつ多様であるため、研究チームは多施設、専門分野間の検証を実施し、モデルの有効性と適用性を実証するのに役立ちます。次の図に示すように:
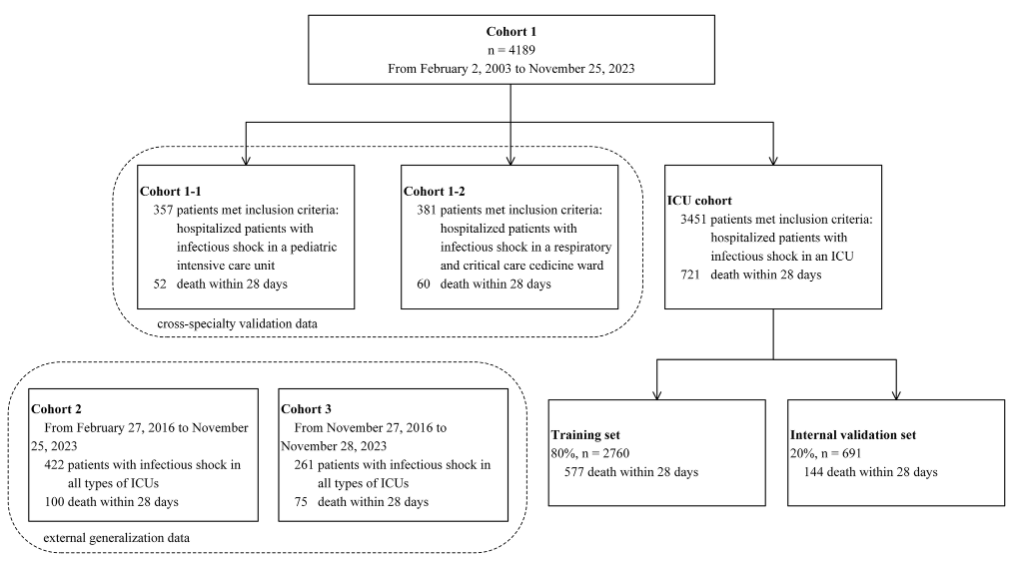
具体的には、コホート 1 には 4,189 人の参加者が含まれていました。そのうち、一般集中治療室には3,451人の患者が入院しており、そのうち陽性者721人、陰性者2,730人であった。小児ICU(コホート1-1)の患者357人(陽性52人)呼吸器ICU(コホート1-2)の患者381名(陽性60名)
* 陽性結果は、ICU入院後28日以内に全死因死亡を経験した参加者であり、全死因死亡を経験しなかった参加者は陰性結果とマークされています(以下同じ)
その中で、一般的な ICU 患者のデータセットが主な研究対象集団として、またモデル構築と内部検証に使用されました。トレーニング データと検証データは 8:2 に分割され、それぞれ 2,760 人の被験者 (陽性 577 人) と 691 人の被験者 (陽性 144 人) になりました。小児 ICU 患者と呼吸器 ICU 患者のデータセットでは、さまざまな専門集中治療室におけるモデルの適用性と安定性がさらに評価されました。
コホート 2 とコホート 3 には、異なる ICU の敗血症性ショックの患者が含まれ、それぞれ 422 人 (陽性 100 人、陰性 322 人) と 261 人 (陽性 75 人、陰性 186 人) が参加しました。データセットのこれら 2 つの部分は、主に、さまざまなセンターでの一般化能力と有効性を評価するための外部検証に使用されます。
さらに、正確な実験結果を得るために、研究チームは93の共通の臨床的特徴を抽出した。人口統計情報、病歴や治療歴、バイタルサイン情報などを含め、最終的に実験用に 34 項目に最適化されました。
具体的には、データの前処理は 5 つの部分から構成されます。最初のステップでは、研究チームはまず欠損率を計算し、欠損率が30%より高い23の変数を削除しました。第2段階では、ベルヌーイの分散公式に従ってブール特徴の分散を計算し、一貫性が90%を超える離散ランダム変数を再度削除しました。 3番目のステップでは、欠損値補間法(ロジスティック回帰多重補間)を使用して、さらに61個の変数に最適化しました。 4番目のステップでは、相関の高い特徴(ピアソン相関係数≥ 0.7)が再度スクリーニングされ、この時点で50個の変数が残りました。次の図に示すように:
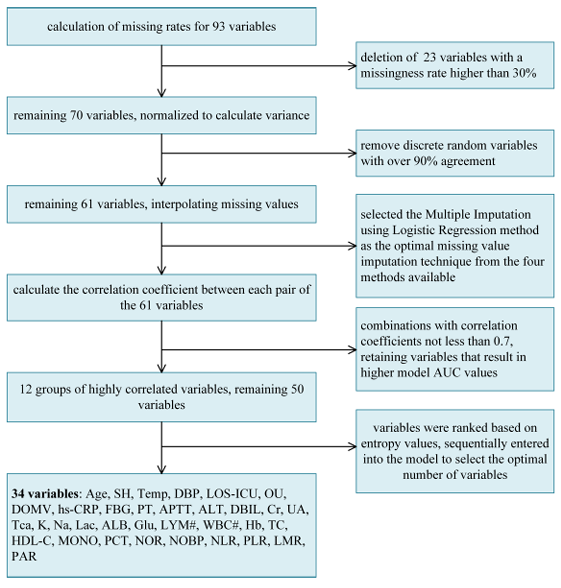
第 5 ステップでは、研究者らは情報エントロピー (高から低) に応じて変数を分類し、最終的に年齢、手術歴、体温、拡張期血圧などの重要な要素を含む、実験の主要変数 34 個を選択しました。
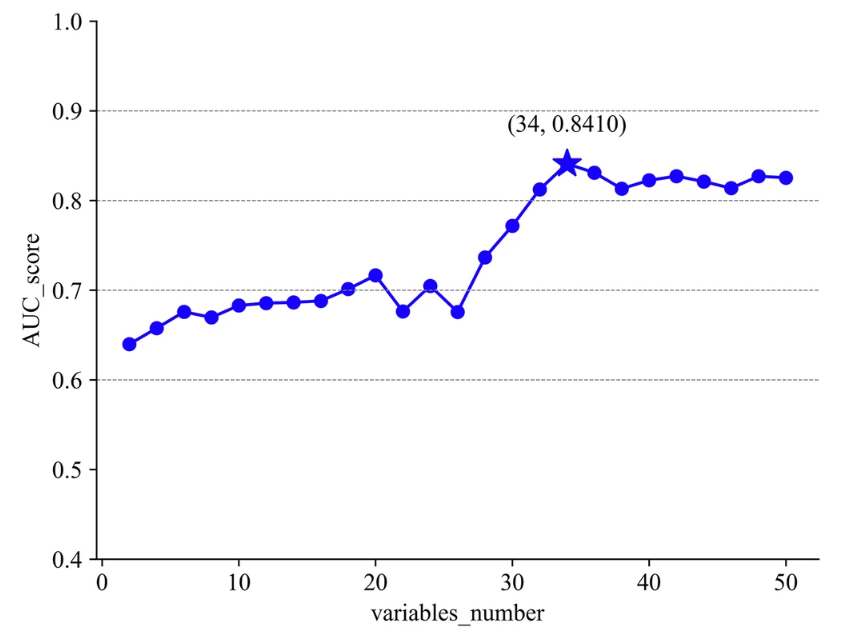
なお、参加者のプライバシーを保護するため、分析前にすべてのデータが匿名化されました。
モデルアーキテクチャ:融合モデル、正確な予測
TCF モデルの研究は主に 3 つのステップに分かれています。最初のステップは、敗血症性ショックの患者の入院データを使用して 7 つのサブモデルを確立し、各サブモデルで 6 つの評価指標の結果を生成することです。 2 番目のステップは、融合戦略に基づいてサブモデルを融合モデルに統合し、そのモデルが他のモデルよりも優れていることを確認することです。 3 番目のステップでは、さまざまなデータ セットにわたってテストを行い、モデルのパフォーマンスを検証し、モデルの解釈可能性分析を実行します (実験結果のセクションで説明されています)。
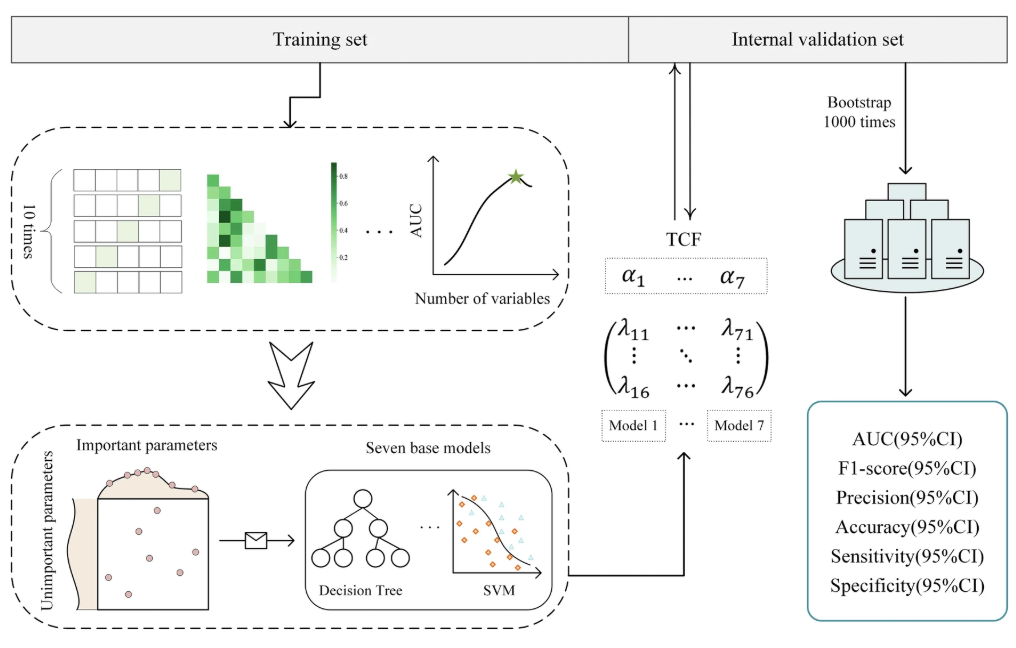
具体的には、最初のステップとして、研究チームはまず、特徴処理された共通 ICU データセットを使用して 7 つのサブモデルをトレーニングおよびテストしました。クラスの不均衡による悪影響を軽減するために、1:1 ルールに従って合成少数オーバーサンプリング手法 (SMOTE) をトレーニング セットに適用しました。最小最大正規化後、5 段階のクロス検証とランダム検索によって最適なパラメータの組み合わせが決定され、トレーニング セットで 7 つのサブモデル (決定木 (DT)、ランダム フォレスト (RF)、XGBoost (XGB)、LightGBM (LGBM)、ナイーブ ベイズ (NB)、サポート ベクター マシン (SVM)、勾配ブースティング決定木 (GBDT)) がトレーニングされました。
最後に、研究チームは内部検証データを使用してテスト結果を検証しました。モデルのパフォーマンスは、6 つの評価指標を使用して評価されます。これらは、ROC曲線下面積(AUC)、F1スコア、精度(PRE)、正確度(ACC)、感度(SEN)、特異度(SPE)です。
第二段階では、研究チームは、それぞれ長所と短所を持つこれら 7 つのサブモデルを統合しました。TOPSIS ベースの分類融合モデル TCF は、7 つのモデルの評価結果を組み合わせて、敗血症性ショックの診断のための包括的な予測結果を提供するように設計されました。サブモデルの重みはTOPSISスコアによって計算され、重み付けされた予測確率がTCFの予測確率となりました。 TCF の分類結果は、0.5 を臨界値として導出されました。
具体的な TCF モデル融合アルゴリズムは次のとおりです。
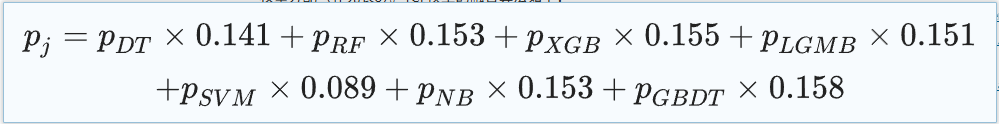
統計分析の観点では、連続的な特徴については、中央値、上位四分位数、下位四分位数の統計が与えられます。個別の機能については、各カテゴリの割合が報告されます。この研究では、最小のデータセットはコホート 3 であり、中心極限定理によれば、連続特徴の平均分布は正規分布であると考えられます。
それから、この研究では、2 つのデータセット間の特性の均一性を判断するために、Levene 検定を使用しました。離散的特徴における他のデータと内部検証セットとの差を比較するためにカイ二乗検定が使用され、連続的特徴における差は独立標本t検定またはウェルチt検定を使用してテストされ、1,000個のブートストラップサンプルを使用して評価指標の95%信頼区間が計算されました。
モデルの推論プロセスをより深く理解するために、研究チームは、SHAP 特徴重要度ヒートマップを描画して特徴重要度を視覚化しました。次の図に示すように、最高の AUC パフォーマンスを備えた GBDT モデルを例に挙げます。
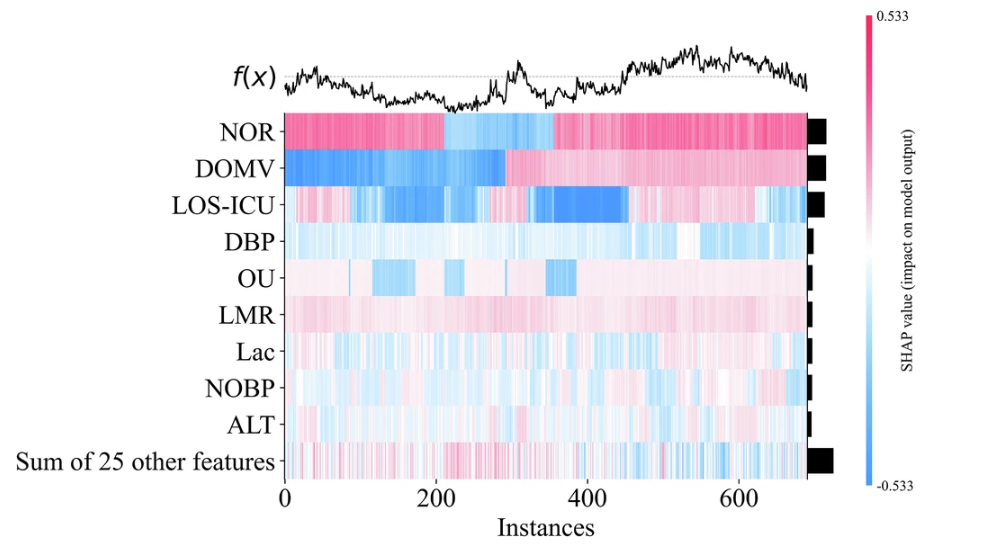
特徴重要度のランキング付けは、臨床予測モデルの透明性と信頼性を向上させるだけでなく、医療実践にとって貴重な参考資料を提供することもできます。このようにして、このモデルは、モデルの透明性に対する医師の要求を満たすだけでなく、臨床上の純利益を定量化します。臨床的解釈可能性と実用性の両方を実現し、臨床実践におけるモデルの適用の基盤を築きます。
実験結果:多次元検証、信頼性が高く使いやすい
融合モデル (TCF) の性能を検証するために、研究チームはまずそれをサブモデルと比較しました。結果は下の図に示されています。
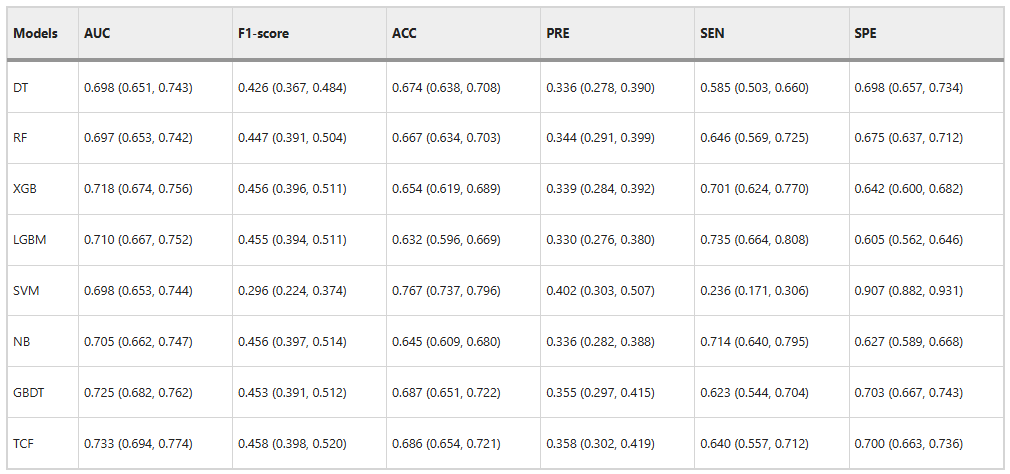
TCF は、内部検証セットの両方の包括的な評価指標においてサブモデルを上回ります。AUC は 0.733、F1 スコアは 0.458 です。さらに、ACC は 0.686、PRE は 0.358 と、ほとんどのサブモデルよりも高くなっています。これは、その優れた分類能力を示しています。
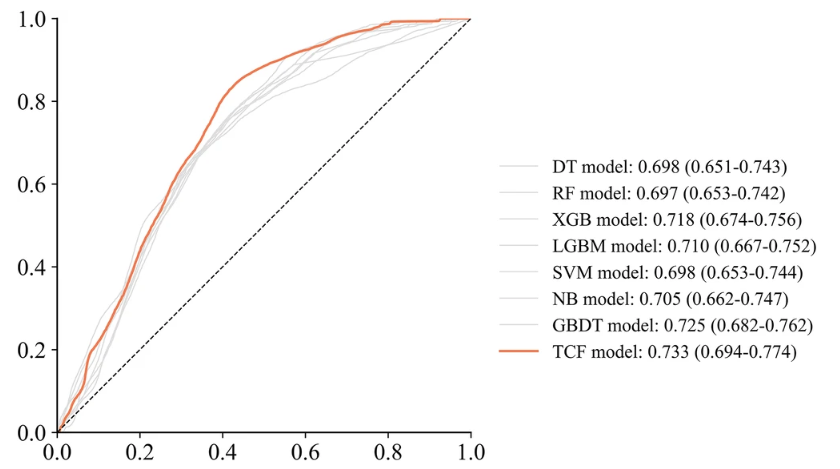
TCFモデルのSENとSPEのスコアは、それぞれ0.640と0.700という最高のパフォーマンスほど良くはないが、しかし、サブモデル全体の偏差を通じて効果を識別できるため、全体的に最高のパフォーマンスを実現できます。以下に示すように。
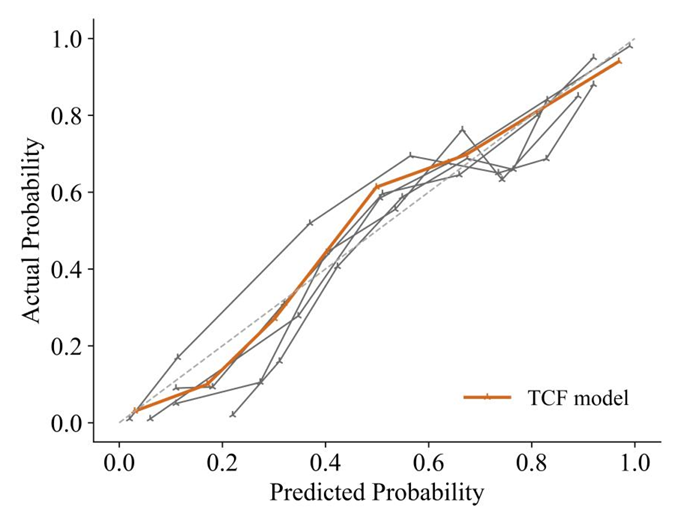
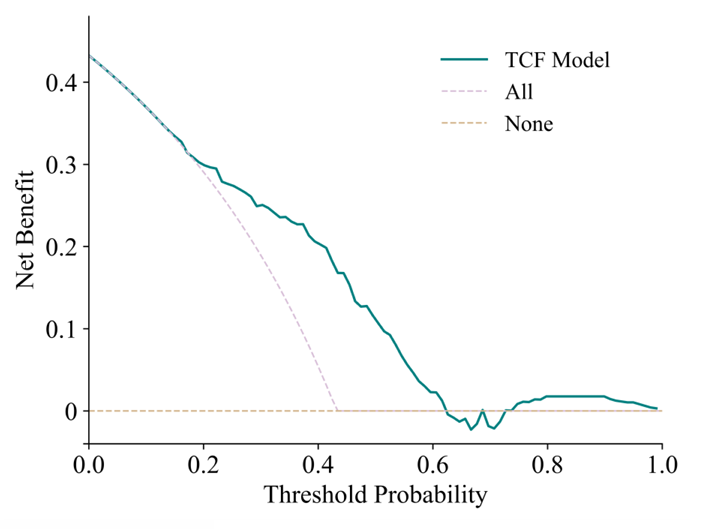
較正曲線と決定曲線分析 (DCA) 曲線は、TCF モデルの予測結果が実際の結果と一致していることを示しています。まず、TCF モデルのキャリブレーション カーブは対角線に最も近いため、すべてのモデルの中で最も優れたキャリブレーション パフォーマンスを備えていることがわかります。 2 番目に、TCF モデルの曲線は、ほとんどの閾値確率、特に 0.1 ~ 0.5 の確率範囲において、「すべて」および「なし」戦略よりも常に優れており、より高い純収益を示します。これは、TCF モデルが一定の範囲内で潜在的な臨床応用価値を持ち、臨床医がより好ましい判断を下すのに役立つ可能性があることを示唆しています。
その後、研究チームは多施設検証を実施し、TCF モデルの予測性能と異なるデータ セット間の異質性をより正確に実証することができました。次の図に示すように:
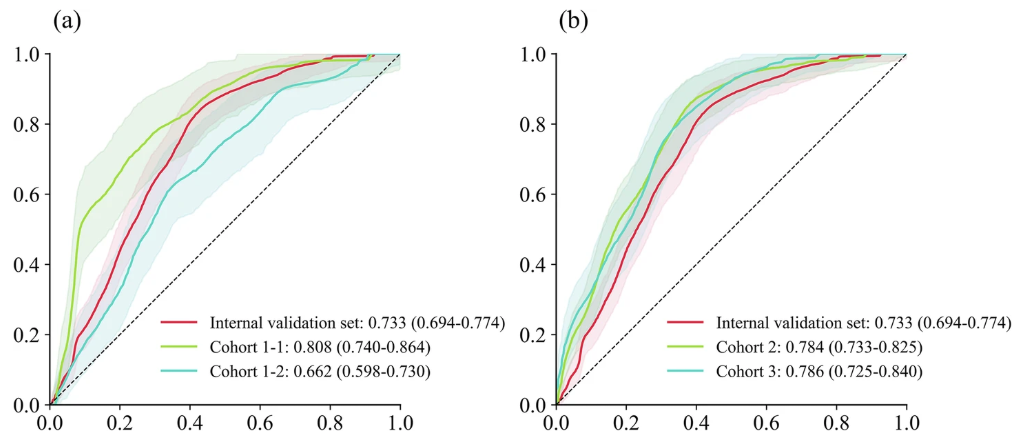
多施設予測効果がトレーニングセットや内部検証セットよりもわずかに低いほとんどの研究とは異なり、この研究では、コホート1-2(呼吸器ICU患者データセット)のAUC(0.662)のわずかな減少を除いて、コホート 1-1 (小児 ICU 患者データセット)、コホート 2、コホート 3 の AUC はすべて改善しました。それぞれ 0.808、0.784、0.786 です。
さらに、多施設サンプル数が限られているため、研究チームは、予測のために 4 つの外部検証データセット (陽性症例 287 件を含む 1,421 件の患者データ) を具体的に組み合わせました。AUC は 0.7705 であり、TCF モデルは敗血症性ショックの危険因子が低い患者を効果的に区別でき、優れた較正能力を備えていることが示されました。
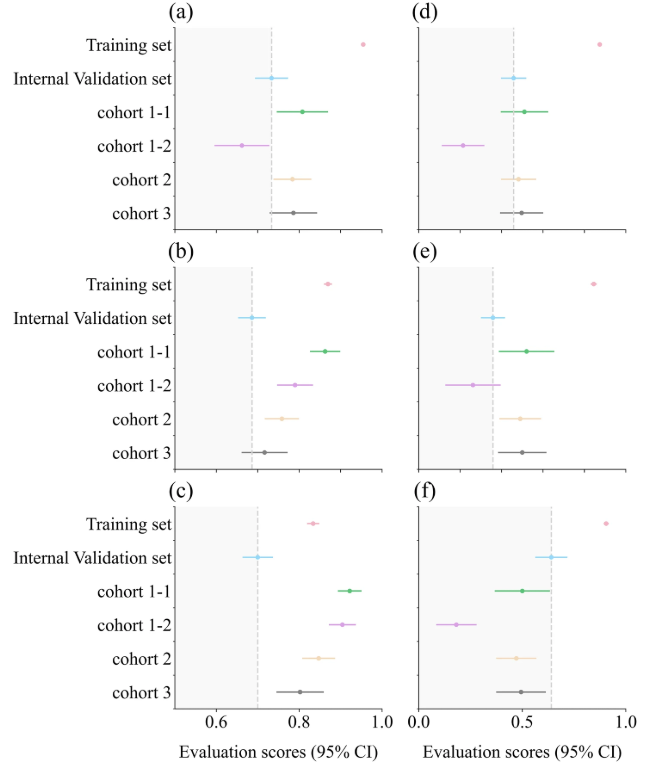
このうち、a は AUC ボックス プロットです。 b は ACC ボックス プロットです。 c は SPE ボックス プロットです。 dはF1スコアボックスプロットです。 eはPREボックスプロットです。 f は SEN ボックス プロットです。灰色の破線は内部検証セットの結果を示しており、他のデータセットの評価スコアは濃い灰色の領域内に収まっており、内部検証セットと比較してパフォーマンスが低下していることを示しています。
要約すると、TCF モデルは内部データセットと外部検証セットの両方で一貫した良好なパフォーマンスを達成し、敗血症性ショックの患者の 28 日以内の死亡リスクの予測において単一モデルよりも優れたパフォーマンスを示しました。このモデルは、特に患者の状態が悪化する重要な初期段階において、ICU の臨床医に信頼性が高く使いやすい予測ツールを提供します。これにより、医師はさまざまな患者に対して効果的で個別化された治療介入を提供し、患者の予後を改善することができます。
敗血症/敗血症性ショックの治療において人工知能が大きな役割を果たす
科学技術の継続的な発展に伴い、人工知能と救命医療の相互統合は、長い間、関係する研究者にとって大きな関心事となっている。この研究は間違いなく先駆的な価値のある探究である。前述のように、敗血症/敗血症性ショックは死亡率と罹患率が高い世界的な公衆衛生危機であり、患者の生存率を向上させるためには早期発見と介入が緊急に必要とされています。
これまで、敗血症の早期警告モデルに関する研究はすでに盛んに行われており、多くの研究室が関連する研究成果を発表しています。
たとえば、Armando D Bedoya らが発表した「敗血症の早期検出のための機械学習: 内部および時間的検証研究」というタイトルの研究があります。アメリカのデューク大学から。ディープラーニング(多重出力ガウス過程とリカレントニューラルネットワーク)をベースにした予測モデルMGP-RNNを紹介し、検証します。ランダムフォレスト、Cox回帰、ペナルティ付きロジスティック回帰の3つの機械学習手法と3つの臨床スコアと比較したところ、このモデルはすべての指標において他のモデルや臨床スコアを上回り、敗血症を5時間前に検出できました。
用紙のアドレス:
https://pmc.ncbi.nlm.nih.gov/articles/PMC7382639
さらに、Dascenaというカリフォルニアの企業のチームも、遡及的な調査方法を用いた研究で洞察を発表しました。MIMIC II 臨床データベースの 32,000 人の患者のデータを使用し、9 つの一般的なバイタル サインの測定値を相関させることで、InSight と呼ばれる敗血症の早期警告アルゴリズムが開発されました。結果によると、このアルゴリズムは持続性全身性炎症反応症候群(SIRS)の発症3時間前に敗血症を予測する際の感度は0.90、特異度は0.81であり、既存のバイオマーカー検出法よりも優れていることが示されました。この研究は「敗血症の早期検出への計算的アプローチ」というタイトルで発表されました。
用紙のアドレス:
https://www.sciencedirect.com/science/article/abs/pii/S0010482516301123?via%3Dihub
人工知能と救命医療の統合により、敗血症の早期警告はもはや困難ではなくなり、この研究は、敗血症が重篤な段階にまで進行したときにタイムリーな警告が得られないというギャップを埋めるものであり、医学的価値の高い研究である。もちろん、より重要なのは、この研究で言及されている融合戦略であり、これはサブモデルの感度と特異性の利点のバランスをとることで、モデル全体の全体的なパフォーマンスを向上させます。これにより、将来的にはマルチモデル統合を通じて関連する問題を解決するための道が開かれ、同様の方法を通じて医療シナリオにおける実際的な困難を解決するためのさらなる研究が促進されます。