Command Palette
Search for a command to run...
Das MIT Nutzt Das Chemprop-Modell, Um Die Menschliche Alterungsuhr Zu Verlangsamen Und Zelluläre Anti-Aging-Verbindungen Zu Entdecken, Die Sowohl Wirksam Als Auch Sicher Sind
Inhalte im Überblick: Vom glamourösen Star bis zum einfachen Menschen in Zivil – jeder wird unweigerlich alt, erlebt Veränderungen im Aussehen und eine Verschlechterung der körperlichen Funktionen. Aus diesem Grund versuchen die Menschen auch, das Geheimnis zu finden, wie sich die Alterung verzögern lässt. Allerdings gehen mit den bestehenden Anti-Aging-Medikamenten immer auch einige Nebenwirkungen einher. Kürzlich wurden in einem in „Nature Aging“ veröffentlichten Forschungsergebnis mithilfe von Deep Learning hochwirksame und sichere Anti-Aging-Medikamente herausgefiltert, die uns der „Unsterblichkeit“ einen Schritt näher bringen könnten.
Schlüsselwörter:Computermodelle Maschinelles Lernen Altern
Autor: Setsuna
Herausgeber|Sanyang
Dieser Artikel wurde zuerst auf der öffentlichen HyperAI WeChat-Plattform veröffentlicht~
Jonathan Swift sagte einmal:Jeder möchte länger leben, aber niemand wird gerne alt.Eine in Nature Medicine veröffentlichte Studie zeigte jedoch, dass zu drei Zeitpunkten, nämlich im Alter von 34, 60 und 78 Jahren, die Genexpression altersbedingter Krankheiten im menschlichen Körper hochreguliert ist, was zu einer „klippenartigen Alterung“ des menschlichen Körpers führt. Das bedeutet, dassDer menschliche Körper altert möglicherweise früher und schneller als wir denken.Wie man für immer jung bleibt, ist wieder einmal ein heißes Thema.
In den letzten Jahren haben Experimente gezeigt, dass Anti-Aging-MedikamenteDie Eliminierung seneszenter Zellen (Snc) im Körper kann die pathophysiologischen Folgen der Zellseneszenz verbessern,Es verlängerte sogar die Lebensdauer von Mäusen. Jedoch,Diese Medikamente haben eine Reihe von Nebenwirkungen,Hierzu zählen eine verlangsamte Wundheilung und die Entstehung einer Fibrosierung der Zellen im Bereich der Lunge und der Blutgefäße. Es ist schwierig, sowohl Wirksamkeit als auch Sicherheit zu erreichen.
Zu diesem Zweck haben Felix Wong et al. vom Massachusetts Institute of Technology (MIT)Durch Deep Learning und Graph-Neural-Netzwerke haben wir aus Hunderttausenden von Verbindungen sichere und wirksame Anti-Aging-Inhaltsstoffe herausgefiltert.Seine Wirksamkeit und Sicherheit wurden an Mäusen überprüft. Die Forschungsergebnisse wurden im Mai 2023 in Nature Aging unter dem Titel „Discovering small-molecule senolytics with deep neural networks“ veröffentlicht.

Die Forschungsergebnisse wurden in der Zeitschrift Nature Aging veröffentlicht
Papieradresse:
https://www.nature.com/articles/s43587-023-00415-z
Experimentübersicht
Die Forscher filterten zunächst aus einigen bestehenden Medikamenten Medikamente mit Anti-Aging-Wirkung als Trainingsdaten für Deep Learning heraus und schlugen Indikatoren zur Messung ihrer Wirksamkeit und Sicherheit vor. Dann,Basierend auf dem Chemprop-Modell (einem neuronalen Netzwerkmodell für Nachrichtenausbreitungsgraphen) filterten sie hochwirksame und sichere Anti-Aging-Medikamente heraus.Nach weiteren Untersuchungen wurden drei Verbindungen erhalten und ihre Anti-Aging-Eigenschaften und Biosicherheit mit herkömmlichen Anti-Aging-Medikamenten verglichen und überprüft.
Datensatz
Der Datensatz für diese Studie besteht aus zwei Teilen: 5.819 Medikamente, die vom Broad Institute Drug Repurposing Center gesammelt wurden, und 799.140 Verbindungen, die vom Broad Institute gesammelt wurden.
Experimentelle Verfahren
Dieses Experiment umfasst im Wesentlichen 3 Schritte:
1. Aus den 2.352 von der US-amerikanischen FDA zugelassenen und in klinischen Tests befindlichen Medikamenten diejenigen mit Anti-Aging-Wirkung herausfiltern, die als Trainingsdatensatz für das Modell dienen;
2. Screening von Anti-Aging-Medikamenten durch das Chemprop-Modell;
3. Die drei herausgesuchten repräsentativen Verbindungen wurden mit dem herkömmlichen Anti-Aging-Medikament ABT-737 verglichen, um ihre Anti-Aging-Eigenschaften und ihre biologische Sicherheit zu überprüfen.
Screening-Prozess
Anti-Aging-Medikamente müssen die folgenden drei Indikatoren erfüllen:
1. Die relative Aktivität normaler Zellen nach der medikamentösen Behandlung beträgt > 0,7
2. Die relative Aktivität seneszenter Zellen liegt unter 0,5
3. Das Aktivitätsverhältnis von seneszenten Zellen zu normalen Zellen beträgt weniger als 0,7
Basierend auf diesen drei Kriterien untersuchten die Forscher zunächst 45 Medikamente mit Anti-Aging-Eigenschaften aus von der FDA zugelassenen und in klinischen Tests befindlichen Arzneimitteln als Trainingsset für das Chemprop-Modell.
Das Chemprop-Modell weist eine extrem hohe Arzneimittelselektivität auf.Der Bereich unter der Präzisions-Recall-Kurve (PR-Kurve) (AUC) beträgt 0,24 und ist damit deutlich höher als beim Zufallsmodell (0,019) und auch höher als beim Random-Forest-Modell (0,15).
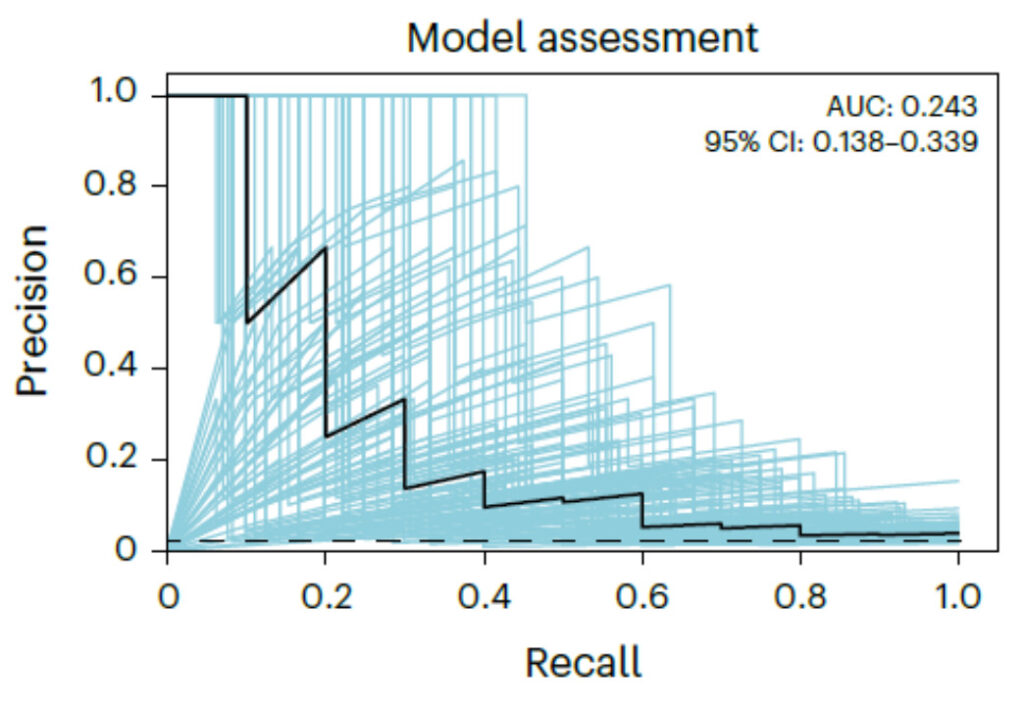
Abbildung 1: PR-Kurve im Chemprop-Modelltraining
Die blaue Linie ist das Ergebnis des Chemprop-Modells und die schwarze Linie das Ergebnis der manuellen Überprüfung.
95% Konfidenzintervall: 0,138-0,339
Angesichts der hervorragenden Leistung des Chemprop-Modells verwendeten die Forscher Chemprop, um die Verbindungen im Datensatz zu screenen. Zu den im Drug Repurposing Center des Broad Institute enthaltenen Medikamenten gehören unter anderem:Es gibt 284 Vorhersagen mit Werten über 0,1. Zu den im Broad Institute erfassten Verbindungen gehörenEs gibt 2.537 Verbindungen mit vorhergesagten Werten (PS) über 0,4 und 3.838 Medikamente mit sehr niedrigen vorhergesagten Werten.Es ist ein Medikament ohne Anti-Aging-Eigenschaften.

Abbildung 2: Ergebnisse des Chemprop-Screenings zu Anti-Aging-Verbindungen
Grün: Medikamente vom Broad Drug Repurposing Center, die möglicherweise Anti-Aging-Eigenschaften haben (PS > 0,1);
Schwarz: Im Broad Institute enthaltene Verbindungen, die möglicherweise Anti-Aging-Eigenschaften haben (PS > 0,4);
Gelb: Verbindungen, bei denen später nachgewiesen wurde, dass sie Anti-Aging-Eigenschaften haben;
Lila: Verbindungen, denen keine Anti-Aging-Eigenschaften vorhergesagt werden;
Rot: Verbindungen mit Anti-Aging-Eigenschaften in den Trainingsdaten;
Blau: Verbindungen ohne Anti-Aging-Eigenschaften in den Trainingsdaten.
Basierend auf der chemischen Struktur und den pharmakokinetischen Eigenschaften hat das Forschungsteam diese Verbindungen weiter untersucht.Zunächst wurden PAINS (Pan-Screening Interfering Compounds) und Chemikalien entfernt, die sich nachteilig auf die pharmakokinetische Leistung auswirken. Anschließend wählten sie 216 Verbindungen mit einer Tanimoto-Ähnlichkeit von weniger als 0,5 aus und unterschieden sie strukturell von bekannten Anti-Aging-Medikamenten. Gleichzeitig wählten sie 50 Medikamente ohne Anti-Aging-Eigenschaften als Negativkontrollen aus. Abschließend überprüften die Forscher die Anti-Aging-Eigenschaften dieser 266 Verbindungen mit chemischen Methoden.
Von den 216 Verbindungen, die hohe Punktzahlen erzielten, zeigten 25 in Experimenten Anti-Aging-Eigenschaften. Die positive Vorhersagerate des Chemprop-Modells beträgt 11,61 TP3T und ist damit höher als die 1,91 TP3T beim manuellen Screening.Allerdings hatte keine der 50 negativen Kontrollverbindungen Anti-Aging-Eigenschaften, was darauf hindeutet, dass das Chemprop-Modell bei der negativen Vorhersage gut abschnitt.

Abbildung 3: Chemprops Vorhersagegenauigkeit
Vergleichende Überprüfung
Nachdem die Forscher die Zielverbindung erhalten hatten, verglichen sie sie mit vorhandenen Anti-Aging-Medikamenten. Zunächst wurde ein Modell seneszenter Zellen aus mit Etoposid behandelten menschlichen Lungenfibroblasten (IMR-90) konstruiert.Die Zellen wurden dann mit den gescreenten Medikamenten BRD-K20733377, BRD-K56819078 und BRD-K44839765 behandelt und mit dem herkömmlichen Medikament ABT-737 verglichen.
In den Ergebnissen können wir sehen, dassDie vom Graph-Neural-Netzwerk gescreenten Verbindungen haben eine gute klärende Wirkung auf seneszente Zellen, ohne das Wachstum normaler Zellen zu beeinträchtigen, und weisen eine starke Selektivität auf.Im Gegenteil: Während ABT-737 seneszente Zellen beseitigt, tötet es auch einige normale Zellen ab, was zu stärkeren Nebenwirkungen führt.

Abbildung 4: Vergleich der Wirksamkeit der untersuchten Verbindungen und herkömmlicher Medikamente
Grau: normale Zellen in der Kontrollgruppe;
Blau: Seneszente Zellen, die nach der Behandlung mit Etoposid gewonnen wurden.
Anschließend führten die Forscher replikative Seneszenz-Experimente mit IMR-90-Zellen der frühen und späten Passage durch und erzielten ähnliche Ergebnisse. Darüber hinaus führten sie Hämolyseexperimente durch, um die biologische Toxizität dieser Medikamente zu testen. Die Ergebnisse zeigen, dassSelbst wenn die Medikamentendosis das Zehnfache der normalen Dosis (100 μM) erreichte, war das durch den Tod der roten Blutkörperchen freigesetzte Hämoglobin im Blut nahezu nicht nachweisbar, was seine biologische Sicherheit beweist.

Abbildung 5: Hämolysetest der untersuchten Verbindungen und herkömmlichen Arzneimittel
Als Kontrollgruppe wurde das Zellpermeabilisierungsmittel Triton X-100 verwendet
Basierend auf den obigen Ergebnissen führten die Forscher In-vivo-Experimente an C57BL/6J-Mäusen mit dem zellselektivsten BRD-K56819078 durch. 14 Tage nach der Arzneimittelinjektion wurden Mäusen Nierenzellen entnommen.Der Gehalt an Seneszenz-assoziierter β-Galaktosidase (SA-β-gal) und die Expression der entsprechenden mRNA wurden beobachtet.
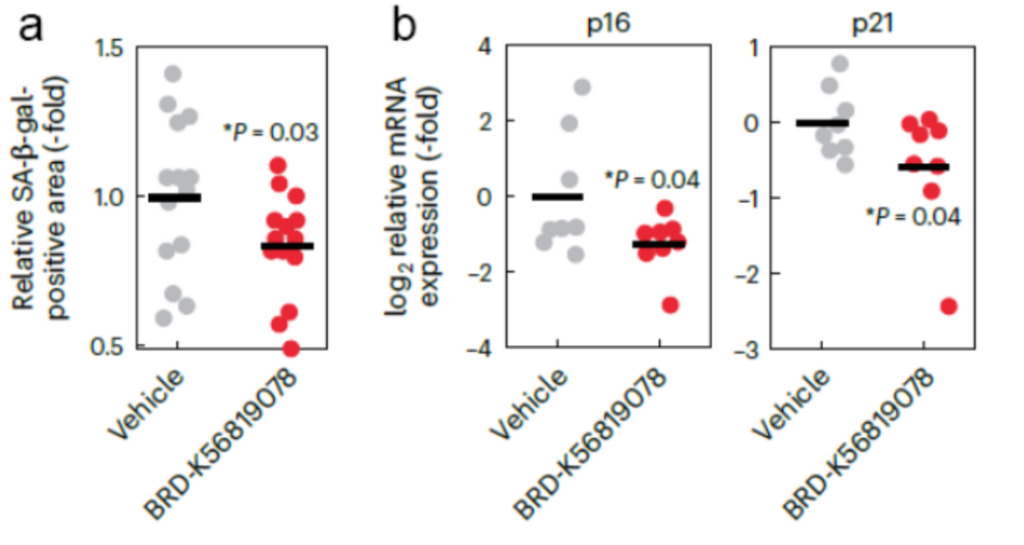
Abbildung 6: Seneszenzindikatoren von Mausnierenzellen
Grau ist die Kontrollgruppe und Rot ist die Versuchsgruppe
a: SA-β-Gal-Gehalt;
b: Expression von alterungsbedingter mRNA
Die Ergebnisse zeigten, dass der Gehalt und die mRNA-Expression von SA-β-gal herunterreguliert waren, was darauf hindeutet, dass BRD-K56819078 seneszente Zellen bei Mäusen effektiv eliminierte.Nach mehreren Screening-Phasen wurde mit dem Chemprop-Modell schließlich ein wirksames und sicheres Anti-Aging-Medikament entwickelt.
Chemprop-Modell: ein guter Helfer für die Arzneimittelentwicklung
Das Chemprop-Modell ist ein Deep-Learning-Modell, das auf einem Graph Neural Network (GNN) basiert. Es verfügt über 5 Schichten und 1.600 verborgene Dimensionen und ist damit komplexer als gewöhnliche GNN-Modelle.
Für jedes Atom und jede Bindung wird in Chemprop ein Eigenvektor basierend auf den folgenden Eigenschaften generiert:
1. Atomare Eigenschaften wie Anzahl der Atome, Anzahl der Bindungen pro Atom, formale Ladung, Chiralität, Anzahl der Bindungen zu Wasserstoffatomen, Hybridisierung, Aromatizität und Atommasse;
2. Chemische Bindungseigenschaften wie Bindungstyp (Einfachbindung, Doppelbindung, Dreifachbindung oder aromatischer Ring usw.), Konjugation, ob ein Ring gebildet wird und dreidimensionale Eigenschaften.
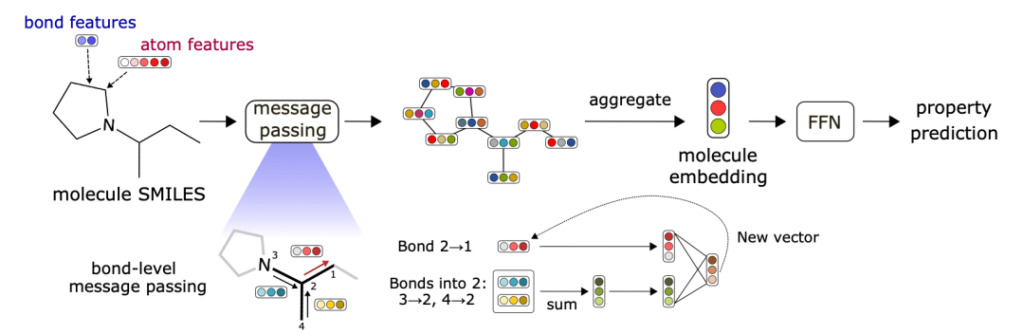
Abbildung 7: Das Hauptgerüst von Chemprop
Das Chemprop-Modell verwendet ein Convolutional Neural Network zur Nachrichtenausbreitung, um die Eigenschaften chemischer Verbindungen zu analysieren.Indem wir die Nachrichten benachbarter Bindungen sammeln, sie dann mit der Gesamtsumme der Bindungen vergleichen und sie schließlich mithilfe einer einzelnen neuronalen Netzwerkschicht mit einer nichtlinearen Aktivierungsfunktion verarbeiten, können wir die Nachricht einer chemischen Bindung erhalten. Nach einer festgelegten Anzahl von Nachrichtenübertragungen werden die Nachrichten des gesamten Moleküls akkumuliert, um den Nachrichtenwert zu erhalten, der das Molekül darstellt. Wenn dieser Wert in ein Feedforward-Neuralnetzwerk eingespeist wird, gibt das Chemprop-Modell einen vorhergesagten Wert aus, der sich auf die Aktivität der Verbindung bezieht.
Derzeit wird das Chemprop-Modell häufig verwendet, um die Arzneimittelaktivität von Verbindungen vorherzusagen und neue Medikamente zu prüfen und zu entwickeln.
Im Jahr 2020 verwendete das MIT Chemprop, um aus mehr als 107 Millionen Molekülen acht antibakterielle Medikamente mit unterschiedlichen Strukturen zu bestehenden Antibiotika herauszufiltern und fand das Medikamentenmolekül Halicin, das bei Mäusen eine antibakterielle Breitbandaktivität aufweist. Im Jahr 2022 nutzte ein Forschungsteam der Capital Medical University Chemprop, um einen möglichen Inhibitor des Gewebeplasminogenaktivators L herauszufiltern und so ein neues Ziel für die Abtötung des neuen Coronavirus zu finden.
Referenzlinks:
[1]https://doi.org/10.26434/chemrxiv-2023-3zcfl
[2]https://www.cell.com/cell/fulltext/S0092-8674(20)30102-1
[3]https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9110316/
Dieser Artikel wurde zuerst auf der öffentlichen HyperAI WeChat-Plattform veröffentlicht~