Command Palette
Search for a command to run...
Um Die Zellalterung Zu Verhindern Und Altersbedingte Krankheiten Zu Vermeiden, Hat Die Universität Edinburgh Drei „KI-Anti-Aging-Rezepte“ Für Zellen Herausgegeben
Inhalte im Überblick:Studien haben gezeigt, dass die Zellalterung eng mit Krankheiten wie Krebs, Typ-2-Diabetes, Osteoarthritis und Virusinfektionen zusammenhängt. Allerdings sind Medikamente zur Beseitigung seneszenter Zellen allmählich zu einem Schwerpunkt der Forschung und Entwicklung geworden. Aufgrund des Mangels an gut charakterisierten molekularen Zielen wurden jedoch nur wenige Anti-Aging-Verbindungen (Senolytics) entdeckt. Kürzlich wurde in der internationalen Fachzeitschrift Nature Communications ein Forschungsergebnis veröffentlicht, in dem Forscher drei neue Arten von Senolytika entdeckten.
Schlüsselwörter:Senolytics Maschinelles Lernen XGBoost
Dieser Artikel wurde zuerst auf der öffentlichen HyperAI WeChat-Plattform veröffentlicht~
Seit der Antike streben die Menschen nach Unsterblichkeit. Überraschend ist, dass Themen wie Anti-Aging und Langlebigkeit in den letzten Jahren aus der mysteriösen und illusorischen Welt der Gesundheitsprodukte in die von der Öffentlichkeit anerkannte Medizin- und Gesundheitswelt gelangen. Es wird allgemein angenommen, dass das Altern ein Prozess ist, bei dem die Körperfunktionen langsam nachlassen. Dieser Prozess ist unumkehrbar, daher bleibt dem Menschen nur, der Natur ihren Lauf zu lassen und alles dem Schicksal zu überlassen. Was viele Menschen jedoch nicht verstehen, ist, dassBereits 2018 erklärte die Weltgesundheitsorganisation im Internationalen Kodex für Krankheiten das Altern zu einer behandelbaren Krankheit.
Innerhalb der weit gefassten Definition des Alterns ist die zelluläre Seneszenz in jüngster Zeit eine der wichtigsten Forschungsrichtungen der Wissenschaft. Zelluläre Seneszenz ist ein Phänomen, das durch das Aufhören der Zellteilung gekennzeichnet ist.Normalerweise kann das menschliche Immunsystem seneszente Zellen wirksam beseitigen, mit zunehmendem Alter lässt diese Beseitigungsfunktion jedoch allmählich nach. Neben einer Verschlechterung des Sehvermögens und eingeschränkter Mobilität besteht auch ein hohes Risiko für die Entstehung von Krebs, Alzheimer und anderen Erkrankungen.
Im Jahr 2015 entdeckten Dr. James L. Kirkland und andere von der Mayo Clinic das erste Anti-Aging-Medikament (Senolytics), das seneszente Zellen entfernen kann.Unter Senolytica versteht man niedermolekulare Verbindungen, die gezielt den Tod seneszenter Zellen herbeiführen. Sein Name leitet sich von Senescence (Altern) und Lytic (Zerstörung) ab.In der neuesten Studie nutzten die Universitäten Edinburgh und Kantabrien maschinelles Lernen, um drei Senolytika – Ginkgetin, Periplocin und Oleandrin – zu entdecken und ihre Anti-Aging-Wirkung in menschlichen Zelllinien zu überprüfen.Die Forschungsergebnisse wurden in der Zeitschrift Nature Communications unter dem Titel „Discovery of Senolytics using machine learning“ veröffentlicht.

Abbildung 1: Dieses Forschungsergebnis wurde in Nature Communications veröffentlicht
Papieradresse:
https://www.nature.com/articles/s41467-023-39120-1#Sec2
Experimentelle Verfahren
Datensatz
Die experimentellen Datensätze stammen aus mehreren Kanälen, darunter akademische Veröffentlichungen und kommerzielle Patente.Zunächst untersuchten die Forscher 58 bekannte Senolytika und anschließend eine Vielzahl von Nicht-Senolytika aus zwei vorhandenen chemischen Bibliotheken, LOPAC-1280 und Prestwick FDA-approved-1280. Der Datensatz kombiniert beides.Insgesamt wurden 2.523 Verbindungen einbezogen, von denen 2,31 TP3T auf Senolytics entfielen.
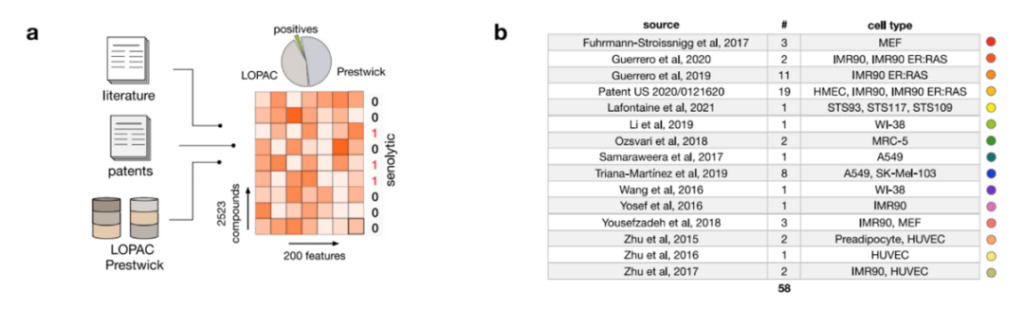
Abbildung 2: Verbindungen, die zum Trainieren von Modellen des maschinellen Lernens verwendet werden
A:Die Trainingsdaten stammen aus mehreren Quellen.
B:58 Quellen für Senolytika, die für das Training verwendet wurden, einschließlich der Anzahl der Verbindungen und Zelllinien für jede Quelle.
Modelltraining
Die Forscher verwendeten den oben genannten Datensatz, um ein Modell zur Identifizierung von Verbindungen mit senolytischen (positiven) Eigenschaften zu trainieren. Zunächst führten die Forscher eine Merkmalsauswahl für den Datensatz durch.Während dieses Prozesses berechneten sie mithilfe des Random-Forest-Modells (RF) die durchschnittliche Gini-Index-Reduktion jedes Merkmals und wählten die 165 wichtigsten Merkmale aus, wodurch die Anzahl der Merkmale und die Komplexität des Modells reduziert wurden.
- Der Gini-Index misst den Grad der Verwirrung der Stichproben in einem Knoten. Je niedriger der Wert, desto reiner sind die Samples im Knoten.
Zweitens entwickelten die Forscher mehrere binäre Klassifizierungsmodelle für Senolytika (zur Identifizierung von Senolytika und Nicht-Senolytika) unter Verwendung der 165 wichtigsten Merkmale und verschiedener Beispieldaten aus dem vollständigen Datensatz.Um die Modelle zu vergleichen und die begrenzte Anzahl an Senolytics-Proben voll auszunutzen, führten die Forscher eine 5-fache Kreuzvalidierung des Datensatzes durch und bewerteten die Modelle anhand von drei Leistungsmetriken: Präzision, Rückruf und F1-Score.
Zunächst konzentrierten sich die Forscher auf Support Vector Machines (SVM) und RF-Modelle, doch Experimente zeigten, dass deren Leistung nicht zufriedenstellend war.Sie bewerteten auch andere Modelle unterschiedlicher Komplexität, darunter logistische Regressoren, naive Bayes-Klassifikatoren und SMOTE, aber die Ergebnisse zeigten, dass die Leistung dieser Modelle nicht so gut war wie die der SVM- und RF-Modelle.
Daher entwickelten die Forscher ein XGBoost-Modell basierend auf der HF-Leistung.Verbessern Sie die Vorhersagekraft durch iteratives Training von Entscheidungsbaummodellen.Wie in Abb. 3b gezeigt, weist das XGBoost-Modell eine verbesserte Präzision, einen verbesserten Rückruf und einen verbesserten F1-Score auf und schneidet von allen betrachteten Modellen am besten ab.
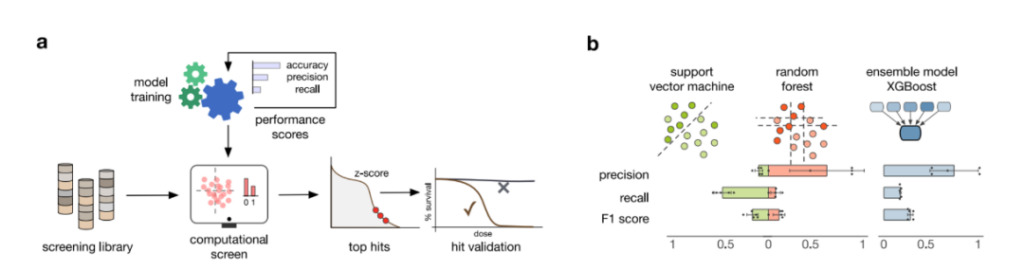
Abbildung 3: Trainieren eines Machine-Learning-Modells
A:Modelltraining, Verbindungsscreening und Ergebnisüberprüfungsprozess unter Verwendung mehrerer Leistungsindikatoren zum Screening geeigneter Modelle.
B:Leistung von 3 Modellen des maschinellen Lernens. Das Balkendiagramm zeigt die durchschnittlichen Leistungskennzahlen, die in einer 5-fachen Kreuzvalidierung berechnet wurden. Die Fehlerbalken stellen eine Standardabweichung dar.
Die Adresse dieses experimentellen Datensatzes wird später mit der offiziellen HyperAI-Website synchronisiert:
https://doi.org/10.5281/zenodo.7870357
Experimentelle Ergebnisse
Zunächst untersuchten die Forscher mehr als 4.340 Verbindungen, um 21 mit potenzieller Anti-Aging-Wirkung zu identifizieren. Anschließend testeten sie diese 21 Verbindungen.Wie in Abbildung 4 gezeigt, haben drei von ihnen die Wirkung, seneszente Zellen zu beseitigen: Periplocin und Oleandrin (zwei Herzglykoside, deren Fähigkeit zur Beseitigung seneszenter Zellen noch nicht bestätigt wurde) und Ginkgetin (eine natürliche, ungiftige Biflavonoidverbindung).
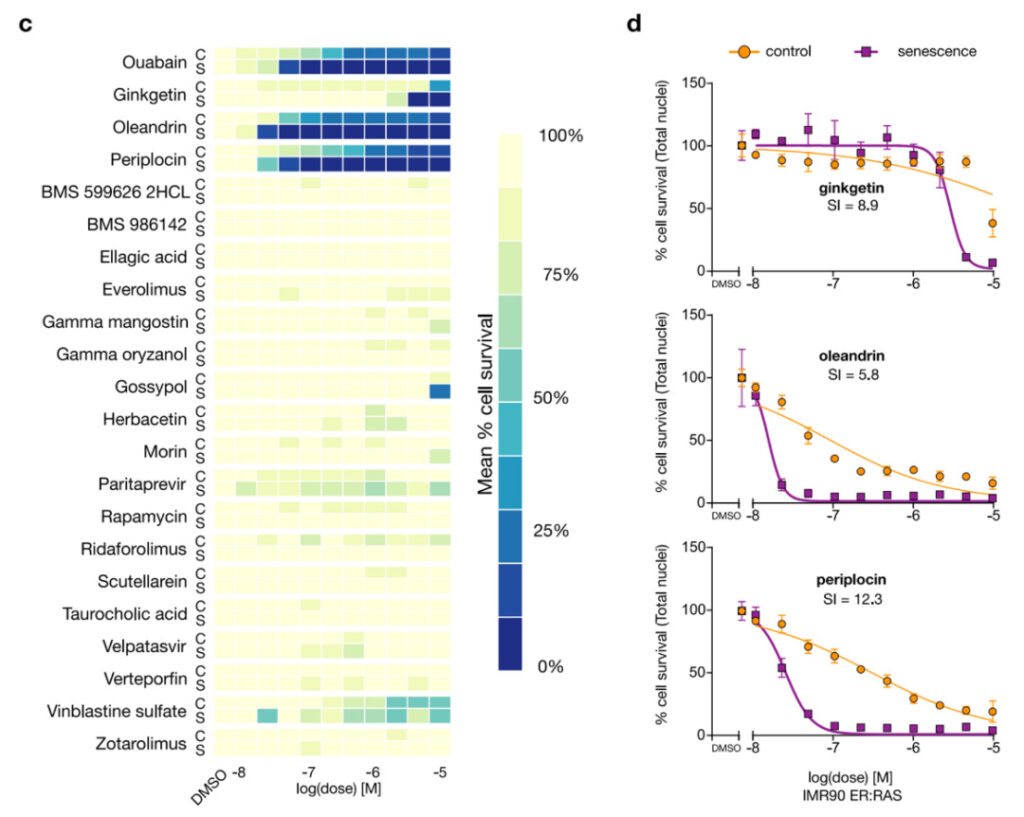
Abbildung 4: Periplocin, Oleandrin und Ginkgetin Wirkt seneszente Zellen beseitigend
C:Experimentelle Überprüfung. Drei der 21 Verbindungen zeigten Anti-Aging-Wirkung: Ginkgetin, Oleandrin und Periplocin; Die Heatmap zeigt den Mittelwert von n = 3 Replikaten. In der Abbildung ist Ouabain ein bekanntes Senolytikum.
D:Dosis-Wirkungs-Kurven von 3 neu entdeckten Anti-Aging-Verbindungen. SI ist der Anti-Aging-Index.
Darüber hinaus wurden während der oben genannten ExperimenteDie Forscher fanden außerdem heraus, dass das neu entdeckte Oleandrin stärkere Anti-Aging-Eigenschaften als Ouabain hatte, insbesondere in niedrigen Konzentrationen.Daher verglichen die Forscher die Anti-Aging-Aktivitäten von Periplocin, Oleandrin und Ouabain bei einer niedrigen Konzentration von 10 nM.
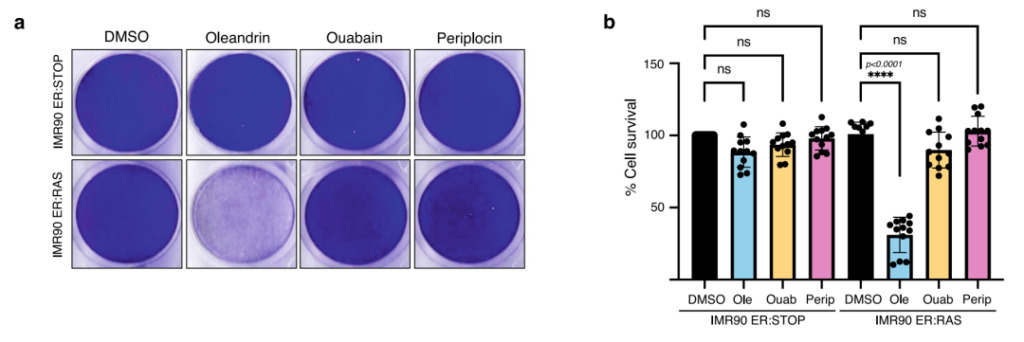
Abbildung 5: Periplocin, Oleandrin und Periplocin Vergleich der Anti-Aging-Leistung bei niedrigen Konzentrationen
A:Die Abbildung zeigt Gewebekulturschalen von IMR90 ER:RAS (seneszente Zellen) und IMR90 ER:STOP (Kontrolle), kultiviert in Gegenwart von 100 nM 4OHT. Während der nächsten 72 Stunden wurden die Zellen mit 10 nM Oleandrin, Ouabain und Periplocin sowie DMSO (Kontrolle) behandelt.
B:Die Zelllebensfähigkeit wurde durch quantitative Analyse beurteilt.
Wie in Abbildung 5b gezeigt, zeigten niedrige Konzentrationen von Ouabain und Periplocin keine signifikante Zytotoxizität in IMR90-ER:STOP und IMR90-ER:RAS.Nach der Behandlung mit Oleandrin war die Überlebensrate der seneszenten Zellen in IMR90-ER:RAS signifikant verringert, was darauf hindeutet, dass Oleandrin bei niedrigeren Arzneimittelkonzentrationen eine stärkere Anti-Aging-Wirkung hat.Basierend auf den oben genannten experimentellen Ergebnissen,Mithilfe maschinellen Lernens lassen sich erfolgreich Anti-Aging-Verbindungen finden. Außerdem wurde Oleandrin entdeckt, das eine stärkere Anti-Aging-Wirkung als bereits vorhandene Anti-Aging-Verbindungen aufweist.
KI-gesteuerte Arzneimittelforschung
KI spielt in jeder Phase der Entwicklung neuer Medikamente eine wichtige Rolle. Derzeit konzentriert sich die Forschung auf die Arzneimittelentdeckung und die präklinische Entwicklungsphase. Diese Studie zeigt das Potenzial der KI in der Arzneimittelentwicklung, insbesondere bei der Behandlung von Krankheiten mit komplexen biologischen Strukturen oder wenigen bekannten molekularen Zielen. Der Autor Diego Oyarzún weist darauf hin:„KI unterstützt uns sehr effektiv bei der Entdeckung neuer Arzneimittelkandidaten, insbesondere in den frühen Phasen der Arzneimittelforschung.“
Vanessa Smer-Barreto, Erstautorin der Studie, betonte die Bedeutung einer engen Zusammenarbeit zwischen Datenwissenschaftlern, Chemikern und Biologen. Sie sagte:„Diese Arbeit entstand aus einer engen Zusammenarbeit zwischen Datenwissenschaftlern, Chemikern und Biologen.Wir haben diese interdisziplinäre Zusammenarbeit genutzt, um ein robustes Modell zu erstellen und Screening-Kosten zu sparen, indem wir für das Modelltraining nur veröffentlichte Daten verwendet haben."Dieses kollaborative Modell bietet neue Möglichkeiten zur Beschleunigung der Anwendung von KI und dürfte Innovation und Entwicklung in der Arzneimittelforschung und -entwicklung vorantreiben.
Obwohl KI in der Forschung und Entwicklung neuer Medikamente Durchbrüche erzielt hat, ist sie derzeit noch mit einigen Herausforderungen konfrontiert, etwa in Bezug auf die Qualität und Zuverlässigkeit der Daten, die Interpretierbarkeit der Algorithmen und die Fähigkeit zur Modellgeneralisierung.Angesichts der kontinuierlichen Weiterentwicklung der Technologie und der zunehmenden Datenressourcen sind die Anwendungsaussichten der KI in der Arzneimittelforschung und -entwicklung nach wie vor sehr breit gefächert.Durch die Stärkung des Datenaustauschs und der interdisziplinären Zusammenarbeit können wir die Vorteile der KI besser nutzen, die Entdeckung und Entwicklung neuer Medikamente beschleunigen und Vorteile für die menschliche Gesundheit erzielen.
Referenzartikel:
[1] http://zixun.69jk.cn/shwx/79532.html
[2]https://en.wikipedia.org/wiki/Cellular_senescence#Characteristics_of_senescent_cells
[3]https://newatlas.com/medical/machine-learning-algorithm-identifies-natural-anti-aging-chemicals/
[4]https://www.sohu.com/a/673349496_121124375
[5]https://www.ed.ac.uk/institute-genetics-cancer/news-and-events/news-2023/ai-algorithms-find-drugs-that-could-combat-ageing
[6]http://www.stcn.com/article/detail/904319.html
Dieser Artikel wurde zuerst auf der öffentlichen HyperAI WeChat-Plattform veröffentlicht~








